НАСЛЕДСТВЕННЫЕ ТРОМБОФИЛИИ ВО ВРЕМЯ БЕРЕМЕННОСТИ — Униклиника — экспертное УЗИ, бережное ведение беременности, щадящая гинекология | UNIKLINIKA
НАСЛЕДСТВЕННЫЕ ТРОМБОФИЛИИ ВО ВРЕМЯ БЕРЕМЕННОСТИ
Введение
Наследственные тромбофилии – это генетические нарушения, которые повышают риск развития тромбоэмболических осложнений. Во время беременности тромбогеный потенциал этих нарушений возрастает из-за гиперкоагуляционного состояния, вызванного физиологическими изменениями:
- Резистентность к активированному протеину С возрастает во втором и третьем триместре
- Активность протеина S снижается из-за уменьшения количества общего и свободного антигенов протеина S
- Повышается количество фибриногена и факторов II, VII, VIII и X
- Повышается уровень и активность фибринолитических ингибиторов, активированного тромбином ингибитора фибринолиза (TAFI), ингибитора активатора плазминогена тип 1 и тип 2 (PAI-1, PAI-2)
Наиболее часто встречающимися документально подтвержденными потенциальными последствиями гиперкоагуляционного состояния являются тромбоз глубоких вен и легочная эмболия. Артериальные тромбозы встречаются редко.
Артериальные тромбозы встречаются редко.
Предполагается небольшая связь с неблагоприятными исходами беременности (повторные спонтанные аборты, гибель плода, мертворождение), однако данные противоречивы. Кроме того, совокупность данных свидетельствует, что терапия антикоагулянтами не предотвращает эти исходы.
Наиболее частыми наследственными тромбофилиями являются мутации фактора V Лейдена (FVL) и протромбинового гена (PGM), которые вместе составляют от 50 до 60% наследственных (первичных) гиперакоагуляционных состояний у представителей европеоидной расы. Дефицит протеина S, протеина С и антитромбина (АТ) составляет большинство остальных случаев.
Существуют и другие мутации, например мутация гена фактора V (не FVL), промоторная мутация гена PAI-1, протеина Z и др., однако их связь с венозным тромбоэмболизмом (ВТЭ) не ясна и скрининг на эти мутации у женщин с ВТЭ или тяжелыми исходами беременности не показан.
Повышения уровня некоторых прокоагулянтных факторов являются фактором риск ВТЭ. Например, повышенная активность фактора VIII является протромботическим фактором риска первого неспровоцированного ВТЭ, однако его повышение не следует рассматривать как наследственную тромбофилию. Кроме того, анализы на ф. VIII не были стандартизированы и нет информации об уровнях ф. VIII во время беременности и протромботического риска.
Например, повышенная активность фактора VIII является протромботическим фактором риска первого неспровоцированного ВТЭ, однако его повышение не следует рассматривать как наследственную тромбофилию. Кроме того, анализы на ф. VIII не были стандартизированы и нет информации об уровнях ф. VIII во время беременности и протромботического риска.
Гомозиготные мутации метилентетрагидрофолат редуктазы (MTHFR) полиморфизмов (C677T, 1298C) является относительно частой причиной повышения уровня гомоцистеина в крови, однако эти мутации не увеличивают риск ВТЭ у беременных или небеременных женщин.
Наследственная тромбофилия увеличивает риск материнского ВТЭ. Было выдвинуто предположение, что они также повышают риск тромбозов в маточно-плацентарном кровотоке. Это приводит к плацента-опосредованным осложнениям (гибель плода, преэклампсия, ЗРП, отслойка плаценты).
Риск ВТЭ
Риск ВТЭ увеличивается во время беременности из-за физиологических изменений в системе коагуляции, а также предрасполагающих физических изменений, таких как застой в венах нижних конечностей из-за компрессии маткой, компрессия левой подвздошной вены правой подвздошной артерией, снижение подвижности, роды (особенно кесарево сечение). Однако абсолютный риск ВТЭ остается примерно 0.1%. На возникновение ВТЭ влияют также дополнительные факторы риска, такие как недавние оперативные вмешательства, возраст более 35 лет, иммобилизация, курение, ожирение.
Однако абсолютный риск ВТЭ остается примерно 0.1%. На возникновение ВТЭ влияют также дополнительные факторы риска, такие как недавние оперативные вмешательства, возраст более 35 лет, иммобилизация, курение, ожирение.
Риск ВТЭ увеличивается у беременных женщин, у которых есть наследственная тромбофилия. По меньшей мере у 50% беременных женщин с ВТЭ есть наследственная тромбофилия. Однако все тромбофилии не дают эквивалентной степени риска тромботических осложнений во время беременности.
Самым важным фактором риска ВТЭ у женщин с наследственной тромбофилией является ВТЭ в анамнезе или в анамнезе у родственников первой линии. В случае FVL, семейный или личный анамнез ВТЭ повышает риск с 0.5-1.2% до 10%.
Вероятность ВТЭ у женщин с наследственной тромбофилией
| Распространенность в общей популяции | Риск ВТЭ во время беременности (у женщин без анамнеза ВТЭ) | Риск ВТЭ во время беременности у женщин с анамнезом ВТЭ | Процент всех ВТЭ во время беременности | |
| Фактор V Лейден гетерозигота | 1-15% | 0. 5-1.2% 5-1.2% |
10% | 40% |
| Фактор V Лейден гомозигота | <1% | 4% | 17% | 2% |
| Ген протромбина гетерозигота | 2-5% | <0.5% | >10% | 17% |
| Ген протромбина гомозигота | <1% | 2-4% | >17% | 0.5% |
| Фактор V Лейден/протромбин двойная гетерозигота | <1% | 4-5% | >20% | 1-3% |
| Дефицит антитромбина | 0.02% | 3-7% | 40% | 1% |
| Дефицит протеина С | 0.2-0.4% | 0.1-0.8% | 4-17% | 14% |
| Дефицит протеина S | 0.03-0.13% | 0.1% | 0-22% | 3% |
Однако, есть несколько проспективных исследований, которые сообщили о меньшей вероятности ВТЭ, чем это было показано в ретроспективных исследования. Оба исследования были недостаточными, чтобы исключить умеренную связь между FVL и ВТЭ, но они подчеркивают низкий риск тромбоза у бессимптомных (без анамнеза ВТЭ) носителей мутации.
Риск осложнений беременности
Маловероятно, что наследственная тромбофилия является основной причиной неблагоприятных исходов беременности. Большинство проспективных исследований не нашли связи, хотя ретроспективные исследования показали умеренную связь между гетерозиготностью FVL (и, возможно, гетерозиготностью PGM и дефицитом белков C и S) и потерей плода после 10 недель гестации и, особенно, для неповторяющихся потерь плода после 20 недель гестации. Это говорит о том, что любая связь ограничена группами высокого риска и является умеренной. Малые исследования типа случай-контроля или ретроспективные когортные исследования с участием гетерогенных популяций часто сообщали о противоречивых результатах, отчасти из-за влияния различных факторов, которые часто не анализируются соответствующим образом. Систематические ошибки, связанные с предпочтительной публикацией положительных результатов исследования, тоже имеют место.
Спонтанный аборт, гибель плода или мертворождение.
Хотя большинство, (но не все), крупные проспективные исследования не обнаружили никакой связи между наследственной тромбофилией и ранней или поздней гибелью плода, исследования типа случай-контроль и ретроспективные когортные исследования часто сообщали о связи, особенно с поздней потерей плода. Cовокупность данных свидетельствует, что терапия антикоагулянтами не предотвращает эти исходы.
В 2003 году был проведен мета-анализ 31 исследований типа случай-контроль и одномоментных исследований и подсчитали отношение шансов (OR) с 95% доверительным интервалом (CI).
- FVL был ассоциирован с ранним (до 13 недель) (OR 2.01, 95% CI 1.13-3.58) и поздним (после 22 недель) (OR 7.83, 95% CI 2.83-21.7) привычным невынашиванием и поздней (после 19 недель) неповторяющейся потерей плода (OR 3.26, 95% CI 1.82-5.83).
- Мутация гена протромбина была связана с ранним привычным невынашиванием (OR 2.
 56, 95% CI 1.04-6.29) и поздней неповторяющейся потерей плода (OR 2.30, 95% CI 1.09-4.87).
56, 95% CI 1.04-6.29) и поздней неповторяющейся потерей плода (OR 2.30, 95% CI 1.09-4.87).
Европейское Проспективное Когортное Исследование Тромбофилии (EPCOT) оценило 843 женщины с тромбофилиями, у 571 из которых было 1524 беременностей по сравнению с 541 женщиной из контрольной группы, 395 из которых имели 1019 беременностей. Они определили выкидыш, как потерю плода до 28 недель гестации и мертворождение как потерю плода после 28 недель.
- Общая частота потери плода была выше у женщин с тромбофилией (29,4 против 23,5%, OR 1,35, 95% CI 1,01-1,82).
- Тем не менее, ОR был статистически значимым только для мертворождения (OR 3.6, 95% CI 1.4-9.4 для мертворождения, против OR 1.27, 95% 0,94-1,71 для выкидыша).
- ОR для мертворождения у женщин с множественными тромбофилиями составлял 14,3 (95% CI 2,4-86,0), что указывало на дозозависимый эффект.
- ОR для мертвождения с различными дефектами: дефицит антитромбина 5.2 (95% CI 1.5-18.1), дефицит протеина С 2.
 3 (95% CI 0.6-8.3), дефицит протеина S 3.3 (95% CI 1.0-11.3), и FVL 2.0 (95% CI 0.5-7.7).
3 (95% CI 0.6-8.3), дефицит протеина S 3.3 (95% CI 1.0-11.3), и FVL 2.0 (95% CI 0.5-7.7). - Не было выявлено статистической значимой связи между тромбофилией в целом или отдельными тромбофильными дефектами (множественные мутации, мутации гена протромбина, дефицит протеина С или S, FVL) и выкидышами. Единственным исключением был дефицит антитромбина.
Несмотря на то, что есть различия между метаанализом и исследованием EPCOT они оба демонстрируют более сильную связь между тромбофилией и поздними потерями беременности.
=================
FVL и мутация гена протромбина
Связь между FVL, мутацией гена протромбина и поздней потерей беременности была изучена в следующих исследованиях:
- В исследовании типа случай-контроль было обследовано 5001 беременных женщин и установлено, что у FVL значительная связь с мертворождением (OR 10.9; 95% CI 2.07- 56.94), и незначительная связь с ранней потерей плода (OR 1.
 76; 95% CI 0.85-3.65). При мутации гена протромбина OR для мертворождаемости и ранней потери плода статистически незначимо.
76; 95% CI 0.85-3.65). При мутации гена протромбина OR для мертворождаемости и ранней потери плода статистически незначимо. - В другом исследовании было обследовано 102 женщины с потерей беременности, у 47 из которых в анамнезе мертворождение. Существует значительная связь между FVL, мутацией гена протромбина и мертворождением. Не было выявлено статистической связи FVL, мутации гена протромбина с привычным невынашиванием.
- В исследовании Университетской клиники Нима выявлено, что у женщин гетерозиготных FVL и PGM без лечения с тремя последовательными необъяснимыми потерями беременности до 10 недель гестации сходный уровень повторяющихся выкидышей с женщинами без тромбофилий (14 против 19.2%), однако по мере развития беременности, у таких женщин выше уровень смерти плода (8,8 против 2.3%)
- Присутствие одной или более тромбофильной мутации защищало от привычного невынашивания до 10 недель беременности OR 0.55, 95% CI 0.33-0.92 для одной и OR 0.48, 95% CI 0.29-0.78 для нескольких мутаций соответственно)
- Наличие одной или нескольких тромбофильных мутаций связано с повышенным риском потери беременности после 10 недель (OR 1,76, 95% CI 1,05-2,94 для одной и OR 1,66, 95% CI 1,03-2,68 для множественных тромбофилий соответственно) , Тромбофилия также была связана с повышенным риском потери плода после 14 недель (OR 3.
 41, 95% CI 1,9-6,1 для одной и OR 3,86, 95% CI 2,26-6,59 для нескольких тромбофилий соответственно).
41, 95% CI 1,9-6,1 для одной и OR 3,86, 95% CI 2,26-6,59 для нескольких тромбофилий соответственно). - У женщин, только с эуплоидными потерями в первом триместре, с большей вероятностью не было выявлено тромбофилии, чем у женщин, с анеуплоидными потерями (OR 1.03, 95% CI 0.38-2.75).
Парадоксальное наблюдение о снижении риска ранней потери беременности у матерей с тромбофилией не является неожиданным. Ранние сроки беременности обычно связаны с низким уровнем кислорода (давление кислорода 17+/- 6.9 мм.рт. ст и 60.7 +/- 8.5 с 8 по 10 неделю и на 13 неделе соответственно), закупоркой трофобластом межворсинчатого пространства и низким уровнем маточно-плацентарного кровотока (по Доплеру). Кислород может оказывать негативное влияние в эмбриональном периоде. Таким образом, влияние материнской тромбофилии на маточно-плацентарный кровоток оказывает негативное влияние в более позднем, а не в первом триместре беременности.
- Связь между ЗРП и тромбофилией не выявлена.

- Тромбофилия не ассоциирована с повышенным риском развития прэклампсии.
- Не было выявлено связи между отслойкой плаценты и тромбофилией.
Риск наследственной тромбофилии у плода:
Плод, с наследственной тромбофилией находится в группе риска возникновения тяжелых клинических состояний из-за тромбоза плодовой части плаценты. Сообщалось о гибели плода, ЗРП, преждевременных родах, перинатальном инсульте, церебральном параличе, однако в эти отчеты были включены только несколько пострадавших пациентов.
Отбор пациентов для скрининга:
Рутинный скрининг не рекомендуется из-за низкой частоты в популяции и отсутствия безопасного, экономически эффективного долгосрочного метода профилактики тромбоэмболии.
Американский колледж акушеров и гинекологов рекомендует скрининг на тромбофилию, когда результаты будут влиять на ведение беременности / послеродового периода, включая (1) анамнез ВТЭ, с или без повторяющихся факторов риска и отсутствием
тестирования на тромбофилию в анамнезе, или (2) родственник первой степени с анамнезом наследственной тромбофилии высокого риска.
Авторы рекомендуют проводить скрининг в таких случаях:
- Анамнез ВТЭ, связанный с временным фактором риска (например перелом, оперативное вмешательство или длительная иммобилизация). Результаты скрининга полезны, поскольку те, у кого нет наследственной тромбофилии, имеют низкий риск повторного тромбоза и не требуют послеродовой тромбопрофилактики, тогда как женщины с тромбофилией подвергаются более высокому риску ВТЭ. Величина риска и тактика ведения зависит от дефекта.
- Анамнез идиопатического ВТЭ, рецидивирующего ВТЭ, или ВТЭ связанного с использованием КОК или беременностью. Эти женщины подвергаются относительно высокому риску рецидива тромбоза и должны получать послеродовую профилактическую антикоагулянтную терапию независимо от наличия тромбофилии. Тем не менее, скрининг по-прежнему полезен для этой группы, поскольку присутствие и тип тромбофилии влияют на дозу антикоагулянтов. Женщины, у которых нет лабораторных доказательств наследственной тромбофилии, получают профилактическую дозу.

- Нет анамнеза ВТЭ, но есть родственник первой линии с анамнезом тромбофилии высокого риска. Обоснованием такого тестирования является то, что дородовая и послеродовая профилактика применяется, если бессимптомная пациентка оказывается носителем одного из наиболее тромбогенных дефектов (например, дефицит АТ, двойная гетерозиготность или гомозиготность для FVL и PGM). Если бессимптомная пациентка является носителем менее тромбогенных дефектов (например, гетерозиготного FVL), тромбопрофилактика может быть показана при присутствии других факторов риска (например, кесарево сечение, длительная иммобилизация, ожирение) или родственника первой линии с ВТЭ до 50 лет.
Скрининг не рекомендуется:
- Женщинам с анамнезом привычного невынашивания, ранней потерей беременности, отслойки, ЗРП или преэклампсии. Отсутствуют доказательства причинно-следственной связи между тромбофилией и этими состояниями, а также доказательства, что применение антикоагулянтов улучшит исход беременности.

- Парам с неудачными попытками ЭКО. Наследственная тромбофилия не связана со способностью к зачатию или с нарушениями имплантации. Гетерозиготность FVL связана со значительно коротким средним временем до зачатия (11 недель) по сравнению с не-носителями (23 недели) (ОR 1,94, 95% CI 1,03-3,65). Наследственные тромбофилии связаны с более высоким коэффициентами рождаемости после вспомогательных репродуктивных технологий.
Лабораторное тестирование:
Лабораторное тестирование проводится не менее чем через шесть недель после тромботического события, если пациентка не беременна и не принимает антикоагулянтную или гормональную терапию. В идеале, гемостаз не оценивается ранее, чем через три месяца после родов и после прекращения грудного вскармливания.
Это связано с:
- Гепарин индуцирует снижение уровня АТ. Варфарин снижает концентрацию протеина С и S, затрудняя интерпретацию результатов.
- Беременность связана с повышенной резистентностью к активированному протеину C (APC) в анализах коагуляции «первого поколения» из-за увеличения уровней фактора VIII и снижения уровня протеина S.
 Ложноположительные результаты в таком случае, были не редкостью. Хотя большинство клинических лабораторий, которые проводят тесты на устойчивость APC для проверки наличия мутации FVL, в настоящее время используют тесты «второго поколения».
Ложноположительные результаты в таком случае, были не редкостью. Хотя большинство клинических лабораторий, которые проводят тесты на устойчивость APC для проверки наличия мутации FVL, в настоящее время используют тесты «второго поколения». - Уровни антигена свободного и общего протеина S, а также активности протеина S значительно снижаются при нормальной беременности, а четкий порог для диагностики дефицита протеина S не был точно установлен
Тестовые панели:
- Для скрининга дефицита АТ: лучший тест для лабораторного скрининга – анализ кофактора АТ-гепарина
- Резистентность активированного протеина С и FVL – наличие FVL можно оценить, используя коагуляционные тесты 2 поколение. Пациенты с низким уровнем резистентности активированного протеина С должны быть генотипированы на наличие FVL мутации. В качестве альтернативы, пациенты могут непосредственно проходить генотитипирование на FVL.
- Дефицит протеина S. Определение свободного протеина S это предпочтительный вариант скрининга.
 Тестирование не должно проводиться во время беременности. И в идеале, не должно проводиться при приеме антикоагулянтной терапии. Уровни общего или свободного протеина С < 65 МЕ/dL считаются дефицитом. Однако в проспективном семейном когортном исследовании с участием 1143 родственников с различными тромбофильными дефектами только молодые родственники с уровнем протеина S меньше, чем 5-й перцентиль (<41 МЕ / дл) или меньше, чем 2,5-й перцентиль (<33 МЕ / дл) были подвержены более высокому риску возникновения первого венозного тромбоза по сравнению с таковыми с нормальным уровнем(> 91 МЕ / дл). В общей популяции людей с первым ВТЭ, но без семейного анамнеза тромбофилии, увеличение OR для первого эпизода ВТЭ было обнаружено только в том случае, если уровень свободного протеина S составлял <33 МЕ / дл.
Тестирование не должно проводиться во время беременности. И в идеале, не должно проводиться при приеме антикоагулянтной терапии. Уровни общего или свободного протеина С < 65 МЕ/dL считаются дефицитом. Однако в проспективном семейном когортном исследовании с участием 1143 родственников с различными тромбофильными дефектами только молодые родственники с уровнем протеина S меньше, чем 5-й перцентиль (<41 МЕ / дл) или меньше, чем 2,5-й перцентиль (<33 МЕ / дл) были подвержены более высокому риску возникновения первого венозного тромбоза по сравнению с таковыми с нормальным уровнем(> 91 МЕ / дл). В общей популяции людей с первым ВТЭ, но без семейного анамнеза тромбофилии, увеличение OR для первого эпизода ВТЭ было обнаружено только в том случае, если уровень свободного протеина S составлял <33 МЕ / дл. - Дефицит протеина С — Функциональные анализы обычно проводят с помощью амидолитических методов с использованием змеиного яда для активации протеина С; также допустимы функциональные анализы с использованием конечного времени свертывания крови.

- Мутации протромбина G202010A — диагностика мутации протромбина G20210A методом ПЦР проста, поскольку мутация включает одно базовое изменение (точечную мутацию), которое может быть обнаружено генетическим тестированием, которое не зависит от интеркуррентной болезни или приема антикоагулянтов.
- Антифосфолипидные антитела — диагноз антифосфолипидного синдрома (AФС) основан на сочетании клинических признаков и лабораторных данных. Тестирование у пациентов с подозрением AФС включает определение IgG и IgM-антител к кардиолипину и бета2-гликопротеину I и функциональный анализ для определения волчаночного антикоагулянта.
Тесты, которые не следует проводить
Авторы рекомендуют не проводить следующие тесты как часть скрининга на тромбофилию:
- Уровень гомоцистеина
- Полиморфизм MTHFR (C677T, A1298C)
- PAI-1 полиморфизм.
В США уровень гомоцистеина снизился, с тех пор как стали проводить обогащение
муки фолатами, таким образом меньшее количество пациентов с ВТЭ имеют высокий уровень гомоцистеина. Беременным женщинам регулярно назначают витамины, содержащие фолиевую кислоты, чтобы снизить риск возникновения дефектов нервной трубки. Кроме того, высокий уровень гомоцистеина, как известно, является более слабым фактором риска для ВТЭ или артериального тромбоза, чем сообщается в более ранних исследованиях (OR 1.2-1.6 по сравнению с 2), а интервенционные исследования с добавлением витамина B, хотя и у небеременных пациентов, не показывают сокращения уровня артериальных или венозных тромботических событий.
Беременным женщинам регулярно назначают витамины, содержащие фолиевую кислоты, чтобы снизить риск возникновения дефектов нервной трубки. Кроме того, высокий уровень гомоцистеина, как известно, является более слабым фактором риска для ВТЭ или артериального тромбоза, чем сообщается в более ранних исследованиях (OR 1.2-1.6 по сравнению с 2), а интервенционные исследования с добавлением витамина B, хотя и у небеременных пациентов, не показывают сокращения уровня артериальных или венозных тромботических событий.
Так же не рекомендуется проводить тестирование на полиморфизмы MTHFR (C677T, A1298C). Гомозиготность для этих генетических вариантов является относительно распространенной причиной умеренно повышенного уровня гомоцистеина плазмы в общей популяции, часто возникающей в связи с уровнями фолата сыворотки на нижней границе нормы. Высококачественные эпидемиологические исследования не обнаружили значительного увеличения риска ВТЭ среди лиц, гомозиготных по полиморфизмам MTHFR.
Распространенность полиморфизма PAI-1 (4G / 5G) очень высока (приблизительно 50 процентов) у общей популяции и 20-25 процентов из них являются гомозиготными 4G / 4G «тромбогенного» генотипа.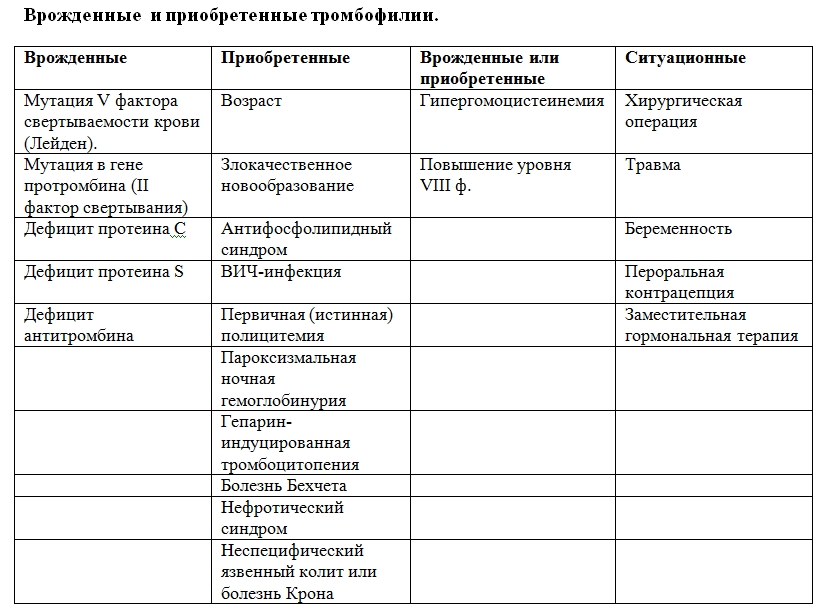 Это связано с двукратным увеличением уровня PAI-1. По мнению автора, имеющиеся исследования, связывающие эти генотипы с преэклампсией и другими неблагоприятными результатами беременности, имеют много ограничений и не дают никаких доказательств для тестирования женщин с неблагоприятным исходом беременности.
Это связано с двукратным увеличением уровня PAI-1. По мнению автора, имеющиеся исследования, связывающие эти генотипы с преэклампсией и другими неблагоприятными результатами беременности, имеют много ограничений и не дают никаких доказательств для тестирования женщин с неблагоприятным исходом беременности.
*********************
Профилактика ВТЭ
Дородовая профилактика
В идеале антикоагулянтная терапия должна быть начата в первом триместре, так как риск ВТЭ увеличивается на ранних сроках беременности. Антикоагулянтная терапия должна быть прекращена при начале родов или до запланированной индукции или кесарева сечения для минимизации риска геморрагических осложнений, в том числе связанных с применением нейроаксиальной анестезии;
Послеродовая профилактика
Схема приема антикоагулянтов в послеродовом периоде должна оставаться такой же. В некоторых случаях рекомендуют даже более агрессивные схемы лечения в послеродовом периоде. Иногда послеродовая профилактика показана женщинам, которые не принимали антикоагулянты до родов. После вагинальных родов гепарин можно применять через 4-6 часов. После кесаревого сечения – через 6-12 часов. Варфарин можно начинать применять сразу после родов.
Иногда послеродовая профилактика показана женщинам, которые не принимали антикоагулянты до родов. После вагинальных родов гепарин можно применять через 4-6 часов. После кесаревого сечения – через 6-12 часов. Варфарин можно начинать применять сразу после родов.
Антикоагулянтная терапия
| Дородовая терапия | Послеродовая терапия | |
| Тромбофилия низкого риска с анамнезом ВТЭ или тромбофилия высокого риска без анамнеза ВТЭ | Антикоагулянтная терапия (средняя доза) | Антикоагулянтная терапия (средняя доза) |
| Тромбофилия низкого риска без анамнеза ВТЭ | Наблюдение без антикоагулянтной терапии. Антикоагулянтная терапия может быть назначена некоторым пациентам с дополнительными факторами риска тромбоза. | Профилактическая антикоагулянтная терапия для женщин после кесаревого сечения |
| Тромбофилия высокого риска с анамнезом ВТЭ при приеме антикоагулянтов | Антикоагулянтная терапия (терапевтическая доза) | Антикоагулянтная терапия (терапевтическая доза) |
Использование гепарина во время беременности
| Гепарин | Доза | Доза |
| Низкомолекулярный гепарин (НМГ) | Профилактическая доза | Эноксипарин 40 мг п/к 1 раз в сутки |
| Дальтепарин 5000 ед п/к 1 раз в сутки | ||
| Средняя доза | Эноксапарин 40 мг п/к 1 раз в сутки увеличивая до 1 мг/кг 1 раз в сутки | |
| Дальтепарин 5000 ед п/к 1 раз в сутки увеличивая до 100 ед/кг 1 раз в сутки | ||
| Терапевтическая доза | Эноксапарин 1 мг/кг каждые 12 часов | |
| Дальтепарин 100 ед/кг каждые 12 часов | ||
| Нефракционированный гепарин (НФГ) | Профилактическая доза | 5000 ед п/к дважды в день |
| Средняя доза | 1 триместр: 5000-7000 ед каждые 12 часов | |
| 2 триместр: 7500-10000 ед каждые 12 часов | ||
| 3 триместр: 10000 ед каждые 12 часов | ||
| Терапевтическая доза | Дозируйте каждые 12 часов, чтобы уровень АЧТВ был в 1. 5-2 раза выше базового через 6 часов после дозы. 5-2 раза выше базового через 6 часов после дозы. |
Послеродовая антикоагулянтная терапия может быть начата через 4-6 часов после вагинальных родов или 6-12 часов после кесаревого сечения если нет выраженного кровотечения или риска выраженного кровотечения.
К тромбофилии низкого риска отнесены женщины, гетерозиготы FVL или PGM, женщины с дефицитом протеина С или протеина S
К тромбофилии высокого риска отнесены женщины с дефицитом антитромбина, гомозиготы FVL или PGM, двойные гетерозиготы FVL и PGM.
Для женщин с тромбофилией высокого риска и анамнезом неспровоцированного ВТЭ или повторяющегося ВТЭ и длительного приема антикоагулянтов до беременности рекомендуется назначение терапевтических доз НМГ и при наличии дефицита антитромбина лечение концентратом антитромбина в перипартальном периоде.
Другие рекомендации:
Американская коллегия специалистов в области торакальной медицины (АССР) рекомендует учитывать личный и семейный анамнез при лечении таких пациентов. Для женщин с тромбофилией высокого риска без анамнеза ВТЭ они рекомендуют только послеродовую антикоагулянтную терапию. Если в личном или семейном анамнезе есть ВТЭ – дородовую и послеродовую антикоагулянтную терапию.
Для женщин с тромбофилией высокого риска без анамнеза ВТЭ они рекомендуют только послеродовую антикоагулянтную терапию. Если в личном или семейном анамнезе есть ВТЭ – дородовую и послеродовую антикоагулянтную терапию.
ACOG также учитывает личный и семейный анамнез ВТЭ
Рекомендации ACOG
| Дородовая терапия | Послеродовая терапия | |
| Тромбофилия низкого риска без анамнеза ВТЭ | Наблюдение без антикоагулянтной терапии | Послеродовая антикоагулянтная терапия для пациентов с дополнительными факторами риска |
| Тромбофилия низкого риска с семейным анамнезом ВТЭ | Наблюдение без антикоагулянтной терапии | Послеродовая антикоагулянтная терапия средними дозами НМГ/НФГ |
| Тромбофилия низкого риска с одним эпизодом ВТЭ в анамнезе, не получающие постоянную антикоагулянтную терапию | Профилактическая или средняя доза НМГ/НФГ или наблюдение без антикоагулянтной терапии | Послеродовая антикоагулянтная терапия средними дозами НМГ/НФГ |
| Тромбофилия высокого риска без анамнеза ВТЭ | Наблюдение без антикоагулянтной терапии или профилактическая доза НМГ/НФГ | Послеродовая антикоагулянтная терапия |
| Тромбофилия высокого риска с одним эпизодом ВТЭ в анамнезе или семейным анамнезом ВТЭ не получающие постоянную антикоагулянтную терапию | Профилактическая, средняя или отрегулированная доза НМГ/НФГ | Послеродовая антикоагулянтная терапия, средняя или отрегулированная доза НМГ/НФГ в течение 6 недель (терапевтическая доза должны быть такая же, как и во время беременности) |
| Нет тромбофилии, но в анамнезе ВТЭ, связанный с временным фактором риска, которого сейчас нет (не включая беременности и прием эстрогенов) | Наблюдение без антикоагулянтной терапии | Послеродовая антикоагулянтная терапия |
| Нет тромбофилии, но в анамнезе ВТЭ связанный с беременностью или приемом эстрогенов | Профилактическая доза НМГ/НФГ | Послеродовая антикоагулянтная терапия |
| Нет тромбофилии, но в анамнезе идиопатический ВТЭ, не получающие постоянную антикоагулянтную терапию | Профилактическая доза НМГ/НФГ | Послеродовая антикоагулянтная терапия |
| Тромбофилия или нет тромбофилии, в анамнезе с двумя или более эпизодами ВТЭ не получающие постоянную антикоагулянтную терапию | Профилактическая или терапевтическая доза НМГ/НФГ | Послеродовая антикоагулянтная терапия или терапевтическая доза НМГ/ГФН в течение 6 недель |
| Тромбофилия или нет тромбофилии, в анамнезе с двумя или более эпизодами ВТЭ получающие постоянную антикоагулянтную терапию | Терапевтическая доза НМГ или НФГ | Возобновление длительной антикоагулянтной терапии. |
Режим антикоагулянтной терапии
| Доза | |
| Профилактическая доза НМГ | Эноксапарин 40 мг п/к один раз в сутки |
| Дальтепарин 5000 ед п/к один раз в сутки | |
| Тинзапарин 4500 ед п/к один раз в сутки | |
| Терапевтическая доза НМГ (также терапевтической отрегулированная по весу) | Эноксапарин 1 мг/кг каждые 12 часов |
| Дальтепарин 200 ед/кг один раз в сутки | |
| Тинзапарин 175 ед/кг п/к один раз в сутки | |
| Дальтепарин 100 ед/кг каждые 12 часов | |
| Мини-профилактическая доза НФГ | НФГ, 5000 ед п/к каждые 12 часов |
| Профилактическая доза НФГ | НФГ, 5000-10000 ед п/к каждые 12 часов |
| В 1 триместре: 5000-7500 ед п/к каждые 12 часов | |
| Во 2 триместре: 7500-10000 ед п/к каждые 12 часов | |
| В 3 триместре: 10000 ед п/к каждые 12 часов за исключением случаев повышения АЧТВ | |
| Терапевтическая доза НФГ (также терапевтической отрегулированная по весу) | НФГ 10000 ед или больше п/к каждые 12 часов. (целевой уровень АЧТВ 1.5-2.5 через 6 часов после инъекции) (целевой уровень АЧТВ 1.5-2.5 через 6 часов после инъекции) |
| Послеродовая антикоагулянтная терапия | Профилактическая доза НМГ/НФГ от 4 до 6 недель |
| или | |
| Антагонист витамина К от 4 до 6 недель с целевым МНО от 2 до 3, с перекрестной терапией НМГ или НФГ до тех пор, пока МНО не будет 2.0 или более. |
Профилактика осложнений беременности:
Как уже было указано выше, нет достоверных доказательств связи между наследственной тромбофилией и преэклампсией, ЗРП, отслойкой плаценты. Поэтому, антикоагулянтная терапия не рекомендуется женщинам для профилактики этих состояний.
Потеря плода
Существует некоторые доказательства ассоциации между наследственной тромбофилией и поздней потерей плода. Хотя совокупность доказательств не поддерживает профилактическую антикоагулянтную терапию для улучшения исхода беременности у подавляющего большинства пациентов, авторы рассматривают антикоагулянтную терапию на индивидуальной основе после учета медицинского и акушерского анамнеза, гистопатологии плаценты и других потенциальных причин неблагоприятного исхода беременности. Например, можно предложить лечение средней или терапевтической дозой НМГ пациентке с наследственной тромбофилией и потерями плода в третьем триместра, связанными с децидуальной васкулопатией и мультифокальным инфарктом плаценты, но без анамнеза преэклампсии или ВТЭ. Эти случаи встречаются редко, и нет четких доказательств такого подхода; снижение риска ВТЭ является дополнительным преимуществом.
Например, можно предложить лечение средней или терапевтической дозой НМГ пациентке с наследственной тромбофилией и потерями плода в третьем триместра, связанными с децидуальной васкулопатией и мультифокальным инфарктом плаценты, но без анамнеза преэклампсии или ВТЭ. Эти случаи встречаются редко, и нет четких доказательств такого подхода; снижение риска ВТЭ является дополнительным преимуществом.
Наблюдение за плодом и срок родов
Учитывая, небольшое повышение риска мертворождения у беременных с тромбофилией, которые получают или не получают профилактическую антикоагулянтную терапию, авторы рекомендуют еженедельную оценку состояния плода при помощи нестрессового теста, с 36 недель беременности, родоразрешение на 39 неделе беременности при отсутствии акушерских осложнений, требующих более ранних родов. Для женщин, которые были на антикоагулянтной терапии, гепарин следует прекратить до индукции родов, чтобы снизить риск материнского кровотечения, включая нейроаксиальную гематому у пациентов, которые предпочитают нейроаксиальную анестезию.
Выводы и рекомендации
- Женщины с наследственными тромбофилиями подвергаются более высокому риску тромбоэмболических осложнений.
- Исследования выявили связь между некоторыми типами тромбофилии и неблагоприятными исходами беременности, но абсолютный риск мал и значительно варьируется в разных исследованиях. Наиболее крупные проспективные когортные исследования не смогли установить последовательную связь между наследственными тромбофилиями и неблагоприятными исходами беременности в группах с низким уровнем риска.
- Авторы проводят скрининг на тромбофилию, когда результаты повлияют на выбор терапии и избегают скрининга, когда лечение показано из-за специфических факторов риска пациента. К подходящим кандидатам для скрининга относятся женщины в репродуктивном возрасте с анамнезом ВТЭ, связанным с временным фактором риска (например, перелом бедренной кости, хирургическое вмешательство или длительная иммобилизация) и бессимптомные женщины (без предшествующего ВТЭ), планирующие беременность, у которой есть родственник первой степени с ВТЭ до 50 лет и тромбофилией высокого риска.
 По возможности, лабораторные исследования должны проводиться через некоторое время после тромботического события, не во время беременности и приема антикоагулянт ной терапии.
По возможности, лабораторные исследования должны проводиться через некоторое время после тромботического события, не во время беременности и приема антикоагулянт ной терапии. - Авторы не рекомендуют скрининг наследственной тромбофилии у женщин с привычным невынашиванием или потерей плода, ЗРП или преэклампсией (класс 1B). Есть все больше доказательств, что введение антикоагулянтов не улучшает исход беременности.
- Авторы рекомендуют не проводить профилактическую антикоагулянтную терапию во время беременности для профилактики плацентарно-опосредованных осложнений беременности.
- При отсутствии акушерских осложнений таких как преэклампсия, ЗРП или отслойка плаценты, авторы рекомендуют еженедельно оценивать состояние плода при помощи нестрессового теста после 36 недель гестации и родоразрешение в сроке 39 недель.
причины появления, симптомы заболевания, диагностика и способы лечения
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Тромбофилия: причины появления, симптомы, диагностика и способы лечения.
Определение
Тромбофилия – наследственные или приобретенные состояния, которые характеризуются чрезмерной склонностью организма к образованию тромбов в кровеносных сосудах. Под тромбообразованием понимают формирование сгустков крови в местах повреждения сосудистой стенки. Это физиологический процесс, который препятствует истечению крови в местах повреждений сосуда.
Однако если тромбообразование становится избыточным или само является причиной повреждения сосудистой стенки, речь идет о патологическом тромбозе. Таким образом, тромбоз – патология, вызванная аномальным формированием тромбов в кровеносных сосудах.
Причины появления тромбофилии
Поддержание крови в жидком состоянии и остановка кровотечения при повреждении сосуда реализуется посредством взаимодействия свертывающей, противосвертывающей и фибринолитической систем, имеющих множество составляющих.
В норме наблюдается равновесие, обеспечивающее жидкое состояние крови при неповрежденной сосудистой стенке, образование тромба при ее повреждении и последующее его растворение (фибринолиз).
В организме существует большое количество факторов свертывания, последовательно активирующихся при необходимости.
Таким образом, основной причиной тромбофилии становится дисбаланс свертывающих и противосвертывающих факторов крови, когда образование тромбов в сосудах происходит независимо от повреждения сосудистой стенки, а организм не может самостоятельно растворить их.
Классификация тромбофилии
В зависимости от этиологии (причины) тромбофилии подразделяются на две большие группы: врожденные (первичные) и приобретенные (вторичные).
К врожденным относят различные генетические дефекты, которые обуславливают предрасположенность организма к тромбозам. В этом случае риск патологического образования тромбов увеличивается при появлении дополнительных факторов тромбообразования (например, во время беременности и родов, у пациентов с выраженным ожирением, а также после травм, ожогов, длительной иммобилизации – неподвижности и др. ).
).
Существуют подтвержденные данные о связи врожденной тромбофилии с дефицитом антитромбина III, протеина С и S, АПС-резистентностью, гомоцистинурией.
Приобретенная тромбофилия может быть связана с различными инфекционными, онкологическими заболеваниями.
Самой частой приобретенной тромбофилией иммунного генеза является антифосфолипидный синдром, возникающий при различных аутоиммунных и инфекционных заболеваниях и связанный с выработкой в организме определенных белков, т. н. антифосфолипидных антител.
Синдром проявляется тромбозами вен и/или артерий, снижением числа тромбоцитов (тромбоцитопенией) и акушерско-гинекологической патологией – чаще всего привычным невынашиванием беременности.
Тромбофилия может быть одним из проявлений так называемого нефротического синдрома. При этом заболевании, наряду со снижением уровня альбумина в крови, выраженными отеками и повышением холестерина, имеется склонность к избыточному тромбообразованию.
Ряд заболеваний крови – истинная полицитемия, пароксизмальная ночная гемоглобинурия также могут проявляться образованием тромбов.
Ситуационная тромбофилия регистрируется при травмах, хирургических вмешательствах, особенно ортопедических, химиотерапии, приеме оральных контрацептивов, гормонально-заместительной терапии.
В зависимости от локализации различают тромбозы артериальные (в артериях), микроциркуляторные (в капиллярном русле), венозные (в венах), смешанные (с поражением различных типов сосудов).
Симптомы тромбофилии
Клинические проявления тромбофилии различаются в зависимости от локализации тромбов.
Для венозных тромбозов, когда закупоривается сосуд, возвращающий кровь к сердцу, характерно нарушение оттока крови от органа, отеки, повышение кожной температуры в области тромбоза, чувство распирания, умеренной интенсивности давящая боль. Часто поражаются поверхностные или глубокие вены нижних конечностей. Поражение может быть односторонним.
При артериальных тромбозах, когда нарушается доставка крови к органу, может возникать резкая болезненность, чувство распирания, постоянные давящие боли, цианоз (синюшность), снижение температуры в области тромбообразования и прилежащих тканях. Так, при поражении артерий нижних конечностей возникает перемежающаяся хромота – боль в икроножных мышцах (реже в бедре, стопе), возникающая во время ходьбы, усиливающаяся при подъеме по лестнице и проходящая через несколько минут после остановки.
Клинические проявления тромбоза артерий головного мозга во многом зависят от локализации и диаметра пораженного сосуда, обратимости изменений, то есть от времени начала активной терапии. При инсульте наблюдается интенсивная головная боль, головокружение, нарушение сознания, речи, чувствительные и двигательные расстройства – онемение, слабость в руке или ноге с одной стороны.
Если предприняты незамедлительные меры по растворению тромба (тромболизис), человек может полностью восстановиться.
Классической картиной при инфаркте миокарда являются интенсивные давящие боли за грудиной, иногда с иррадиацией в левую лопатку, левую руку; возможны резкая слабость, тошнота, рвота, страх смерти. При проведении тромболизиса возможен регресс симптоматики. Если же своевременное лечение не было проведено – участок сердечной мышцы замещается соединительной тканью (образуется рубец), он выключается из эффективного сокращения, из-за чего человек может хуже переносить физические нагрузки, могут появляться одышка, отеки нижних конечностей, как проявление сердечной недостаточности.
Диагностика тромбофилии
Диагноз подтверждается лабораторными и инструментальными методами. Основа диагностики – различные анализы крови.
Исследуют клинический анализ крови, отдельные параметры биохимического анализа крови – общий белок, альбумин, общий холестерин, креатинин и др.
Клинические наблюдения инфаркта миокарда у беременных: роль наследственной тромбофилии | Мравян
1. Tripathi B, Kumar V, Pitiliya A, Arora S, Sharma P, Shah M, Atti V, Ram P, Patel B, Patel NJ, Tripathi A, Savani S, Wojtaszek E, Patel T, Deshmukh A, Figueredo V, Gopalan R. Trends in Incidence and Outcomes of Pregnancy-Related Acute Myocardial Infarction (From a Nationwide Inpatient Sample Database). Am J Cardiol. 2019;123(8):1220-7. doi: 10.1016/j.amjcard.2019.01.030.
2. Elkayam U, Jalnapurkar S, Barakkat MN, Khatri N, Kealey AJ, Mehra A, Roth A. Pregnancy-associated acute myocardial infarction: a review of contemporary experience in 150 cases between 2006 and 2011. Circulation. 2014;129(16):1695-702. doi: 10.1161/CIRCU-LATIONAHA.113.002054.
3. Dtuski D, Mierzynski R, Poniedzialek-Czajkowska E, Leszczynska-Gorzelak B. Adverse pregnancy outcomes and inherited thrombophilia. J Perinat Med. 2018;46(4):411-7. doi: 10.1515/jpm-2017-0059.
4. Баринов СВ, Полтанова АА, Плехо РМ, Стариков НВ, Кролевец ЭН, Медянникова ИВ, Тирская ЮИ, Шамина ИВ, Ковалева ЮА, Шлапаков ОВ. Клиническое наблюдение родоразрешения при многоплодной беременности пациентки с крупноочаговым инфарктом миокарда в анамнезе и стентированием коронарной артерии. Российский вестник акушера-гинеколога. 2019;19(1):76-9. doi: 10.17116/rosakush30191901176.
5. Roth A, Elkayam U. Acute myocardial infarction associated with pregnancy. J Am Coll Cardiol. 2008;52(3):171-80. doi: 10.1016/j.jacc.2008.03.049.
6. Ito H, Taylor L, Bowman M, Fry ET, Hermiller JB, Van Tassel JW. Presentation and therapy of spontaneous coronary artery dissection and comparisons of postpartum versus nonpost-partum cases. Am J Cardiol. 2011;107(11): 1590-6. doi: 10.1016/j.amjcard.2011.01.043.
7. Al-Sadawi M, Shaikh S, Marmur JD, Salcicci-oli L, Kariyanna PT, McFarlane IM. Post-par-tum spontaneous coronary artery dissection: a case report. Am J Med Case Rep. 2018;6(10): 218-21. doi: 10.12691/ajmcr-6-10-6.
8. Elkayam U, Jalnapurkar S, Barakkat MN, Kha-tri N, Kealey AJ, Mehra A, Roth A. Pregnancy-associated acute myocardial infarction: a review of contemporary experience in 150 cases between 2006 and 2011. Circulation. 2014;129(16):1695-702. doi: 10.1161/CIRCU-LATIONAHA.113.002054.
9. Lindor RA, Tweet MS, Goyal KA, Lohse CM, Gulati R, Hayes SN, Sadosty AT. Emergency Department Presentation of Patients with Spontaneous Coronary Artery Dissection. J Emerg Med. 2017;52(3):286-91. doi: 10.1016/j.jemermed.2016.09.005.
10. Hossain N, Shamsi T, Soomro N. Frequency of thrombophilia in patients with adverse pregnancy outcome. J Pak Med Assoc. 2005;55(6): 245-7.
11. Галайко МВ, Рыбина ОВ, Литвиненко МС, Климов ЮВ, Альтшулер БЮ, Губкин АВ. Тромбофилия и беременность. Клиническая онкогематология. 2017;10(3): 409-22. doi: 10.21320/2500-2139-2017-103-409-422.
12. Trasca LF, Patrascu N, Bruja R, Munteanu O, Cirstoiu M, Vinereanu D. Therapeutic Implications of Inherited Thrombophilia in Pregnancy. Am J Ther. 2019;26(3):e364-74. doi: 10.1097/MJT.0000000000000985.
13. Bohiltea RE, Turcan N, Muresian H, Condu S, Bratila E, Cirstoiu MM. Postpartum Aortic Bifurcation Thrombosis on the Background of Thrombophilic Disorder. Maedica (Bucur). 2016;11(3):241-4.
14. Фазлиахметова АГ, Богданов ЭИ. Тромбофилия и инсульт. Практическая медицина. 2016;4-2(96):133-6.
15. Кокорин ВА, Кочмарева ЕА, Варданян АГ, Кондрашова ЕА, Хохлова НВ, Дорошенко ДА, Каширин ВВ, Конышева ОВ. Некомпактный миокард левого желудочка у беременной пациентки с наследственной тромбофилией: разбор клинического случая. Медицинский вестник Северного Кавказа. 2017;12(2): 222-5. doi: 10.14300/mnnc.2017.12064.
16. Couto E, Nomura ML, Barini R, Pinto e Silva JL. Pregnancy-associated venous thromboembolism in combined heterozygous factor V Leiden and prothrombin G20210A mutations. Sao Paulo Med J. 2005;123(6):286-8. doi: 10.1590/s1516-31802005000600007.
17. Gerhardt A, Scharf RE, Beckmann MW, Struve S, Bender HG, Pillny M, Sandmann W, Zotz RB. Prothrombin and factor V mutations in women with a history of thrombosis during pregnancy and the puerperium. N Engl J Med. 2000;342(6):374-80. doi: 10.1056/NEJM200002103420602.
18. Kim RJ, Becker RC. Association between factor V Leiden, prothrombin G20210A, and methylenetetrahydrofolate reductase C677T mutations and events of the arterial circulatory system: a meta-analysis of published studies. Am Heart J. 2003;146(6):948-57. doi: 10.1016/S0002-8703(03)00519-2.
19. Chen H, Nie S, Lu M. Association between plasminogen activator inhibitor-1 gene polymorphisms and recurrent pregnancy loss: a systematic review and meta-analysis. Am J Reprod Immunol. 2015;73(4):292-300. doi: 10.1111/aji.12321.
20. Jung RG, Motazedian P, Ramirez FD, Simard T, Di Santo P, Visintini S, Faraz MA, Labinaz A, Jung Y, Hibbert B. Association between plasminogen activator inhibitor-1 and cardiovascular events: a systematic review and me-ta-analysis. Thromb J. 2018;16:12. doi: 10.1186/s12959-018-0166-4.
21. Song C, Burgess S, Eicher JD, O’Donnell CJ, Johnson AD. Causal Effect of Plasminogen Activator Inhibitor Type 1 on Coronary Heart Disease. J Am Heart Assoc. 2017;6(6):e004918. doi: 10.1161/JAHA.116.004918.
22. James AH, Jamison MG, Biswas MS, Brancazio LR, Swamy GK, Myers ER. Acute myocardial infarction in pregnancy: a United States population-based study. Circulation. 2006;113(12): 1564-71. doi: 10.1161/CIRCULATIONA-HA.105.576751.
23. Kealey A. Coronary artery disease and myocardial infarction in pregnancy: a review of epidemiology, diagnosis, and medical and surgical management. Can J Cardiol. 2010;26(6):185-9. doi: 10.1016/s0828-282x(10)70397-4.
24. Мравян СР, Петрухин ВА, Давыдова ТВ, Будыкина ТС, Тишенина РС, Пронина ВП, Гришин ВЛ. Особенности ведения беременности после множественного стентирования коронарных артерий. Клиническая медицина. 2012;90(9):69-74.
25. Макацария АД., Бицадзе ВО. Антифосфолипидный синдром, генетические тромбофилии в патогенезе основных форм акушерской патологии. Русский медицинский журнал. 2006;S0:2-10.
Морфология плаценты при наследственной тромбофилии
Тромбофилия — это патологическое состояние, характеризующееся повышением свертывания крови и склонностью к тромбозам и тромбоэмболиям. Классически выделяют два типа тромбофилии — наследственную и приобретенную [1]. Частота наследственной тромбофилии составляет 10-12%, а у женщин с привычным невынашиванием беременности достигает 48% [2]. Наследственные, генетически детерминированные тромбофилии наиболее часто обусловлены мутациями гена G1691A фактора V (Лейдена) (гетерозиготными носителями являются 3-5% европейского населения), протромбина
(G 20210DA) (гетерозиготными носителями являются 1-3% европейского населения гена метилентетрагидрофолатредуктазы (MTHFR) (C677T) в сочетании с гипергомоцистеинемией и другими тромбогенными генетическими полиморфизмами [1]).
При тромбофилии во всех жизненно важных органах беременной, включая систему мать-плацента-плод может развиться тромбоз. Нарушение маточно-плацентарного, плодово-плацентарного кровотока вследствие развития тромбоза сосудов, приводящего к хронической плацентарной недостаточности (ХПН), может быть причиной самопроизвольного прерывания беременности (35%), рождения детей с низкой массой тела (33-60%), задержки роста плода (до 33%), внутриутробной гибели плода, преждевременной отслойки плаценты, а также типичных акушерских осложнений — коагулопатических кровотечений и тяжелого гестоза (6-44%) [3-8]. Среди причин невынашивания беременности до 55-62% составляют дефекты коагуляционных протеинов или тромбоцитов [9]. При наследственной тромбофилии отмечены тератогенные эффекты. Наследственная тромбофилия способствует развитию у женщин аутоиммунных нарушений, в том числе антифосфолипидного синдрома, являющегося проявлением приобретенной тромбофилии [1].
При приобретенной тромбофилии в плаценте на ранних сроках беременности формируются морфологические изменения, характеризующиеся повреждением эндотелия сосудов и синцитиотрофобласта, разобщением цито- и синцитиотрофобласта, микродефектами синцитиотрофобласта ворсин с закрывающими их фибриновыми слепками, задержка децидуализации стромы эндометрия, неполная гестационная перестройка спиральных артерий вследствие недостаточности первой волны интравазальной трофобластической инвазии [2]. В более поздние сроки беременности формируется ХПН с задержкой созревания и преждевременным старением плаценты, тромбы разной давности в сосудах и интервиллезном пространстве, инфаркты, псевдоинфаркты, гематомы разной давности, избыточное отложение в интервиллезном пространстве и в базальной пластинке фибриноида [10]. Однако исследования, посвященные морфологическим изменениям в плаценте при наследственной тромбофилии, немногочисленны.
Цель исследования — изучить морфологические изменения в плаценте при наследственной тромбофилии.
Материал и методы
Для исследования были взяты образцы плаценты от 37 женщин, разделенных на 3 группы. В 1-ю группу вошли 13 (35,3%) беременных с верифицированной наследственной тромбофилией в возрасте 29,67±1,11 года, родивших при сроке гестации 40,0±0,11 нед, масса новорожденных 3284,54±80,63 г. Учитывая, что ранее было показано частое сочетание наследственной тромбофилии и инфекционного поражения плаценты [9], способствующего прогрессирующему течению тромбофилии, во 2-ю группу мы включили 14 (37,84%) беременных с наследственной тромбофилией и признаками воспалительных проявлений в плаценте (базальный децидуит, интервиллезит, плацентит) в возрасте 27,67±0,89 года, роды произошли при сроке гестации 38,9±0,87 нед, масса новорожденных 3385,0±183,39 г. В 3-ю (контрольную) группу были включены 10 беременных с нормально развивавшейся беременностью в возрасте 28,2±1,77 года, самопроизвольные роды при сроке гестации 40 нед, масса новорожденных 3302,0±56,42 г.
У женщин 1-й и 2-й групп наследственная тромбофилия была диагностирована во время беременности и представлена следующими вариантами: гомозиготная мутация гена фактора VII, гетеро- и гомозиготная мутация MTHFR, гомозиготная мутация V фактора (Лейдена), гетерозиготная мутация генов фолатного цикла: метионин-синтетазы (MTRR), цистататион-β-синтетазы (CBS), а также мутация ингибитора активатора плазминогена (PAI-I), факторов XII, VIII. Количество выявленных дефектов гемостаза у беременных женщин было представлено одним дефектом в 64,5%, двумя дефектами и более — в 35,4% случаев.
В анамнезе у 50% женщин при повторной беременности были самопроизвольные выкидыши на малом сроке и неразвивающаяся беременность; в 50% наблюдений при первой беременности отмечали бесплодие в течение 2-3 лет, наличие урогенитальной инфекции.
Образцы плаценты из центральной части плацентарного диска фиксировали в 10% нейтральном формалине, обезвоживали в спиртах восходящей концентрации, заливали в парафин, готовили срезы толщиной 5 мкм и окрашивали их гематоксилином и эозином, по ван Гизону, проводили ШИК-реакцию [11]. В плаценте с помощью окулярной сетки подсчитывали численную плотность (Nai) сосудов терминальных ворсин, объемную плотность (Vv) структур плаценты, типов ворсин, межворсинчатого пространства, стромы и трофобластического эпителия терминальных ворсин. Различий средних величин при нормальном распределении оценивали с помощью t-критерия Стьюдента и считали их достоверными при p<0,05 [12].
Результаты и обсуждение
В плаценте у женщин 1-й и 2-й групп в интервиллезном пространстве отмечали очаги отложения фибриноида (см. рисунок, а)Рисунок 1. Плацента при наследственной тромбофилии. ШИК-реакция. а — в интервиллезном пространстве избыточное отложение фибриноида, ×100. с замуровыванием групп ворсин и образованием псевдоинфарктов (см. рисунок, б).Рисунок 1. Плацента при наследственной тромбофилии. ШИК-реакция. б — образование псевдоинфаркта, ×400. Во всех плацентах были обнаружены очаги кальцификации в псевдоинфарктах, синцитиальных почках, строме ворсин, клеточных островках, септах; были выявлены интервиллезные тромбы разной степени давности, а также кровоизлияния в децидуальной базальной пластине.
Структурная организация плаценты у женщин 1-й и 2-й групп (наследственная тромбофилия) характеризовалась увеличением объемной плотности межворсинчатого фибриноида и очагов обызвествления (в 5 и 10 раз соответственно) по сравнению с аналогичным показателем в плаценте у женщин 3-й группы (табл. 1).
Объемная плотность базальной пластины в плаценте у женщин 1-й и 2-й групп была меньше по сравнению с аналогичным показателем у женщин 3-й группы в 1,4 и 1,2 раза соответственно (см. табл. 1), что может способствовать развитию преждевременной отслойки плаценты.
При наследственной тромбофилии (1-я и 2-я группы) в плаценте во всех наблюдениях была выявлена незрелость ворсин (варианты промежуточных дифференцированных ворсин и диссоциированного созревания котиледонов). При исследовании типов ворсин объемная плотность (Vv) терминальных ворсин, преобладающих в плаценте у женщин 3-й группы, при наследственной тромбофилии (1-я группа) и при сочетании наследственной тромбофилии с воспалением (2-я группа) была существенно меньше (в 3 и 2 раза соответственно), со значительным увеличением доли ворсин, замурованных в фибриноид и выключенных из обменных процессов в плаценте (табл. 2).
В терминальных ворсинах, обеспечивающих основной обмен между организмом матери и плода, количество капилляров у женщин 1-й и 2-й групп было меньше по сравнению с величиной аналогичного показателя в плаценте у женщин 3-й группы в 3 раза (табл. 3). Вследствие уменьшенного количества сосудов и нарастающей гипоксии возрастала доля стромы ворсин за счет увеличения в них процессов склерозирования. Число свободных симпластов было увеличено в 1,5-2 раза по сравнению с 3-й группой, по-видимому, как компенсаторная реакция [14, 15].
Известно, что тромбогенное действие при наследственной тромбофилии обусловлено повреждением эндотелиоцитов при повышении содержания гомоцистеина, активацией факторов V и VII, усилением агрегации тромбоцитов вследствие снижения синтеза эндотелием релаксирующего фактора и оксида азота и др. [13]. Учитывая, что гомоцистеин может проходить через плаценту, вероятно, он оказывает деструктивное действие на трофобластический эпителий с последующим запуском процессов свертывания крови, избыточного образования фибриноида в межворсинчатом пространстве, что ведет к формированию ХПН. В случаях Лейденской мутации фактора V с развитием резистентности к активированному протеину С и созданием условий для гиперактивации протромбокиназного комплекса и мутации гена протромбина с повышением уровня протромбина и запуском коагуляционного каскада основным морфологическим проявлением в плаценте является тромбоз, формирование ХПН, в том числе с задержкой внутриутробного развития плода, отслойки нормально расположенной плаценты. При дефекте ингибитора активатора плазминогена (PAI-1) увеличивается резистентность к фибринолизу и стабилизация фибринового сгустка, что приводит к увеличению доли межворсинчатого фибриноида. Кроме того, продукция PAI-1 увеличивается под действием С-реактивного белка в условиях системного воспалительного ответа, в том числе при инфекционном поражении плаценты.
Вероятно, гипергомоцистеинемия ведет к задержке созревания ворсин, их незрелости и склерозу с редукцией капиллярного русла и ишемией плаценты [17]. Развитию ишемизации плаценты может также способствовать нарушение гестационной перестройки спиральных артерий вследствие задержки I и II волны интравазальной трофобластической инвазии, наблюдаемой при тромбофилии, а также способность гомоцистеина стимулировать пролиферацию гладкомышечных клеток. В основе развития задержки созревания ворсин при наследственной тромбофилии возможна роль уменьшения пролиферативной активности трофобластического эпителия, усиление экспрессии противоапоптотического белка bcl-2. Показано, что выраженность этих процессов увеличивается при возрастании количества мутаций у беременной [17].
При наследственной тромбофилии в плаценте были выявлены морфологические проявления хронической плацентарной недостаточности в виде патологической незрелости с преобладанием промежуточных дифференцированных ворсин и диссоциированного созревания котиледонов, с существенной редукцией числа терминальных специализированных ворсин, избыточным образованием межворсинчатого фибриноида с замуровыванием ворсин, их кальцификацией, уменьшением количества капилляров в терминальных ворсинах, увеличением в них доли стромы. При этом в условиях сочетания наследственной тромбофилии с воспалительными изменениями в плаценте существенных особенностей морфологической картины не выявлено.
Возможность клинико-морфологической диагностики наследственной тромбофилии позволяет определить причину и прогноз беременности, а при своевременной коррекции гемореологических нарушений у беременных с тромбофилией они имеют шанс выносить беременность. Знание морфологических основ плацентарной недостаточности при наследственной тромбофилии необходимо для совершенствования методов своевременной коррекции гемореологических нарушений [1, 4-6, 18].
Участие авторов:
Концепция и дизайн исследования: А.П.Н.
Сбор и обработка материала: А.Н.Д., М.А.К., Н.В.Т.
Написание текста: В.А.Ж.
Подготовка микрофотографий: Н.В.Т.
Редактирование: А.П.Н., Н.М.П.
Конфликт интересов отсутствует.
Тромбофилия – причины, симптомы, классификации, диагностика и лечение — Клиника «Доктор рядом»
Что такое тромбофилия?
Изучением и лечением тромбофилии занимаются несколько областей медицины: гематология, флебология и сосудистая хирургия. Нарушения гемостаза, т. е. кровяного тока и предрасположенность к формированию тромбов — отличительные особенности приобретённой и наследственной тромбофилии. Как уже упоминалось, она проявляется частыми повторяющимися тромбозами различной локализации. Они могут возникать при появлении различных дополнительных факторов в виде оперативного вмешательства, травм, беременности у женщин.
Вид тромбофилии
Врождённая
Приобретённая
Почему возникает?
Аномалии строения генов, провоцирующие сбои в функционировании системы свёртываемости крови, передающиеся по наследству.
Ряд других заболеваний, включая злокачественные новообразования, приём определённых фармакологических препаратов.
Виды
-
дефицит протеина «S»; -
дефицит протеина C; -
полиморфизм V фактора свёртываемости крови; -
полиморфизм в гене протромбина ІІ фактора свёртываемости крови; -
дефицит антитромбина.
-
антифосфолипидный синдром; -
приобрётенный дефицит антитромбина III; -
пиелопролиферативные патологии, для которых характерно производство мозгом избыточного количества кровяных клеток.
Перечисление этиологических факторов
-
высокий уровень липопротеидов; -
дефицит антитромбина III; -
талассемия; -
дефицит протромбинов «S» и «C»; -
мутации генов фактора «V» и протромбинов.
-
катетеризация вен в течение длительного времени; -
химиотерапия злокачественных новообразований; -
инсульты, инфаркты; -
протезирование сердечных клапанов; -
обезвоживание организма, сопровождающееся увеличением числа эритроцитов; -
аутоиммунные заболевания.
Классификация
Современная медицина выделяет две основные группы тромбофилий:
|
|
|
|
|
|
Клинические проявления и диагностика тромбофилии
Заболевание проявляет себя часто повторяющимися рецидивами тромбоза, клиническая картина, которого определяется:
-
Локализацией тромба; -
Степенью нарушения тока крови; -
Наличием заболевания, на фоне которого всё это приоисходит.
Помимо этого, о наличии этого заболевания могут сигнализировать такие признаки, как инфаркты органов у молодых пациентов, а также ТЭЛА, повторные выкидыши на ранних сроках беременности.
На основании клинических проявлений заболевания сбора анамнеза, врач выясняет имеется ли генетическая предрасположенность, а также лабораторных анализов, ставят диагноз «Тромбофилия». Анализы проводят в два этапа, первый из которых посвящён определению вида тромбофилии, второй, генетический позволяет типировать вид тромбофилии и определить ее риск у потомства.
Лечение тромбофилии
Тактику лечения тромбофилии подбираются индивидуально, однако цели, которые она преследует, всегда направлены на решение следующих задач:
Важно понимать, что специфической терапии для лечения данного патологического состояния не существует. Консервативные методики, которые применяются в процессе, предусматривают комплексный подход и включают в себя следующее:
-
Диета, исключающая потребление жирных и жареных блюд, а также продуктов с высоким содержанием холестерина; -
Приём фармакологических средств: дезагрегантов («Аспирин», «Курантил», плаквенил), а в некоторых случаях и антикоагулянтов («Варфарин», прадакса, ксарелто), вазодилататаров («Трентал»).
Тромбофилия, развитие которой было спровоцировано недостаточностью факторов свёртывания, требует переливания плазмы, которое комбинируют с введением гепарина.
При генетической тромбофилии помимо гепарина в кровь вводят средства с антитромбином III.
В сети клиник «Доктор рядом» работает профессиональная команда флебологов, гематологов и сосудистых хирургов, которые помогут справиться с заболеванием. Звоните: +7 495 230-03-09.
Влияние наследственной и приобретенной тромбофилии на исходы программ вспомогательных репродуктивных технологий
ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, Москва, Россия
На основании анализа данных литературы дана оценка влиянию наследственной и приобретенной тромбофилии на эффективность программ вспомогательных репродуктивных технологий (ВРТ) и эффективность использования низкомолекулярных гепаринов (НМГ) в улучшении исходов программ ВРТ. В обзор включены данные зарубежных и отечественных статей, найденных в базах данных PubMed, Elsevier, Cochrane Library по данной теме, опубликованные за последние 10 лет. Роль наследственной и приобретенной тромбофилии в эффективности программ ВРТ, а также применение НМГ с целью улучшения исходов программ ВРТ является дискутабельным вопросом и требует проведения дальнейших исследований.
вспомогательные репродуктивные технологии
наследственные тромбофилии
антифосфолипидный синдром
антифосфолипидные антитела
низкомолекулярные гепарины
- Корсак В.С., Смирнова А.А., Шурыгина О.В. Регистр центров ВРТ в России. Отчет за 2015 г. Проблемы репродукции. 2017; 23(5): 8-22.
- Bashiri A., Harlev A., Agarwal A., eds. Recurrent pregnancy loss : evidence-based evaluation, diagnosis and treatment. Springer; 2016. 208 p.
- Cinnioglu C., Kayali R., Darvin T., Akinwole A., Jakubowska M., Harton G. Aneuploidy screening using next generation sequencing. Methods Mol. Biol. 2019; 1885: 85-102. https://doi.org/10.1007/978-1-4939-8889-1_6.
- Alteri A., Corti L., Sanchez A.M., Rabellotti E., Papaleo E., Viganò P. Assessment of pre-implantation genetic testing for embryo aneuploidies: A SWOT analysis. Clin. Genet. 2019; 95(4): 479-87. https://doi.org/10.1111/cge.13510.
- Kovalevsky G., Gracia C.R., Berlin J.A., Sammel M.D., Barnhart K.T. Evaluation of the association between hereditary thrombophilias and recurrent pregnancy loss: a meta-analysis. Arch. Intern. Med. 2004; 164(5): 558-63. https://doi.org/10.1001/archinte.164.5.558.
- Kupferminc M.J., Eldor A., Steinman N., Many A., Bar-Am A., Jaffa A. et al. Increased frequency of genetic thrombophilia in women with complications of pregnancy. N. Engl. J. Med. 1999; 340(1): 9-13. https://doi.org/10.1056/NEJM199901073400102.
- Rodger M.A., Betancourt M.T., Clark P., Lindqvist P.G., Dizon-Townson D., Said J. et al. The association of factor V leiden and prothrombin gene mutation and placenta-mediated pregnancy complications: a systematic review and meta-analysis of prospective cohort studies. PLoS Med. 2010; 7(6): e1000292. https://doi.org/10.1371/journal.pmed.1000292.
- Rey E., Kahn S.R., David M., Shrier I. Thrombophilic disorders and fetal loss: a meta-analysis. Lancet. 2003; 361(9361): 901-8. https://doi.org/10.1016/S0140-6736(03)12771-7.
- Azem F., Many A., Ben Ami I., Yovel I., Amit A., Lessing J.B., Kupferminc M.J. Increased rates of thrombophilia in women with repeated IVF failures. Hum. Reprod. 2004; 19(2): 368-70.
- Qublan H.S., Eid S.S., Ababneh H.A., Amarin Z.O., Smadi A.Z., Al-Khafaji F.F., Khader Y.S. Acquired and inherited thrombophilia: implication in recurrent IVF and embryo transfer failure. Hum. Reprod. 2006; 21(10): 2694-8. https://doi.org/10.1093/humrep/del203.
- Grandone E., Colaizzo D., Lo Bue A., Checola M.G., Cittadini E., Margaglione M. Inherited thrombophilia and in vitro fertilization implantation failure. Fertil. Steril. 2001; 76(1): 201-2.
- Martinelli I., Taioli E., Ragni G., Levi-Setti P., Passamonti S.M., Battaglioli T. et al. Embryo implantation after assisted reproductive procedures and maternal thrombophilia. Haematologica. 2003; 88(7): 789-93.
- Qublan H., Amarin Z., Dabbas M., Farraj A.-E., Beni-Merei Z., Al-Akash H. et al. Low-molecular-weight heparin in the treatment of recurrent IVF-ET failure and thrombophilia: a prospective randomized placebo-controlled trial. Hum. Fertil. (Camb.). 2008; 11(4): 246-53. https://doi.org/10.1080/14647270801995431.
- Urman B., Ata B., Yakin K., Alatas C., Aksoy S., Mercan R., Balaban B. Luteal phase empirical low molecular weight heparin administration in patients with failed ICSI embryo transfer cycles: a randomized open-labeled pilot trial. Hum. Reprod. 2009; 24(7): 1640-7. https://doi.org/10.1093/humrep/dep086.
- Клинические рекомендации МЗ РФ «Профилактика венозных тромбоэмболических состояний в акушерстве и гинекологии». М.; 2014.
- Rambaldi M.P., Mecacci F., Guaschino S., Paidas M.J. Inherited and acquired thrombophilias. Reprod. Sci. 2014; 21(2): 167-82. https://doi.org/10.1177/1933719113497282.
- Кузнецова И.В., Суханова Г.А. Возможности снижения перинатального и акушерского риска у женщин с тромбофилиями. Эффективная фармакотерапия. 2017; 25: 14-21.
- Акиньшина С.В., Макацария А.Д., Бицадзе В.О. Патогенез и профилактика тромбоэмболических осложнений, связанных с использованием вспомогательных репродуктивных технологий. Медицинский совет. 2014; 9: 84-9.
- Бицадзе В.О., Акиньшина С.В., Андреева М.Д,. Макацария А.Д. Тромбоэмболические осложнения, связанные с использованием вспомогательных репродуктивных технологий. Синдром гиперстимуляции яичников. Практическая медицина. 2013; 7: 20-31.
- Steinvil A., Raz R., Berliner S., Steinberg D.M., Zeltser D., Levran D. et al. Association of common thrombophilias and antiphospholipid antibodies with success rate of in vitro fertilisation. Thromb. Haemost. 2012; 108(6): 1192-7. https://doi.org/10.1160/Th22-06-0381.
- Tan X., Yu Z., Sao J., Chen L., Shen Y., Ding J., Shi W. Association between in vitro fertilization outcomes and inherited thrombophilias: a meta-analysis. J. Assist. Reprod. Genet. 2016; 33(8): 1093-8. https://doi.org/10.1007/s10815-016-0726-0.
- Di Nisio M., Rutjes A.W.S., Ferrante N., Tiboni G.M., Cuccurullo F., Porreca E. Thrombophilia and outcomes of assisted reproduction technologies: a systematic review and meta-analysis. Blood. 2011; 118(10): 2670-8. https://doi.org/10.1182/blood-2011-03-340216.
- Клинические рекомендации МЗ РФ «Вспомогательные репродуктивные технологии и искусственная инсеминация». М.; 2019.
- ACOG Practice Bulletin No. 197. Inherited thrombophilias in pregnancy. June 2018.
- Royal College of Obstetricians and Gynaecologists (RCOG). Reducing the risk of venous thromboembolism during pregnancy and the puerperium. Green-top guideline No. 37a. April 2015.
- Chighizola C.B., de Jesus G.R. Antiphospholipid antibodies and infertility. Lupus. 2014; 23(12): 1232-8. https://doi.org/10.1177/0961203314529171.
- American College of Obstetricians and Gynecologists (ACOG). Antiphospholipid syndrome. Practice bulletin No.132.December 2012.
- Jeve Y.B., Davies W. Evidence-based management of recurrent miscarriages. J. Hum. Reprod. Sci. 2014; 7(3): 159-69. https://doi.org/10.4103/0974-1208.142475.
- Rand J.H., Wolgast L.R. Dos and don’ts in diagnosing antiphospholipid syndrome. Hematol. Am. Soc. Hematol. Educ. Progr. 2012; 2012: 455-9. https://doi.org/10.1182/asheducation-2012.1.455.
- Макацария А.Д., ред. Антифосфолипидный синдром – иммунная тромбофилия в акушерстве и гинекологии (монография). М.: Триада-Х; 2007. 451 c.
- Di Rosa R., Ferrero S., Cifani N., Ferri L., Proietta M., Picchianti Diamanti A., Del Porto F. In vitro fertilization and autoimmunity: Evidence from an observational study. Eur. J. Obstet. Gynecol. Reprod. Biol. 2019; 234: 137-42. https://doi.org/10.1016/j.ejogrb.2018.12.042.
- Khizroeva J., Makatsariya A., Bitsadze V., Makatsariya N., Khamani N. In vitro fertilization outcomes in women with antiphospholipid antibodies circulation. J. Matern. Fetal Neonatal Med. 2018; Oct 12: 1-11. https://doi.org/10.1080/14767058.2018.1535586.
- Royal College of Obstetricians and Gynaecologists (RCOG). The investigation and treatment of couples with recurrent first-trimester and second-trimester miscarriage. Green-top Guideline No.17. 2011. UpdateFebruary 2017.
- Клинические рекомендации МЗ РФ: «Синдром гиперстимуляции яичников: диагностика, лечение, профилактика, интенсивная терапия». М.; 2019.
- Spratte J., Bornkessel F., Schütz F., Zygmunt M., Fluhr H. The presence of heparins during decidualization modulates the response of human endometrial stromal cells to IL-1β in vitro. J. Assist. Reprod. Genet. 2016; 33(7): 949-57. https://doi.org/10.1007/s10815-016-0703-7.
- Seshadri S., Sunkara S.K., Khalaf Y., El-Toukhy T., Hamoda H. Effect of heparin on the outcome of IVF treatment: a systematic review and meta-analysis. Reprod. Biomed. Online. 2012; 25(6): 572-84. https://doi.org/10.1016/j.rbmo.2012.08.007.
- Akhtar M.A., Sur S, Raine-Fenning N., Jayaprakasan K., Thornton J.G., Quenby S. Heparin for assisted reproduction. Cochrane database Syst. Rev. 2013; (8): CD009452. 0.1002/14651858.CD009452.pub2.
- Ata B., Urman B. Thrombophilia and assisted reproduction technology-any detrimental impact or unnecessary overuse? J. Assist. Reprod. Genet. 2016; 33(10): 1305-10. https://doi.org/10.1007/s10815-016-0771-8.
- Siristatidis C.S., Basios G., Pergialiotis V., Vogiatzi P. Aspirin for in vitro fertilisation. Cochrane database Syst. Rev. 2016; (11): CD004832. https://doi.org/10.1002/14651858.CD004832.pub4.
Поступила 22.02.2019
Принята в печать 19.04.2019
Краевая Елизавета Евгеньевна, м.н.с. отделения вспомогательных технологий в лечении бесплодия ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России.
Тел.: +7 (495) 438-25-01. E-mail: [email protected]. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4.
Долгушина Наталия Витальевна, д.м.н., профессор, заместитель директора – руководитель департамента организации научной деятельности ФГБУ «НМИЦ АГП
им. В.И. Кулакова» Минздрава России. Тел.: +7 (495) 438-49-77. E-mail: [email protected]. Адрес: 117997, Россия, Москва, ул. Академика Опарина, д. 4.
Для цитирования: Краевая Е.Е., Долгушина Н.В. Влияние наследственной и приобретенной тромбофилии на исходы программ вспомогательных репродуктивных технологий.
Акушерство и гинекология. 2019; 8:20-25.
https://dx.doi.org/10.18565/aig.2019.8.20-25
Генетический риск развития тромбофилии: исследования в лаборатории KDLmed
Комплексный генетический анализ, который позволяет определить риск развития тромбофилии. Он представляет собой молекулярно-генетическое исследование генов факторов свертываемости крови и ферментов обмена гомоцистеина, изменение активности которых напрямую или опосредованно обуславливают склонность к повышенному тромбообразованию.
Какой биоматериал можно использовать для исследования?
Буккальный (щечный) эпителий, венозную кровь.
Как правильно подготовиться к исследованию?
Подготовки не требуется.
Подробнее об исследовании
В результате различных патологических процессов, в сосудах могут образовываться тромбы, которые блокируют кровоток. Это самое частое и неблагоприятное проявление наследственной тромбофилии – состояния, обуславливающего повышенную склонность к тромбообразованию и связанного с определенными генетическими дефектами. Она может приводить к артериальным и венозным тромбозам, которые в свою очередь зачастую вызывают инфаркт миокарда, ишемическую болезнь сердца, инсульт, тромбоэмболию легочной артерии и др.
В системе гемостаза участвуют факторы свёртывающей и противосвертывающей систем крови. В нормальном состоянии они находятся в равновесии и обеспечивают физиологические свойства крови, не допуская повышенного тромбообразования или, наоборот, кровоточивости. Но при воздействии внешних или внутренних факторов это равновесие может нарушаться.
Значительный вклад в развитие генетически обусловленной формы тромбофилии вносит мутация Лейден в гене фактора свертываемости 5 (F5 G1691A). Результатом данной мутации является устойчивость активной формы фактора 5 к расщепляющему действию специализированного фермента С-белка, что приводит к повышению свёртываемости крови. Соответственно, и риск образования тромбов увеличивается. Другим важным фактором развития генетически обусловленной склонности к тромбозам считается мутация в гене коагуляционного фактора 2, или протромбина (F2 G20210A). При носительстве этой мутации отмечается увеличение синтеза протромбина и, как следствие, нарушение равновесия в системе гемостаза – усилению процессов свертывания крови.
При мутациях в генах F2 и F5 риск возникновения тромбозов значительно возрастает, особенно при наличии провоцирующих факторов, таких как приём оральных контрацептивов или заместительная гормональная терапия. Кроме того, у носительниц этих мутаций высока вероятность неблагоприятного течения беременности: невынашивания беременности, фетоплацентарной недостаточности, задержки внутриутробного развития плода и других осложнений.
Существенное значение в формировании предрасположенности к тромботическим состояниям имеет повышение содержания в крови аминокислоты гомоцистеина. Его концентрация может возрастать по многим причинам, в том числе при дефектах генов ферментов, контролирующих его обмен. При чрезмерном накоплении гомоцистеин оказывает токсическое действие на сосудистую стенку. В месте повреждения образуются тромбы, там же может осесть избыточный холестерин, что опасно закупориванием сосудов. Одной из причин повышения уровня гомоцистеина является снижение активности ферментов, обеспечивающих его обмен. Ген MTHFR (фермент фолатного цикла – метилентетрагидрофолат редуктаза) играет ключевую роль в обмене фолиевой кислоты. На данный момент известны два генетических маркера, приводящие к снижению активности фермента и, как следствие, к изменению уровня гомоцистеина: MTHFR (C677T) и MTHFR (A1298C).
Гипергомоцистеинемия повышает риск развития атеросклероза, ишемической болезни сердца, венозных тромбозов и ишемических инсультов. Кроме того, наличие изменений в данном гене позволяет определить предрасположенность к неблагоприятному течению беременности (фетоплацентарной недостаточности, незаращению нервной трубки и другим осложнениям для плода). При изменениях в фолатном цикле в качестве профилактики применяются фолиевая кислота и витамины В6, В12. Продолжительность терапии и дозировка препаратов может определяться на основании генотипа, уровня гомоцистеина и особенностей сопутствующих факторов риска у человека.
Комплексное молекулярно-генетическое исследование позволяет оценить индивидуальный генетический риск тромбофилии и при наличии предрасположенности предотвратить развитие тромбозов профилактическими мероприятиями.
Важно знать, что сочетание генетических дефектов, предрасполагающих к тромбообразованию, и наличие дополнительных факторов риска тромбозов значительно усугубляет риск развития тромбоэмболических осложнений.
Факторы риска развития тромбофилии:
- постельный режим (более 3 суток), длительная иммобилизация, длительные статические нагрузки, в том числе связанные с работой, малоподвижный образ жизни;
- применение пероральных контрацептивов, содержащих эстрогены;
- избыточная масса тела;
- венозные тромбоэмболические осложнение в анамнезе;
- катетер в центральной вене;
- обезвоживание;
- хирургические вмешательства;
- травма;
- курение;
- онкологические заболевания;
- беременность;
- сопутствующие сердечно-сосудистые заболевания; злокачественные новообразования.
Когда назначается исследование?
- При имеющихся сердечно-сосудистых заболеваниях (венозный тромбоз, тромбоэмболии, случаи ранних инфарктов и инсультов) в семейном анамнезе.
- В случае тромбоза в анамнезе, особенно в возрасте до 50 лет, повторных тромбозах.
- При тромбозе в любом возрасте в сочетании с наличием отягощенного семейного анамнеза по тромбоэмболии, в том числе тромбозах сосудов мозга, портальных вен и др.
- При тромбозе в отсутствие очевидных факторов риска в возрасте старше 50 лет.
- В случае применения гормональных контрацептивов или заместительной гормональной терапии у женщин, имеющих тромбозы в анамнезе, а также у родственников 1-й степени родства, у которых была диагностирована наследственная тромбофилия.
- При осложненном акушерском анамнезе (невынашивание беременности, фетоплацентарная недостаточность, тромбозы во время беременности и раннем послеродовом периоде и др.).
- При планировании беременности женщиной, у которой родственники 1-й степени родства страдали тромбозом.
- В условиях высокого риска (полостные оперативные вмешательства, длительная иммобилизация, постоянные статические нагрузки, малоподвижный образ жизни).
- При оценке риска тромботических осложнений у больных со злокачественными новообразованиями.
Что означают результаты?
По результатам комплексного исследования выдается заключение врача-генетика, которое позволит оценить риск тромбофилии, прогнозировать развитие тромбозов и других сосудистых осложнений, выбрать направления оптимальной профилактики, а при уже имеющихся нарушениях детально разобраться в их причинах.
Генетические маркеры
Также рекомендуется
Литература
- Letter M.H. et al., Lung artery thromboembolism prevention in obstetrics – thrombosis and thrombophilia genetic forms. 2002.
- Smith K. J. et al., Should female relatives of factor V Leiden carriers be screened prior to oral contraceptive use? A cost-effectiveness analysis, Thromb. Haemost. 2008 Sep;100(3):447-52. [PMID: 18766261]
- Venous thromboembolism, thrombophilia, antithrombotic therapy, and pregnancy. American College of Chest Physicians evidence-based clinical practice guidelines 8th edition. American College of Chest Physicians — Medical. Specialty Society. 2001 January.
Унаследованная тромбофилия: палка о двух концах | Гематология, Образовательная программа ASH
В 1995 году мои коллеги-младшие исследователи в отделении отметили большое количество выкидышей и мертворождений у женщин, которые участвовали в семейном исследовании, которое было организовано для оценки абсолютного риска ВТЭ в семьях с дефицитом антитромбина, протеина С или протеина S. . Действительно, они обнаружили, что риск у женщин с дефицитом повышается в 2 раза по сравнению с родственниками, не имеющими дефицита. .С тех пор в многочисленных исследованиях изучалась связь между наследственной тромбофилией и различными осложнениями беременности, от единичного выкидыша до внутриутробной гибели плода, преэклампсии, HELLP (гемолиз, повышенные ферменты печени и низкие тромбоциты) и отслойка плаценты. 27,40 Обследование женщин с осложнениями беременности вскоре стало обычной клинической практикой, но основанного на доказательствах ответа о последующих терапевтических последствиях не было. Этот частый клинический вопрос подогревал мой интерес не только к ассоциациям и абсолютным рискам, но и к проверке часто обсуждаемой гипотезы о том, что антикоагуляция низкомолекулярным гепарином (НМГ) может улучшить исход беременности у женщин с наследственной тромбофилией и без нее и с другими необъяснимыми рецидивами. выкидыш.Это был мой первый личный опыт успешного создания и ведения многоцентрового рандомизированного клинического исследования по инициативе исследователя, которое называлось ALIFE. 41 Несмотря на то, что набор и проведение исследования были сложными, а результат был отрицательным, я считаю его завершение, публикацию и влияние на клиническую практику важным моментом в моей карьере. После 15 лет различных клинических испытаний, проведенных коллегами по всему миру, мы теперь знаем, что НМГ не улучшает вероятность живорождения у женщин с невынашиваемым невынашиванием беременности без объяснения причин. 42-45 Однако мы все еще не уверены в том, что это также относится к женщинам с наследственной тромбофилией. 46,47 В исследовании ALIFE подгруппа женщин с наследственной тромбофилией (n = 47) показала тенденцию к преимуществу НМГ и аспирина (относительный риск живорождения 1,31 [95% ДИ 0,74–2,33] для НМГ и аспирин по сравнению с плацебо: относительный риск живорождения 1,22 [95% ДИ 0,69–2,16] для аспирина с соответствующей абсолютной разницей в коэффициентах живорождения 16.3% [95% ДИ, от –18,2% до 50,8%] и 11,8% [95% ДИ, от –21,1% до 44,6%], соответственно). 41 На основе этих результатов мы инициировали исследование ALIFE2, в которое с 2013 года набирают пациентов в Нидерландах, Великобритании и Бельгии и, надеюсь, вскоре в США и Словении. 48
Что касается других осложнений беременности, опосредованных плацентой, результаты метаанализа индивидуальных данных пациентов AFFIRM включали 963 женщины, которые участвовали в 8 рандомизированных контролируемых исследованиях, включая исследование TIPPS, которое было полностью посвящено женщинам с тромбофилией. 49-51 НМГ существенно не снижали риск повторных осложнений беременности, опосредованных плацентой (14% против 22%; относительный риск 0,64; 95% ДИ 0,36–1,11). Между одноцентровыми и многоцентровыми исследованиями наблюдалась значительная неоднородность. В анализе подгрупп, НМГ значительно снижал первичный исход у женщин с предыдущей отслойкой, но не в любой из других подгрупп с предыдущими осложнениями. Следует отметить, что со временем ассоциации наследственной тромбофилии и осложнений беременности стали менее сильными или даже отсутствовали, когда были оценены более качественные проспективные исследования. 52
Унаследованная тромбофилия: палка о двух концах | Гематология, Образовательная программа ASH
В 1995 году мои коллеги-младшие исследователи в отделении отметили большое количество выкидышей и мертворождений у женщин, которые участвовали в семейном исследовании, которое было организовано для оценки абсолютного риска ВТЭ в семьях с дефицитом антитромбина, протеина С или протеина S. . Действительно, они обнаружили, что риск у женщин с дефицитом повышается в 2 раза по сравнению с родственниками, не имеющими дефицита. .С тех пор в многочисленных исследованиях изучалась связь между наследственной тромбофилией и различными осложнениями беременности, от единичного выкидыша до внутриутробной гибели плода, преэклампсии, HELLP (гемолиз, повышенные ферменты печени и низкие тромбоциты) и отслойка плаценты. 27,40 Обследование женщин с осложнениями беременности вскоре стало обычной клинической практикой, но основанного на доказательствах ответа о последующих терапевтических последствиях не было. Этот частый клинический вопрос подогревал мой интерес не только к ассоциациям и абсолютным рискам, но и к проверке часто обсуждаемой гипотезы о том, что антикоагуляция низкомолекулярным гепарином (НМГ) может улучшить исход беременности у женщин с наследственной тромбофилией и без нее и с другими необъяснимыми рецидивами. выкидыш.Это был мой первый личный опыт успешного создания и ведения многоцентрового рандомизированного клинического исследования по инициативе исследователя, которое называлось ALIFE. 41 Несмотря на то, что набор и проведение исследования были сложными, а результат был отрицательным, я считаю его завершение, публикацию и влияние на клиническую практику важным моментом в моей карьере. После 15 лет различных клинических испытаний, проведенных коллегами по всему миру, мы теперь знаем, что НМГ не улучшает вероятность живорождения у женщин с невынашиваемым невынашиванием беременности без объяснения причин. 42-45 Однако мы все еще не уверены в том, что это также относится к женщинам с наследственной тромбофилией. 46,47 В исследовании ALIFE подгруппа женщин с наследственной тромбофилией (n = 47) показала тенденцию к преимуществу НМГ и аспирина (относительный риск живорождения 1,31 [95% ДИ 0,74–2,33] для НМГ и аспирин по сравнению с плацебо: относительный риск живорождения 1,22 [95% ДИ 0,69–2,16] для аспирина с соответствующей абсолютной разницей в коэффициентах живорождения 16.3% [95% ДИ, от –18,2% до 50,8%] и 11,8% [95% ДИ, от –21,1% до 44,6%], соответственно). 41 На основе этих результатов мы инициировали исследование ALIFE2, в которое с 2013 года набирают пациентов в Нидерландах, Великобритании и Бельгии и, надеюсь, вскоре в США и Словении. 48
Что касается других осложнений беременности, опосредованных плацентой, результаты метаанализа индивидуальных данных пациентов AFFIRM включали 963 женщины, которые участвовали в 8 рандомизированных контролируемых исследованиях, включая исследование TIPPS, которое было полностью посвящено женщинам с тромбофилией. 49-51 НМГ существенно не снижали риск повторных осложнений беременности, опосредованных плацентой (14% против 22%; относительный риск 0,64; 95% ДИ 0,36–1,11). Между одноцентровыми и многоцентровыми исследованиями наблюдалась значительная неоднородность. В анализе подгрупп, НМГ значительно снижал первичный исход у женщин с предыдущей отслойкой, но не в любой из других подгрупп с предыдущими осложнениями. Следует отметить, что со временем ассоциации наследственной тромбофилии и осложнений беременности стали менее сильными или даже отсутствовали, когда были оценены более качественные проспективные исследования. 52
Каковы классификации наследственной тромбофилии?
Saultz A, Mathews EL, Saultz JW, Judkins D. Клинические исследования. Полезно ли тестирование на гиперкоагулопатию пациентам с ТГВ? J Fam Pract . 2010 май. 59 (5): 291-4. [Медлайн].
Бьюкенен GS, Роджерс GM, филиал DW. Наследственные тромбофилии: генетика, эпидемиология и лабораторная оценка. Лучший Практик Res Clin Obst Gynecol .2003. 138: 128-34.
Franchini M, Veneri D, Salvagno GL, Manzato F, Lippi G. Унаследованная тромбофилия. Clin Lab Sci . 2006. 43: 249-90.
Whitlatch NL, Ortel TL. Тромбофилии: когда проводить обследование и как это помогает. Semin Respir Crit Care Med . 2008. 29: 25-39.
Thomas JH. Лекция Эдгара Дж. Пота. Патогенез, диагностика и лечение тромбозов. Am J Surg .1990 Декабрь 160 (6): 547-51. [Медлайн].
Каккар В.В., Хау СТ, Николаидес А.Н., Ренни Дж. Т., Кларк МБ. Тромбоз глубоких вен голени. Есть ли группа «повышенного риска»? Am J Surg . 1970 Октябрь 120 (4): 527-30. [Медлайн].
Samlaska CP, Джеймс В.Д. Поверхностный тромбофлебит. II. Вторичные гиперкоагуляционные состояния. Дж. Ам Акад Дерматол . 1990 июл.23 (1): 1-18. [Медлайн].
Schafer AI. Состояния гиперкоагуляции. Энн Интерн Мед. . 1985 июн. 102 (6): 814-28. [Медлайн].
Chengelis DL, Bendick PJ, Glover JL, Brown OW, Ranval TJ. Прогрессирование тромбоза поверхностных вен до тромбоза глубоких вен. J Vasc Surg . 1996 24 ноября (5): 745-9. [Медлайн].
Samama MM, Trossaert M, Horellou MH, Elalamy I, Conard J, Deschamps A. Риск тромбоза у пациентов для фактора V Лейден. Кровь . 86. 1995: 4700-4702.
Рик МЭ.Белок С и белок S. Витамин К-зависимые ингибиторы свертывания крови. ЯМА . 1990, 2 февраля. 263 (5): 701-3. [Медлайн].
Bauer KA. Патобиология гиперкоагуляции: клинические особенности, лабораторная оценка и лечение. Хоффман Р. и др., Ред. Гематология: основные принципы и клиническая практика . Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 1991.
Фридман Т., О’Брайен Кун Д., Майклс В. Дж., Бонтемпо Ф., Янг В. Л., Клавихо Дж. А. и др.Наследственные коагулопатии: практическая диагностика и лечение для пластического хирурга. Пласт Реконстр Сург . 2010 май. 125 (5): 1544-52. [Медлайн].
Collen D, Schetz J, de Cock F, Holmer E, Verstraete M. Метаболизм антитромбина III (кофактор гепарина) у человека: эффекты венозного тромбоза и введения гепарина. евро J Clin Invest . 1977 г., 7 (1): 27-35. [Медлайн].
Odegård OR, Abildgaard U. Антитромбин III: критический обзор методов анализа.Значимость различий в состоянии здоровья и болезни. Гемостаз . 1978. 7 (2-3): 127-34. [Медлайн].
Rosendaal FR. Факторы риска венозной тромботической болезни. Тромб Гемост . 1999, август 82 (2): 610-9. [Медлайн].
Miletich J, Sherman L, Broze G Jr. Отсутствие тромбоза у субъектов с гетерозиготной недостаточностью протеина C. N Engl J Med . 1987 15 октября. 317 (16): 991-6. [Медлайн].
Engesser L, Broekmans AW, Briët E, Brommer EJ, Bertina RM.Наследственный дефицит белка S: клинические проявления. Энн Интерн Мед. . 1987 май. 106 (5): 677-82. [Медлайн].
Свенссон П.Дж., Дальбек Б. Устойчивость к активированному протеину С как основа венозного тромбоза. N Engl J Med . 1994 24 февраля. 330 (8): 517-22. [Медлайн].
Peus D, Heit JA, Pittelkow MR. Активированная резистентность к протеину С, вызванная мутацией гена фактора V: общий дефект свертывания крови при хронических венозных язвах ног ?. Дж. Ам Акад Дерматол . 1997 Апрель, 36 (4): 616-20. [Медлайн].
Николс WL, Heit JA. Активированная резистентность к протеину С и тромбоз. Mayo Clin Proc . 1996 Сентябрь 71 (9): 897-8. [Медлайн].
Таун JB. Состояния гиперкоагуляции и необъяснимый тромбоз сосудистого трансплантата. Бернхард В.М., Таун Дж. Б., ред. Осложнения сосудистой хирургии . Сент-Луис, Миссури: Качественное медицинское издательство; 1991.
Эспиноза LR, Hartmann RC.Значение антикоагулянта при волчанке. Ам Дж. Гематол . 1986 22 июля (3): 331-7. [Медлайн].
Табачник-Шор Н.Ф., Липтон С.А. Ассоциация волчаночного антикоагулянта и неваскулитного церебрального инфаркта. Арка Нейрол . 1986, август 43 (8): 851-2. [Медлайн].
Ши В., Крилис С.А., Чонг Б.Х., Гордон С., Честерман С.Н. Распространенность волчаночных антикоагулянтов и антикардиолипиновых антител у здорового населения. Aust N Z J Med .1990 июн.20 (3): 231-6. [Медлайн].
Mueh JR, Herbst KD, Rapaport SI. Тромбоз у больных, принимающих волчаночный антикоагулянт. Энн Интерн Мед. . 1980, февраль 92 (2, часть 1): 156-9. [Медлайн].
Элиас М., Элдор А. Тромбоэмболия у пациентов с циркулирующим антикоагулянтом типа волчанки. Arch Intern Med . 1984 Март 144 (3): 510-5. [Медлайн].
Каплан НМ. Сердечно-сосудистые осложнения пероральных контрацептивов. Анну Рев Мед . 1978. 29: 31-40. [Медлайн].
Durand JL, Bressler R. Клиническая фармакология стероидных оральных контрацептивов. Расширенный медицинский центр . 1979. 24: 97-126. [Медлайн].
Полицейский Столли, Тонация Дж. А., Токман М. С., Сартвелл ЧП, Рутледж А. Х., Джейкобс МП. Тромбоз при применении оральных контрацептивов с низким содержанием эстрогенов. Am J Epidemiol . 1975 сентябрь 102 (3): 197-208. [Медлайн].
DeSancho MT, Дорфф Т., Рэнд Дж. Х.Тромбофилия и риск тромбоэмболических событий у женщин, принимающих оральные контрацептивы и заместительную гормональную терапию. Свертывание крови Фибринолиз . 2010 Сентябрь 21 (6): 534-8. [Медлайн].
Весси М., Мант Д., Смит А., Йейтс Д. Оральные контрацептивы и венозная тромбоэмболия: результаты большого проспективного исследования. Br Med J (Clin Res Ed) . 1986 22 февраля. 292 (6519): 526. [Медлайн].
Helmrich SP, Rosenberg L, Kaufman DW, Strom B, Shapiro S.Венозная тромбоэмболия в связи с использованием оральных контрацептивов. Акушерский гинекол . 1987, январь 69 (1): 91-5. [Медлайн].
Робинсон Г.Е., Буррен Т., Маки И.Дж., Баундс В., Уолш К., Фэйнт Р. и др. Изменения гемостаза после прекращения приема комбинированных противозачаточных таблеток: значение для серьезной хирургии. BMJ . 1991, 2 февраля. 302 (6771): 269-71. [Медлайн].
Seigel DG. Беременность, послеродовой период и стероидные противозачаточные средства. Milbank Mem Fund Q .1972, 50 января (1): Дополнение 2: 15-23. [Медлайн].
Бостонская программа совместного надзора за наркотиками. Оральные контрацептивы и венозная тромбоэмболия, хирургически подтвержденное заболевание желчного пузыря и опухоли груди. Отчет Бостонской программы совместного надзора за наркотиками. Ланцет . 23 июня 1973 г. 1 (7817): 1399-404. [Медлайн].
Куинн Д.А., Томпсон Б.Т., Террин М.Л., Тралл Дж. Х., Атанасулис КА, МакКусик К.А. и др. Перспективное исследование тромбоэмболии легочной артерии у женщин и мужчин. ЯМА . 1992, 7 октября. 268 (13): 1689-96. [Медлайн].
Мащак С.А., Лобо Р.А., Дозоно-Такано Р., Эггена П., Накамура Р.М., Бреннер П.Ф. и др. Сравнение фармакодинамических свойств различных препаратов эстрогена. Am J Obstet Gynecol . 1 ноября 1982 г. 144 (5): 511-8. [Медлайн].
Grady D, Hulley SB, Furberg C. Венозные тромбоэмболические события, связанные с заместительной гормональной терапией. ЯМА . 1997 13 августа. 278 (6): 477.[Медлайн].
Stadel BV. Оральные контрацептивы и сердечно-сосудистые заболевания (первая из двух частей). N Engl J Med . 1981, 10 сентября. 305 (11): 612-8. [Медлайн].
Alkjaersig N, Fletcher A, Burstein R. Связь между использованием оральных контрацептивов и тромбоэмболией: новый подход к ее исследованию, основанный на хроматографии фибриногена плазмы. Am J Obstet Gynecol . 1975 Май. 122 (2): 199-211. [Медлайн].
Siegbahn A, Ruusuvaara L.Возрастная зависимость фибринолитических компонентов крови и влияние низких доз пероральных контрацептивов на коагуляцию и фибринолиз у подростков. Тромб Гемост . 1988 22 декабря. 60 (3): 361-4. [Медлайн].
Srinivasan S, Solash J, Redner A, Moser C, Farhangian D, Lucas TR и др. Изменение характеристик поверхностного заряда сосудистой системы пероральными противозачаточными стероидами. Контрацепция . 1974, 9 (3): 291-303. [Медлайн].
Оски Ф.А., Любин Б., Бухерт ЭД.Снижение фильтруемости эритроцитов с помощью оральных контрацептивов. Энн Интерн Мед. . 1972 Сентябрь 77 (3): 417-9. [Медлайн].
Аронсон HB, Magora F, Schenker JG. Влияние оральных контрацептивов на вязкость крови. Am J Obstet Gynecol . 1971, 1 августа. 110 (7): 997-1001. [Медлайн].
Драйер Н.А., Пиццо С.В. Свертывание крови и идиопатическая тромбоэмболия у фертильных женщин. Контрацепция . 1980 22 августа (2): 123-35.[Медлайн].
Сагар С., Стаматакис Дж. Д., Томас Д. П., Каккар В. В.. Оральные контрацептивы, активность антитромбина-III и послеоперационный тромбоз глубоких вен. Ланцет . 6 марта 1976 г. (7958): 509-11. [Медлайн].
фон Каулла Э, фон Каулла KN. Оральные контрацептивы и низкая активность антитромбина-3. Ланцет . 1970 г. 3 января (7636): 36. [Медлайн].
Pizzo SV. Венозный тромбоз. Коепке Я.А., изд. Лаборатория гематологии .Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 1984. Том 2:
.
Миллер К.Е., Пиццо С.В. Венозная и артериальная тромбоэмболия у женщин, принимающих оральные контрацептивы. Am J Obstet Gynecol . 1 декабря 1982 г. 144 (7): 824-7. [Медлайн].
Astedt B, Isacson S, Nilsson IM, Pandolfi M. Тромбоз и оральные контрацептивы: возможная предрасположенность. Br Med J . 1973 15 декабря. 4 (5893): 631-4. [Медлайн].
Джадд Х.Л., Мелдрам Д.Р., Дефтос Л.Дж., Хендерсон Б.Е.Заместительная терапия эстрогенами: показания и осложнения. Энн Интерн Мед. . 1983 февраль 98 (2): 195-205. [Медлайн].
Гудрич С.М., Вуд Дж. Влияние эстрадиола-17-бета на растяжимость периферических вен и скорость венозного кровотока. Am J Obstet Gynecol . 1966, 1 октября. 96 (3): 407-12. [Медлайн].
Алькьерсиг Н., Флетчер А.П., де Зиглер Д., Штейнгольд К.А., Мелдрам Д.Р., Джадд Х.Л. Свертывание крови у женщин в постменопаузе, получавших лечение эстрогенами: сравнение трансдермального и перорального введения. Дж. Лаборатория Клин Мед. . 1988 Февраль 111 (2): 224-8. [Медлайн].
Lipton A, Харви HA, Гамильтон RW. Венозный тромбоз как побочный эффект лечения тамоксифеном. Центр лечения рака . 1984 июн. 68 (6): 887-9. [Медлайн].
Фишер Б., Костантино Дж., Редмонд С., Пуассон Р., Боуман Д., Кутюр Дж. И др. Рандомизированное клиническое исследование по оценке тамоксифена в лечении пациентов с раком молочной железы без лимфоузлов и опухолями, положительными по рецепторам эстрогена. N Engl J Med . 1989, 23 февраля. 320 (8): 479-84. [Медлайн].
Jordan VC, Fritz NF, Tormey DC. Долгосрочная адъювантная терапия тамоксифеном: влияние на глобулин, связывающий половые гормоны, и антитромбин III. Рак Res . 1987 15 августа. 47 (16): 4517-9. [Медлайн].
Любовь RR, Суравич Т.С., Вильямс ЕС. Уровень антитромбина III, уровень фибриногена и количество тромбоцитов изменяются при адъювантной терапии тамоксифеном. Arch Intern Med .1992 Февраль 152 (2): 317-20. [Медлайн].
Оже MJ, Маки MJ. Влияние тамоксифена на свертываемость крови. Рак . 1988 г. 1. 61 (7): 1316-9. [Медлайн].
Бертелли Г., Пронзато П., Аморосо Д., Кузимано М.П., Конте П.Ф., Монтанья Г. и др. Адъювант тамоксифена при первичном раке молочной железы: влияние на уровни липидов плазмы и антитромбина III. Лечение рака груди . 1988 12 декабря (3): 307-10. [Медлайн].
Weitz IC, Израиль VK, Liebman HA.Венозный тромбоз, связанный с тамоксифеном, и активированная резистентность к протеину С из-за фактора V Лейдена. Рак . 1997 15 мая. 79 (10): 2024-7. [Медлайн].
Боннар Дж. Гемостатическая функция и коагулопатия во время беременности. Акушерский гинекол Анну . 1978. 7: 195-217. [Медлайн].
Боннар Дж., Макникол Г.П., Дуглас А.С. Фибринолитическая ферментная система и беременность. Br Med J . 1969 16 августа 3 (5667): 387-9. [Медлайн].
Comp PC, Thurnau GR, Welsh J, Esmon CT.Функциональные и иммунологические уровни протеина S снижаются во время беременности. Кровь . 1986 Октябрь 68 (4): 881-5. [Медлайн].
Ааро Л.А., Джонсон Т.Р., Юргенс Дж.Л. Острый тромбоз глубоких вен, связанный с беременностью. Акушерский гинекол . 1966, 28 октября (4): 553-8. [Медлайн].
Pomp ER, Lenselink AM, Rosendaal FR, Doggen CJM. Беременность, послеродовой период и посттромботические дефекты: риск венозного тромбоза в исследовании MEGA. Дж. Тромб Хемост . 2008. 6: 632-637.
Макколл, доктор медицины, Рамзи Д.Э., Тейт Р.С., Уокер ID, Макколл Ф., Конки Д.А. Факторы риска венозной тромбоэмболии, связанной с беременностью. Тромб Гемост . 1997 Октябрь 78 (4): 1183-8. [Медлайн].
Beller FK. Тромбоэмболическая болезнь при беременности. Андерсон A, изд. Тромбоэмболические заболевания . Нью-Йорк, штат Нью-Йорк: Харпер и Роу; 1968.
Homans J. Тромбоз глубоких вен ног из-за длительного сидения. N Engl J Med . 1954, 28 января, 250 (4): 148-9. [Медлайн].
Lord RS, McGrath M. Travelers Венозный тромбоз. 1993.
Кушман М. Эпидемиология и факторы риска венозного тромбоза. Семин Гематол . 2007 апр. 44 (2): 62-9. [Медлайн].
Лорд RS. Тромбоз глубоких вен, связанный с авиаперелетами. Сиднейские виды. Кардиоваск Хирургия . 2001 Apr, 9 (2): 149-50; обсуждение 153-6. [Медлайн].
Парси К.А., МакГрат Массачусетс, Лорд Р.С. Венозная тромбоэмболия путешественника. Кардиоваск Хирургия . 2001 апр. 9 (2): 157-8. [Медлайн].
McQuillan AD, Eikelboom JW, Baker RI. Венозная тромбоэмболия у путешественников: можем ли мы выявить тех, кто находится в группе риска ?. Свертывание крови Фибринолиз . 14 октября 2003 г. (7): 671-5. [Медлайн].
Синдром Варки А. Труссо: множественные определения и множественные механизмы. Кровь .2007. 110: 1723-1729.
Канаан А.О., Сильва М.А., Донован Дж.Л., Рой Т., Аль-Хомси А.С. Мета-анализ профилактики венозной тромбоэмболии у пациентов с заболеваниями. Клин Тер . 2007 29 ноября (11): 2395-405. [Медлайн].
Geerts WH, Code KI, Jay RM, Chen E, Szalai JP. Проспективное исследование венозной тромбоэмболии после обширной травмы. N Engl J Med . 1994 15 декабря. 331 (24): 1601-6. [Медлайн].
Perry SL, Ortel TL.Клинико-лабораторная оценка тромбофилии. Clin Chest Med . 2003 24 марта (1): 153-70. [Медлайн].
Ковалевски Р., Соболевски К., Воланска М., Гацко М. Матричные металлопротеиназы в стенке вены. Инт Ангиол . 2004 г., 23 (2): 164-9. [Медлайн].
Кагель Э.М., Райан ГМ. Осложнения при внутривенном катетере кисти и предплечья. J Травма . 2004, январь, 56 (1): 123-7. [Медлайн].
Gupta A, Mehta Y, Juneja R, Trehan N.Влияние материала канюли на частоту тромбофлебита периферических вен. Анестезия . 2007 ноябрь 62 (11): 1139-42. [Медлайн].
Сиддоуэй Л.А. Амиодарон: руководство по применению и мониторинг. Ам Фам Врач . 1 декабря 2003 г. 68 (11): 2189-96. [Медлайн].
Хохмайр М., Валипур А., Ошац Э, Холлаус П., Хубер М., Крис Бургхубер О. От боли в горле до отделения интенсивной терапии: синдром Лемьера. Wien Klin Wochenschr .2006 май. 118 (7-8): 243-6. [Медлайн].
Brinsuk M, Tank J, Luft FC, Busjahn A, Jordan J. Наследование венозной функции у людей. Артериосклер Тромб Vasc Biol . 2004 24 января (1): 207-11. [Медлайн].
Tröbinger C, Wiedermann CJ. Болезнь Мондора грудной клетки, вызванная бодибилдингом. Физика . 2017 23 января: 133-135. [Медлайн].
Амано М., Симидзу Т. Болезнь Мондора: Обзор литературы. Медицинский работник . 2018 18 мая. [Medline].
Джебара С., Хенкертс Л., Ванбрабант П. Двусторонняя болезнь Мондора при инфицировании вирусом чикунгунья. Сообщения о случаях болезни Oxf Med . 2020 авг.2020 (8): omaa065. [Медлайн].
Мароне Э.М., Боналуми Дж., Курчи Р., Арзини А., Кьерико С., Марацци Дж. И др. Характеристики венозной тромбоэмболии у пациентов с COVID-19: многоцентровый опыт Северной Италии. Анн Васк Сург .2020 14 июля. [Medline].
Belcaro G, Nicolaides AN, Errichi BM, Cesarone MR, De Sanctis MT, Incandela L, et al. Поверхностный тромбофлебит ног: рандомизированное контролируемое катамнестическое исследование. Ангиология . 1999 июл.50 (7): 523-9. [Медлайн].
Agnelli G, Verso M, Ageno W, Imberti D, Moia M, Palareti G и др. Регистр MASTER по венозной тромбоэмболии: описание исследуемой когорты. Исследование тромба .2008. 121: 605-610.
Galanaud JP, Sevestre MA, Pernod G, Kahn SR, Genty C, Terrisse H, et al. Долгосрочный риск рецидива венозной тромбоэмболии после изолированного тромбоза поверхностных вен. Дж. Тромб Хемост . 2017 июн.15 (6): 1123-1131. [Медлайн].
Де Стефано В., Росси Э., Пачарони К., Леоне Г. Скрининг наследственной тромбофилии: показания и терапевтические последствия. Trends Hematol Oncol . 2002. 87: 1095-1108.
Crandon AJ, Peel KR, Anderson JA, Thompson V, McNicol GP. Послеоперационный тромбоз глубоких вен: выявление пациентов из группы высокого риска. Br Med J . 2 августа 1980 г. 281 (6236): 343-4. [Медлайн].
Sue-Ling HM, Johnston D, McMahon MJ, Philips PR, Davies JA. Предоперационная идентификация пациентов с высоким риском тромбоза глубоких вен после плановой обширной абдоминальной хирургии. Ланцет . 1986 24 мая. 1 (8491): 1173-6. [Медлайн].
Енот WW. Эпидемиология венозной тромбоэмболии. Энн Сург . 1977, август 186 (2): 149-64. [Медлайн].
Schina MJ Jr, Neumyer MM, Healy DA, Atnip RG, Thiele BL. Влияние возраста на физиологические параметры вен. J Vasc Surg . 1993 18 ноября (5): 749-52. [Медлайн].
Belcaro G, Nicolaides AN, Errichi BM, Cesarone MR, De Sanctis MT, Incandela L. Поверхностный тромбофлебит ног: рандомизированное контролируемое исследование с последующим наблюдением. Ангиология . 1999 июл.50 (7): 523-9. [Медлайн].
Ascer E, Lorensen E, Pollina RM, Gennaro M. Предварительные результаты неоперативного подхода к тромбофлебиту сафенофеморального соединения. J Vasc Surg . 1995 22 ноября (5): 616-21. [Медлайн].
Кэмпбелл Б. Варикозное расширение вен и их лечение. BMJ . 2006 5 августа. 333 (7562): 287-92. [Медлайн].
Plate G, Eklöf B, Jensen R, Ohlin P.Тромбоз глубоких вен, тромбоэмболия легочной артерии и неотложные операции при тромбофлебите длинной подкожной вены. Акта Чир Сканд . 1985. 151 (3): 241-4. [Медлайн].
Gjores JE. Хирургическая терапия восходящего тромбофлебита подкожной системы. Ангиология . 1962 Май. 13: 241-3. [Медлайн].
Бергквист Д., Линдблад Б. 30-летнее исследование тромбоэмболии легочной артерии, подтвержденной при вскрытии: анализ 1274 хирургических пациентов. руб. J Surg . 1985 Февраль 72 (2): 105-8. [Медлайн].
Bergqvist D, Jaroszewski H. Тромбоз глубоких вен у пациентов с поверхностным тромбофлебитом голени. Br Med J (Clin Res Ed) . 1986 8 марта. 292 (6521): 658-9. [Медлайн].
Галлоуэй Дж. М., Кармоди А. М., Мавор Дж. Э. Тромбофлебит длинной подкожной вены, осложненный тромбоэмболией легочной артерии. руб. J Surg . 1969 Май. 56 (5): 360-1. [Медлайн].
Леон Л., Яннукас А.Д., Додд Д., Чан П., Лабропулос Н.Клиническое значение тромбоза поверхностных вен. евро J Vasc Endovasc Surg . 2005 29 января (1): 10-7. [Медлайн].
Di Nisio M, Middeldorp S. Лечение поверхностного тромбофлебита нижних конечностей. ЯМА . 2014 19 февраля. 311 (7): 729-30. [Медлайн].
Roach RE, Lijfering WM, van Hylckama Vlieg A, Helmerhorst FM, Rosendaal FR, Cannegieter SC. Риск венозного тромбоза у лиц с тромбозом поверхностных вен в анамнезе и приобретенными факторами риска венозного тромбоза. Кровь . 2013 19 декабря. 122 (26): 4264-9. [Медлайн].
Schönauer V, Kyrle PA, Weltermann A, Minar E, Bialonczyk C, Hirschl M, et al. Поверхностный тромбофлебит и риск рецидива венозной тромбоэмболии. J Vasc Surg . 2003 Апрель, 37 (4): 834-8. [Медлайн].
Бендик П.Дж., Райан Р., Альперс М. и др. Клиническое значение поверхностного тромбофлебита. Дж, Vasc Technol . 1995. 19: 57-61.
Verlato F, Zucchetta P, Prandoni P, Camporese G, Marzola MC, Salmistraro G и др.Неожиданно высокая частота тромбоэмболии легочной артерии у пациентов с поверхностным тромбофлебитом бедра. J Vasc Surg . 1999 г. 30 (6): 1113-5. [Медлайн].
Krunes U, Lindner F, Lindner R, Gnutzmann J. Genugt die klinische untersuchung einer varikophlebitis des unterschenkels ?. Флебология . 1999. 28: 93-6.
Трухильо-Сантос Дж., Эррера С., Рпаж М.А., Сото М.Дж., Равентос А., Санчес Р. и др. Прогнозирование неблагоприятного исхода у амбулаторных пациентов с острым тромбозом глубоких вен: данные реестра RIETE. J Vasc Surg . 2006. 44: 789-793.
Торпи Дж. М., Берк А. Э., Гласс РМ. Страница пациента JAMA. Тромбофлебит. ЯМА . 26 июля 2006 г., 296 (4): 468. [Медлайн].
Greenleaf JE, Rehrer NJ, Mohler SR, Quach DT, Evans DG. Удаление опоры кресла в самолете: индукция иммобилизационных тромбоэмболий ?. Спортивная медицина . 2004. 34 (11): 705-25. [Медлайн].
Lee C, Moll S. Мигрирующий поверхностный тромбофлебит у курильщика каннабиса. Тираж . 2014 8 июля. 130 (2): 214-5. [Медлайн].
Nachmann MM, Jaffe JS, Ginsberg PC, Horrow MM, Harkaway RC. Серповидноклеточный эпизод, проявляющийся в виде поверхностного тромбофлебита полового члена. Дж. Ам Остеопат Асс . 2003 Февраль 103 (2): 102-4. [Медлайн].
Hutachuda P, Hanamornroongruang S, Pattanaprichakul P, Chanyachailert P, Sitthinamsuwan P. Надежность гистопатологических признаков для различения кожного узелкового полиартериита и поверхностного тромбофлебита. Гистопатология . 19 апреля 2018 г. [Medline].
[Рекомендации] Кеарон С., Акл Э.А., Комерота А.Дж., et al. Антитромботическая терапия при ВТЭ: Антитромботическая терапия и профилактика тромбоза, 9-е изд: Руководства по клинической практике Американского колледжа грудных врачей. Сундук . 2012, февраль, 141 (2 доп.): E419S-94S. [Медлайн]. [Полный текст].
Di Nisio M, Wichers IM, Middeldorp S. Лечение поверхностного тромбофлебита ноги. Кокрановская база данных систематических обзоров . 2007. 2: 1-90.
Даунинг LJ, Strieter RM, Kadell AM, Wilke CA, Greenfield LJ, Wakefield TW. Низкие дозы низкомолекулярного гепарина обладают противовоспалительным действием при венозном тромбозе. J Vasc Surg . 1998 28 ноября (5): 848-54. [Медлайн].
Marchiori A, Verlato F, Sabbion P, Camporese G, Rosso F, Mosena L. и др. Сравнение высоких и низких доз нефракционированного гепарина для лечения поверхностного тромбофлебита голени.Проспективное контролируемое рандомизированное исследование. Гематология . 2002 май. 87 (5): 523-7. [Медлайн].
Rathbun SW, Aston CE, Whitsett TL. Рандомизированное испытание далтепарина по сравнению с ибупрофеном для лечения поверхностного тромбофлебита. Дж. Тромб Хемост . 2012 май. 10 (5): 833-9. [Медлайн]. [Полный текст].
Bachmeyer C, Elalamy I. Ривароксабан как эффективное средство лечения рецидивирующего поверхностного тромбофлебита, связанного с первичным антифосфолипидным синдромом. Клин Эксперимент Дерматол . 2014 Октябрь 39 (7): 840-1. [Медлайн].
Di Nisio M, Wichers IM, Middeldorp S. Лечение поверхностного тромбофлебита ноги. Кокрановская база данных Syst Rev . 2013 30 апреля. 4: CD004982. [Медлайн].
Захер Р. Дефицит антитромбина при особых клинических синдромах — Часть II: панельная дискуссия №2. Семин Гематол . 1995 г., 32 октября (4 приложение 2): 67-71. [Медлайн].
Chengelis DL, Bendick PJ, Glover JL, Brown OW, Ranval TJ.Прогрессирование тромбоза поверхностных вен до тромбоза глубоких вен. J Vasc Surg . 1996 24 ноября (5): 745-9. [Медлайн].
Sigg K. Лечение варикозного расширения вен и сопутствующих осложнений; (амбулаторное лечение флебита давящей повязкой). Ангиология . 1952 г., 3 (5): 355-79. [Медлайн].
Belcaro G, Cesarone MR, Rohdewald P, Ricci A, Ippolito E, Dugall M, et al. Профилактика венозного тромбоза и тромбофлебита при дальних перелетах пикногенолом. Clin Appl Thromb Hemost . 2004 октября 10 (4): 373-7. [Медлайн].
De Sanctis MT, Cesarone MR, Incandela L, Belcaro G, Griffin M. Лечение тромбофлебита поверхностных вен руки гелем Essaven — плацебо-контролируемое рандомизированное исследование. Ангиология . 2001 декабрь 52 Дополнение 3: S63-7. [Медлайн].
Битти Дж, Фитридж Р., Бенвенист Дж., Гринштейн Д. Острый поверхностный венозный тромбофлебит: играет ли роль экстренная хирургия ?. Инт Ангиол . 2002 21 марта (1): 93-5. [Медлайн].
Test | Панель «Наследственная тромбофилия Invitae»
Анализ и техническая информация
Invitae — аккредитованный Колледжем американских патологов (CAP) и внесены поправки в клинические лаборатории.
(CLIA) -сертифицированная клинико-диагностическая лаборатория, выполняющая полное секвенирование генов и анализ делеций / дупликаций
с использованием технологии секвенирования нового поколения (NGS).
Наш анализ последовательности охватывает клинически важные области каждого гена, включая кодирующие экзоны и от 10 до 20 оснований.
пары соседних интронных последовательностей по обе стороны от кодирующих экзонов в транскрипте, перечисленном ниже, в зависимости от
на конкретный ген или тест. Кроме того, анализ охватывает отдельные варианты без кодирования. Любые варианты, которые выпадают
за пределами этих регионов не анализируются. Любые ограничения в анализе этих генов будут перечислены в отчете.
Свяжитесь со службой поддержки клиентов с любыми вопросами.
На основании результатов валидационного исследования этот анализ достигает> 99% аналитической чувствительности и специфичности для одного
нуклеотидные варианты, вставки и делеции длиной <15 п.н., а также делеции и дупликации на уровне экзонов.
Методы Invitae также обнаруживают вставки и делеции размером более 15 п.н., но меньше, чем полный экзон, но чувствительность
поскольку они могут быть незначительно уменьшены. Анализ делеции / дупликации Invitae определяет количество копий на одном экзоне
разрешение практически на всех целевых экзонах.Однако в редких случаях события числа копий одного экзона могут не происходить.
проанализированы из-за присущих свойств последовательностей или изолированного снижения качества данных. Определенные типы вариантов,
такие как структурные перестройки (например, инверсии, события конверсии генов, транслокации и т. д.) или варианты
встроены в последовательность со сложной архитектурой (например, короткие тандемные повторы или сегментные дупликации), не могут быть
обнаружен. Кроме того, может быть невозможно полностью разрешить некоторые детали о вариантах, такие как мозаицизм,
фазирование или неоднозначность отображения.Если явно не указано иное, изменения последовательности в промоторе, некодирующих экзонах,
и другие некодирующие области не охватываются этим анализом. Пожалуйста, ознакомьтесь с определением теста на нашем веб-сайте для
подробные сведения о регионах или типах вариантов, которые включены или исключены для этого теста. Этот отчет отражает
анализ выделенного образца геномной ДНК. В очень редких случаях (циркулирующее гематолимфоидное новообразование, костный мозг
трансплантат, недавнее переливание крови) анализируемая ДНК может не отражать конституциональный геном пациента.
| Джин | Ссылка на стенограмму | Анализ секвенирования | Анализ удаления / дублирования |
|---|---|---|---|
| F2 * | NM_000506.3 | ||
| F5 * | NM_000130.4 | ||
| F9 | NM_000133.3 | ||
| МПЛ | NM_005373.2 | ||
| ПРОЦЕСС | NM_000312.3 | ||
| ПРОС1 | NM_000313.3 | ||
| SERPINC1 | NM_000488.3 |
F2: Только вариант протромбина G20210A (c. * 97G> A).
F5: Только вариант Factor V Leiden.
Унаследованная тромбофилия — Консультант по терапии рака
Унаследованная тромбофилия. Протромботическое расстройство. Предрасположенность к образованию тромбов.
1. Что должен знать каждый врач
Тромбофилии — это гетерогенная группа состояний, предрасполагающих людей к тромбоэмболическим событиям (ВТЭ).Большинство из них — венозные тромбозы.
Нормальный гемостаз включает тонкий баланс прокоагулянтных белков, которые способствуют образованию сгустка в случае кровотечения или повреждения эндотелия, и антикоагулянтных белков, которые предотвращают образование слишком большого количества сгустка, тем самым препятствуя кровотоку (ВТЭ). Большинство тромбофилий связано с недостатком или отклонением антикоагулянтных белков. В некоторых случаях они связаны с увеличением количества прокоагулянтных белков.
Тромбоэмболия — причина номер один или номер два (наиболее частая) материнской смертности в развитых странах.Связь между тромбофилиями и тромбоэмболией очень сильна. Тромбофилии связаны с повышенным риском неблагоприятных акушерских исходов, таких как мертворождение, нарушение роста плода и преэклампсия. Связь между тромбофилиями и акушерскими осложнениями слаба и противоречива. У большинства женщин с тромбофилиями исход беременности НОРМАЛЬНЫЙ.
Наиболее распространенные и важные тромбофилии включают лейденскую мутацию фактора V, мутацию гена протромбина G20210A, дефицит антитромбина III (AT III), дефицит протеина C и дефицит протеина S.
-
Люди, происходящие из Северной Европы и некоторых частей Ближнего Востока, имеют более высокую частоту наследственных тромбофилий.
-
Люди с ВТЭ, особенно во время беременности, подвергаются повышенному риску.
-
Лица с сильным семейным анамнезом ВТЭ (родственники первой степени родства) относятся к группе повышенного риска.
-
Лица с такими осложнениями беременности, как мертворождение, имеют несколько повышенный риск развития некоторых тромбофилий.
Тромбофилии и неблагоприятные исходы беременности
Тромбофилии являются фактором риска гибели плода (потери после 10 недель беременности) и мертворождения (потери после 20 недель беременности). Они НЕ были связаны с потерей беременности на ранних сроках или повторяющимися выкидышами на ранних сроках. Лейденский фактор V и мутации гена протромбина связаны примерно с трехкратным увеличением риска поздней гибели плода. Этот уровень риска аналогичен демографическим факторам, таким как ожирение и пожилой возраст матери.Примечательно, что тромбофилии НЕ были связаны с потерей беременности в нескольких проспективных когортных исследованиях.
Тромбофилии были связаны с повышенным риском преэклампсии в некоторых, но не в большинстве ретроспективных исследований. Кроме того, в проспективных когортных исследованиях тромбофилии НЕ были связаны с преэклампсией.
В нескольких ретроспективных исследованиях тромбофилии были связаны с плодами, малыми для гестационного возраста. Однако в большинстве ретроспективных и всех проспективных исследованиях НЕТ связи между малым для гестационного возраста плодом и тромбофилиями.
Тромбофилии были связаны с отслойкой в нескольких небольших ретроспективных исследованиях. В проспективных исследованиях НЕТ связи между отслойкой и тромбофилиями.
Тромбофилии и ВТЭ
Тромбофилии увеличивают риск ВТЭ, связанного с беременностью, примерно в восемь раз. Риск выше для людей с более чем одной тромбофилией. Примером может служить тот, кто является гетерозиготным по лейденскому фактору V и мутациям гена протромбина.Эти люди называются «сложными» гетерозиготами.
Большинство тромбофилий являются аутосомно-доминантными с переменной пенетрантностью. Многие люди протекают бессимптомно и никогда не страдают ВТЭ. Риск тромбоза варьируется в зависимости от тромбофилии. Дефицит ATIII является наиболее тромбогенным, за ним следует дефицит протеина C и дефицит протеина S. Лейденские мутации фактора V и протромбина G20210A являются менее тромбогенными, а гипергомоцистеинемия является наименее тромбогенной.Хотя описаны другие тромбофилии, их связь с ВТЭ неясна, и тестирование в настоящее время не рекомендуется.
Распространенность тромбофилий намного выше у женщин с ВТЭ, связанными с беременностью, по сравнению с населением в целом. У женщин с ВТЭ, ассоциированным с беременностью, 20-40% будут иметь лейденский фактор V, 6-15% — мутацию протромбина G20210A, 1–2% дефицит протеина C и протеина S и менее 1% дефицита ATIII. Распространенность мутации C677T MTHFR составляет 10%, что аналогично показателям в общей популяции.
Факторы беременности и свертывания крови
Беременность связана со следующими состояниями:
-
Повышение факторов свертывания крови (факторы II, VII, VIII, X и XII)
-
Снижение уровня антикоагулянтного белка S
-
Повышение уровня плазминоген-активирующего фактора-I (прокоагулянт)
-
Повышенная устойчивость к активированному протеину C (устойчивость к антикоагулянтному протеину)
-
Нарушение фибринолиза
Распространенность и генетика конкретных тромбофилий
Как следует из этого термина, наследственные тромбофилии — это генетические состояния.Распространенность зависит от расы / этнической принадлежности и известна для некоторых групп населения. Беременность усиливает свертываемость.
Лейденская мутация фактора V вызывает нарушение белка фактора V. Обычно активированный фактор V инактивируется комплексом протеин C: протеин S. Аномальный лейденский белок фактора V сложнее инактивировать, и, таким образом, сгусток продолжает формироваться.
Состояние аутосомно-доминантное. Поражаются гетерозиготные особи. Редкие особи гомозиготны.
Лейденская мутация фактора V присутствует примерно у 5% европеоидов, 8–9% скандинавов, 1–3% афроамериканцев.Это редко встречается у чернокожих африканцев и азиатов.
Мутация гена протромбина G20210A — это мутация в промоторе протромбина (фактор II), которая приводит к увеличению протромбина на 150–200%. Состояние аутосомно-доминантное. Поражаются гетерозиготные особи. Редкие особи гомозиготны. Ген протромбина присутствует примерно у 2–3% европейцев.
Дефицит протеина C включает снижение количества и / или активности протеина C. Дефицит протеина C является аутосомно-доминантным и связан с более чем 160 мутациями.Поражаются гетерозиготные особи. Дефицит протеина C присутствует у 0,2% -0,5% европейцев.
Дефицит протеина S включает снижение количества, активности или кофакторной активности протеина S. Дефицит протеина S является аутосомно-доминантным. Поражаются гетерозиготные особи. Дефицит протеина S присутствует у 0,8% кавказцев.
Дефицит антитромбина III вызывает снижение количества или активности ATIII. Дефицит ATIII является аутосомно-доминантным.Поражаются гетерозиготные особи. Дефицит ATIII встречается редко и встречается примерно у 0,07% кавказцев.
Гипергомоцистеинемия связана с инфарктом миокарда. Связь с ВТЭ слабая.
Есть несколько мутаций, связанных с гипергомоцистеинемией. На уровень гомоцистеина влияют многие факторы, и многие люди с этими мутациями имеют нормальный уровень гомоцистеина. Наиболее распространенной является мутация метилентетрагидрофолатредуктазы (MTHFR) C677T.Поражаются только гомозиготы. 10-11% европейцев являются гомозиготными по мутации C677T MTHFR. Второй по распространенности является мутация A1298C MTHFR. Поражаются только гомозиготы. 4–6% европейцев являются гомозиготами по мутации A1298C MTHFR.
Редкие люди имеют мутацию цистатионин-бета-синтазы (1 из 200 000). Гетерозиготы с этой мутацией поражаются.
2. Диагностика и дифференциальный диагноз
Диагностика большинства тромбофилий относительно проста и проводится с помощью анализов крови.Дифференциальный диагноз не является важной проблемой при обследовании пациента на наследственные тромбофилии. На тесты на тромбофилии может повлиять антикоагулянтная терапия и беременность.
Кого следует обследовать на тромбофилии?
Популяция пациентов, которым следует пройти тестирование на тромбофилии, неоднозначна.
-
Пациенты с ВТЭ должны быть обследованы на тромбофилии
-
Некоторые органы рекомендуют проводить тестирование пациентов с родственником первой степени родства с тромбофилией высокого риска (например, с дефицитом ATIII).
-
Некоторые авторитетные источники рекомендуют тестировать пациентов с родственником первой степени с ВТЭ до 50 лет, у которых не было явного побуждающего события (например, операции на бедре).
-
Большинство авторитетных источников НЕ рекомендуют проводить тестирование на наследственные тромбофилии у пациентов с неблагоприятными акушерскими исходами, такими как мертворождение, преэклампсия, плод с SGA или отслойка плода.
Специфические тесты на тромбофилии
Фактор V Лейден — это генетический тест, который можно оценить с помощью образца крови.Это надежно, даже если пациентка принимает антикоагулянтную терапию или беременна. Тест будет зарегистрирован как отрицательный, гетерозиготный (пораженный) или гомозиготный (пораженный). Это также можно оценить с помощью функционального анализа, который оценивает устойчивость фактора V к активированному белку C. Последний анализ не подходит для женщин, принимающих антикоагулянтную терапию. Хотя этот анализ идентифицирует несколько иную группу женщин, чем анализ фактора V Лейдена, в большинстве случаев проще всего просто заказать анализ фактора V Лейдена.
Мутация гена протромбина G20210A — это генетический тест, который можно оценить с помощью образца крови. Это надежно, даже если пациентка принимает антикоагулянтную терапию или беременна. Тест будет зарегистрирован как отрицательный, гетерозиготный (пораженный) или гомозиготный (пораженный).
Тест на дефицит ATII — тест на свертывание. Это ненадежно, если пациент принимает антикоагулянтную терапию. В таких случаях тестирование следует отложить до тех пор, пока пациент не перестанет принимать антикоагулянтную терапию.Тест надежен при беременности.
Тест на дефицит протеина C — тест на свертываемость. Это ненадежно, если пациент принимает антикоагулянтную терапию. В таких случаях тестирование следует отложить до тех пор, пока пациент не перестанет принимать антикоагулянтную терапию. Тест не является надежным при беременности или если пациентка принимает оральные контрацептивы, содержащие эстроген. В таких случаях тестирование следует отложить до 6 недель после родов.
Тест на дефицит протеина S — тест на свертываемость.Это ненадежно, если пациент принимает антикоагулянтную терапию. В таких случаях тестирование следует отложить до тех пор, пока пациент не перестанет принимать антикоагулянтную терапию. Тест не является надежным при беременности или если пациентка принимает оральные контрацептивы, содержащие эстроген. На самом деле, это особенно ненадежно при беременности. В таких случаях в идеале тестирование следует отложить до 6 недель после родов. Хотя это несколько спорно, есть некоторые свидетельства того, что уровни СВОБОДНОГО антигена протеина S менее 0% во втором триместре и менее 24% в третьем триместре указывают на дефицит протеина S во время беременности.Таким образом, если тестирование необходимо провести во время беременности, эти значения можно использовать в качестве порогового значения для данного состояния.
Обследование на гипергомоцистеинемию может быть сложным. Это делается с помощью анализа крови. Лучше всего получить уровень гомоцистеина, когда пациент голоден в течение 12 часов. Уровень выше 10 мг / дл считается повышенным. Тесты на мутации, связанные с гипергомоцистеинемией, являются генетическими тестами и могут быть получены в любое время с помощью анализа крови. Большинство авторитетов НЕ рекомендуют тестирование на гипергомоцистеинемию или мутации, связанные с гипергомоцистеинемией, в случаях ВТЭ.
Если трудно интерпретировать лабораторные показатели тромбофилий, особенно функциональные анализы. Может быть полезно записаться на консультацию к гематологу.
3. Менеджмент
Дородовой
Ключевым вопросом в дородовом ведении тромбофилий является профилактика ВТЭ. Спорный вопрос о том, каким пациентам следует проводить дородовую тромбопрофилактику или антикоагулянтную терапию, для чего существует несколько вариантов. Лечение пациентов антикоагулянтной терапией, направленной на улучшение акушерского исхода, считается экспериментальным.Дополнительное дородовое наблюдение за плодом должно проводиться по обычным акушерским показаниям.
во время родов
Цель тактики ведения родов — избежать как ВТЭ, так и кровотечения. Часто возникает желание получить безопасную нейроаксиальную анальгезию. Всегда есть потенциальная необходимость в хирургическом вмешательстве. Существует несколько вариантов антикоагулянтной терапии во время родов.
Послеродовой
Есть несколько вариантов послеродовой антикоагулянтной терапии
Сроки и маршрут доставки
Ятрогенные преждевременные роды не показаны из-за диагноза тромбофилии (или ВТЭ).Разумно предложить стимуляцию родов или запланировать кесарево сечение после 39 недель беременности, чтобы оптимально управлять антикоагулянтной терапией. Кесарево сечение у женщин с тромбофилией должно проводиться по обычным акушерским показаниям.
Антенатальное тестирование плода
Нет доказанной эффективности дополнительных антенатальных тестов плода, таких как NST, для единственного указания на тромбофилию или тромбофилию с ВТЭ. У пациентов с предшествующими неблагоприятными акушерскими исходами (с тромбофилиями или без них) обследование следует проводить на основании акушерского анамнеза (например, предшествующих мертворождений).
Дородовая антикоагулянтная терапия по акушерским показаниям
Нет основанных на доказательствах рекомендаций по использованию дородовой антикоагулянтной терапии в попытке улучшить акушерский исход у пациентов с предшествующими неблагоприятными акушерскими исходами, такими как потеря беременности, преэклампсия, малый для гестационного возраста плод и прерывание беременности. Некоторые тромбофилии являются умеренными факторами риска этих неблагоприятных акушерских явлений. Соответственно, возможно, что антикоагулянтная терапия может снизить риск нежелательных акушерских явлений у пациентов с тромбофилиями.Однако это не было доказано соответствующими клиническими испытаниями. Хотя несколько ретроспективных исследований и одно РКИ показали, что НМГ были полезны у пациентов с тромбофилиями и неблагоприятными акушерскими исходами, другие не показали положительного эффекта. Таким образом, лечение следует считать экспериментальным.
Послеродовая антикоагулянтная терапия
Послеродовая антикоагулянтная терапия обычно начинается через 6–12 часов после кесарева сечения или через 6 часов после удаления катетера из эпидурального пространства.Дозировка тромбопрофилактики или полного антикоагулянта теперь может быть такой же, как и у небеременных людей. У пациентов, которым не требуется пожизненная антикоагулянтная терапия, тромбопрофилактику следует продолжать в течение 6 недель после родов. Этого можно добиться с помощью нефракционированного гепарина, НМГ или варфарина. Все они считаются безопасными для кормящих женщин.
Пациентам, которым требуется пожизненная антикоагулянтная или полная антикоагулянтная терапия в течение более шести недель после родов, варфарин можно начинать после родов, обычно в начальной дозе 5 мг в день (если не известна доза до беременности).Цель — 2,0–3,0 INR. НМГ или нефракционированный гепарин следует начинать и продолжать до тех пор, пока МНО не станет терапевтическим в течение двух дней.
Антикоагулянтная терапия во время родов
У пациентов с относительно низким риском тромбоза целесообразно прекратить антикоагулянтную терапию во время родов и родоразрешения. Сюда входят пациенты с тромбофилиями и отдаленными тромбозами. Во время родов они должны носить пневматические компрессионные устройства. Разумно предложить индукцию родов подходящим кандидатам на сроке беременности 39-40 недель, чтобы иметь возможность контролировать антикоагулянтную терапию.
Тромбопрофилактические дозы НМГ и нефракционированного гепарина можно прекратить за 12 часов до необходимости нейроаксиальной анальгезии или анестезии. В качестве альтернативы пациенту следует рекомендовать прекратить прием антикоагулянтов при спонтанном разрыве плодных оболочек или начале родов. Анестезиологи разрешат нейроаксиальную анальгезию в условиях нормальной ЧТВ у пациентов, принимающих нефракционированный гепарин. У тех, кто принимает НМГ, результаты анти-Ха обычно слишком долго не могут быть полезными в родах.Нейроаксиальная анальгезия / анестезия считается безопасной, если прошло 12 часов с момента последней тромбопрофилактической дозы НМГ или 24 часа с момента последней полной дозы антикоагулянта НМГ. В случаях, когда необходимо срочное кесарево сечение, антикоагулянтную терапию можно отменить с помощью сульфата протамина.
У пациентов с чрезвычайно высоким риском ВТЭ, таких как женщины с тромбоэмболой легочной артерии за несколько дней до родов, целесообразно продолжать антикоагулянтную терапию полной дозой во время родов и родоразрешения. Это достигается с помощью непрерывного внутривенного вливания нефракционированного гепарина.Его можно отключить в случае кровотечения или необходимости операции. Нейроаксиальная анестезия противопоказана. Сульфат протамина можно использовать для отмены антикоагулянтных эффектов. Это редкое обстоятельство.
У пациентов с высоким риском ВТЭ, таких как пациенты с множественными предшествующими ВТЭ и тяжелой тромбофилией, другой подход заключается в продолжении низкой дозы тромбопрофилактики нефракционированным гепарином (5000 единиц подкожно [п / к] два раза в день) во время родов. Несмотря на то, что нейроаксиальная анальгезия противопоказана, роды через естественные родовые пути обычно могут быть благополучно выполнены без увеличения риска кровотечения.
Пациентам с дефицитом ATIII может быть полезно лечение концентратом ATIII во время родов или перед кесаревым сечением. Дозирование и мониторинг уровней следует обсудить с гематологом или фармацевтом.
Режим антикоагуляции
Антикоагулянтная терапия во время беременности может осуществляться с помощью низкомолекулярного гепарина (НМГ) или нефракционированного гепарина. В целом, НМГ предпочтительнее нефракционированного гепарина из-за более постоянной биодоступности, меньшего риска гепарин-индуцированной тромбоцитопении, меньшего риска остеопении и меньшей необходимости оценивать уровни антикоагуляции у женщин, принимающих полную антикоагулянтную терапию.Нефракционированный гепарин предпочтительнее НМГ у женщин, у которых возможны спонтанные роды (обычно после 36 недель беременности), поскольку он с меньшей вероятностью будет мешать безопасной нейроаксиальной анальгезии. Кроме того, это может быть дешевле, чем LMWH. НМГ настоятельно рекомендуется женщинам, нуждающимся в полной антикоагулянтной терапии в течение 36 недель беременности.
Существует небольшая значимая разница между НМГ и нефракционированным гепарином у женщин, получающих тромбопрофилактические дозы. В таких случаях целесообразно использовать нефракционированный гепарин, если стоимость / доступ к НМГ является проблемой.
Тромбопрофилактика нефракционированным гепарином у небеременных женщин проводится подкожно по 5000 единиц каждые 12 часов. Большинство авторитетов советуют немного увеличить дозу во время беременности. Из-за увеличения количества прокоагулянтных белков значительный процент женщин не может достичь необходимого уровня антикоагуляции с обычной дозой «небеременных». Простой способ добиться этого — использовать 7500 единиц SC два раза в день (каждые 12 часов). В качестве альтернативы можно использовать 5000-7500 единиц подкожно дважды в день в первом триместре, 7500-10 000 единиц подкожно дважды в день во втором триместре и 10 000 единиц подкожно дважды в день в третьем триместре.
Тромбопрофилактика НМГ у небеременных женщин осуществляется с помощью эноксапарина 40 мг подкожно ежедневно, далтепарина 5000 единиц подкожно ежедневно или тинзапарина 4500 единиц подкожно ежедневно. Некоторые авторитеты советуют немного увеличить дозу во время беременности. Например, 30 мг эноксапарина подкожно дважды в день.
Полная антикоагуляция нефракционированным гепарином осуществляется путем дозирования два раза в день (каждые 12 часов) или трижды в день (каждые 8 часов) для достижения ЧТВ 1,5–2,0 X контроля через 6 часов после инъекции.Некоторые данные подтверждают более надежные уровни в тканях при дозировке трижды в день.
Полная антикоагуляция НМГ осуществляется дозированием в зависимости от веса. Примеры включают эноксапарин 1 мг / кг два раза в день, далтепарин 200 единиц / кг в день, далтепарин 100 единиц / кг два раза в день и тинзапарин 175 единиц / кг в день. Некоторые специалисты рекомендуют оценивать уровни антикоагулянтов из-за измененной фармакокинетики беременности. Целью у пациентов, принимающих эноксапарин, является уровень анти-Ха 0,6–1,0 единиц / мл через 6 часов после приема препарата.
Показания к дородовой антикоагулянтной терапии
Пациентам с острой ВТЭ следует пройти полную антикоагулянтную терапию НМГ или нефракционированным гепарином в течение 3–6 месяцев после острого события. Это верно независимо от статуса тромбофилии. Большинство авторитетных специалистов обычно рекомендуют полную антикоагулянтную терапию через 6 месяцев после острого события, которое произошло во время беременности. Если до окончания беременности прошло 6 месяцев, в большинстве случаев следует уменьшить дозу антикоагуляции до тромбопрофилактической дозы.Пациенту требуется полная антикоагуляция при множественных тромбозах или статусе тромбофилии, как показано ниже.
Пациенты с двумя или более предшествующими ВТЭ должны пройти полную антикоагуляцию в течение дородового периода, независимо от статуса тромбофилии. В качестве альтернативы допустимо лечить этих женщин тромбопрофилактикой, если они не проходят пожизненную антикоагулянтную терапию (но это редко).
Пациенты с единичным предшествующим тромбозом и «большой» тромбофилией или тромбофилией высокого риска должны пройти полную антикоагулянтную терапию в течение всего дородового периода.Примеры основной тромбофилии включают дефицит ATIII, гомозиготы по лейденской мутации фактора V, гомозиготы по мутации протромбина G20210A и сложные гетерозиготы по лейденской мутации фактора V и мутациям протромбина G20210A. То же самое и с женщинами с антифосфолипидным синдромом, приобретенной тромбофилией, о которой рассказывается в отдельной главе.
Пациенты с «незначительной» тромбофилией или тромбофилией низкого риска, такие как гетерозиготы по лейденской мутации фактора V и мутации протромбина G20210A, дефицит протеина C и протеина S, а также один предшествующий тромбоз, должны пройти тромбопрофилактику в дородовой период.
Спорный вопрос относительно лучшего дородового лечения для пациентов с тромбофилией и отсутствия в личном анамнезе ВТЭ. Большинство авторитетных специалистов рекомендуют дородовую тромбопрофилактику женщинам с тяжелой тромбофилией и без предшествующей ВТЭ. Считается приемлемым либо отсутствие тромбопрофилактики, либо тромбопрофилактика у пациентов с незначительной тромбофилией и без предшествующей ВТЭ. Пациенты с сильным семейным анамнезом ВТЭ имеют более высокий риск ВТЭ, чем женщины без семейного анамнеза ВТЭ.
4.Осложнения
Кровотечение
Кровотечение у пациентов, принимающих тромбопрофилактические дозы гепаринов, встречается крайне редко. Это риск у пациентов, принимающих полные дозы антикоагулянтов. Риски можно свести к минимуму, если быть уверенным в правильности дозирования и в том, что пациент избегает действий, которые могут привести к травматическим повреждениям. Сульфат протамина можно использовать для отмены антикоагулянтного действия гепаринов в экстренных ситуациях.
Раздражение кожи / аллергия
У большинства пациентов в месте инъекции гепарина будут небольшие синяки.В некоторых случаях у пациента наблюдается локализованная кожная аллергическая реакция с воспалением и дискомфортом. В таких случаях разумно перейти с нефракционированного гепарина на НМГ в надежде, что он лучше переносится. В редких случаях необходимо использовать один из альтернативных методов лечения антикоагулянтами, описанных в разделе о ГИТ.
Гепарин-индуцированная остеопения
Это, вероятно, обратимо после прекращения приема нефракционированного гепарина или НМГ. Это хуже с нефракционированным гепарином, чем с НМГ.По-видимому, существует зависимость от дозы: чем выше доза гепарина, тем сильнее остеопения.
Нет необходимости проходить рутинное сканирование DEXA у женщин, принимающих гепарин. Несмотря на недоказанную эффективность, может быть полезно, чтобы женщины, принимающие гепарин, дополнительно принимали кальций и витамин D и выполняли упражнения с опорой на осевой скелет.
Гепарин-индуцированная тромбоцитопения (HIT)
HIT — серьезное осложнение терапии нефракционированным гепарином или НМГ.Это редко (<1%) во время беременности, но МОЖЕТ произойти. Это может привести к опасному для жизни парадоксальному тромбозу.
Все пациенты, принимающие любую дозу нефракционированного гепарина, должны проходить скрининг на ГИТ, как и все пациенты, принимающие полные дозы антикоагулянтов НМГ. Скрининг следует проводить с серийным подсчетом тромбоцитов каждые 1-3 дня, начиная с 4-14 дня терапии. Если количество тромбоцитов уменьшается, HIT можно подтвердить с помощью оценки антител против комплекса гепарин-тромбоцитарный фактор 4 и анализа высвобождения серотонина 14C.
И нефракционированные, и НМГ обладают перекрестной реактивностью. Таким образом, если HIT развивается у одного агента, НЕ БЕЗОПАСНО переключаться на другого. Альтернативные антикоагулянты у пациентов с ГИТ включают фондапаринукс, данапароид, лепирудин, бивалирудин и аргатробан.
ВТЕ
Основным осложнением тромбофилий во время беременности и послеродового периода является ВТЭ.
Риск ВТЭ во время беременности без тромбопрофилактики оценивается в пределах от 1: 200 до 1: 400 у женщин, гетерозиготных по лейденской мутации фактора V и не имеющих личного или семейного анамнеза тромбоза.Риск оценивается в 10% у гетерозигот фактора V Лейдена с личным анамнезом ВТЭ. Риск составляет 1-2% для гомозигот без личного или семейного анамнеза ВТЭ. Риск оценивается в 17% у гомозигот с личным анамнезом ВТЭ.
Риск ВТЭ во время беременности без тромбопрофилактики оценивается ниже 1: 200 у женщин, гетерозиготных по мутации гена протромбина G20210A и не имеющих личного или семейного анамнеза ВТЭ. Риск превышает 10%, если у них в анамнезе есть ВТЭ.Риск гомозигот без личного или семейного анамнеза ВТЭ составляет 2–3%. Риск гомозигот с предшествующей ВТЭ увеличивается.
Риск ВТЭ во время беременности без тромбопрофилактики у сложных гетерозигот (гетерозиготных как по лейденскому фактору V, так и по мутациям гена протромбина G20210A) у женщин без личного или семейного анамнеза ВТЭ составляет 4-5%.
Риск ВТЭ у женщин с дефицитом протеина C во время беременности без тромбопрофилактики и тромбоза в анамнезе или тромбоза в семейном анамнезе составляет 2–7%.Почти всегда семейный анамнез тромбоза в семьях с дефицитом протеина С.
Риск ВТЭ во время беременности без тромбопрофилактики и предшествующего тромбоза или семейного анамнеза ВТЭ у женщин с дефицитом протеина S составляет 6-7%. В семьях с дефицитом протеина S почти всегда имеется семейный анамнез ВТЭ.
Риск ВТЭ у женщин с дефицитом ATIII во время беременности без тромбопрофилактики и предшествующего тромбоза или тромбоза в семейном анамнезе точно не известен, но, по оценкам, увеличивается в 15 раз.В семьях с дефицитом ATIII почти всегда имеется семейный анамнез тромбоза.
5. Прогноз и исход
Следует сообщить пациенту, что у большинства женщин с тромбофилиями исходы беременности превосходны. Действительно, проспективные исследования показывают результаты, аналогичные результатам у женщин без тромбофилий. Некоторые тромбофилии могут быть небольшим фактором риска некоторых неблагоприятных исходов беременности, таких как ожирение, раса и возраст. Однако нет никаких доказательств того, что акушерские или медицинские вмешательства улучшают исходы.
Женщины с предшествующими неблагоприятными исходами беременности и тромбофилиями имеют повышенный риск рецидива неблагоприятных исходов беременности, который основан на их прошлом акушерском анамнезе, а не на их тромбофилическом статусе. Таким образом, женщины, у которых ранее были мертворождения, имеют повышенный риск последующего мертворождения, который не связан с их лабораторными исследованиями на тромбофилии или ВТЭ в анамнезе. Люди с тромбофилиями в течение всей жизни подвергаются повышенному риску ВТЭ. Им следует по возможности избегать ситуаций, повышающих риск ВТЭ.Примером могут служить оральные контрацептивы, содержащие эстроген. (Не рекомендуется обследовать всех женщин на тромбофилии до начала лечения оральными контрацептивами).
Если таких ситуаций невозможно избежать (например, операция на бедре или желаемая беременность), им следует пройти курс тромбопрофилактики. Некоторым женщинам с тромбофилиями требуется пожизненная антикоагулянтная терапия. Всем женщинам с тромбофилиями рекомендуется проконсультироваться с гематологом, чтобы обсудить оптимальную антикоагулянтную терапию небеременным, особенно с учетом большого количества текущих исследований, направленных на прояснение этих вопросов.
6. Каковы доказательства для конкретных рекомендаций по ведению и лечению?
«Практический бюллетень ACOG № 124». Obstet Gynecol. об. 118. 2011. С. 730-40. (Отличный и актуальный обзор, предназначенный для практикующего врача)
Franco, RF, Reitsma, PH. «Генетические факторы риска венозной тромбоэмболии». Hum Genet. об. 109. 2001. С. 369–84. (Хороший обзор тромбофилий)
Робертсон, L, Ву, O, Langhorne, P, Twaddle, S, Clark, P, Lowe, GD.«Тромбофилия при беременности: систематический обзор. Тромбоз: риск и экономическая оценка скринингового исследования на тромбофилию (TREATS) ». Br J Haematol. об. 132. 2006. С. 171–96. (Резюме обследования и лечения беременных)
Дайзон-Таунсон, Д., Миллер, К., Сибай, Б., Спонг, К.Й., Том, Э, Вендель, Г. «Взаимосвязь лейденской мутации фактора V и исходов беременности для матери и плода. Сеть отделений материнско-фетальной медицины Национального института детского здоровья и развития человека ». Obstet Gynecol. об. 106. 2005. С. 517-24. (Проспективное исследование фактора V Лейдена и исходов беременности)
Сильвер, Р.М., Чжао, И, Спонг, С.Й., Сибай, Б., Вендель, Дж., Венстром, К. «Мутация гена протромбина G20210A и акушерские осложнения. Юнис Кеннеди Шрайвер Сеть отделений материнско-фетальной медицины Национального института детского здоровья и человеческого развития ». Obstet Gynecol. об. 115. 2010. С. 14-20. (Проспективное исследование гена протромбина G20210A и исходов беременности)
Роджер, Массачусетс, Пайдас, М., МакЛинток, К., Миддельдорп, С., Кан, С., Мартинелли, И.«Унаследованная тромбофилия и осложнения беременности». Obstet Gynecol. об. 112. 2008. С. 320-4. (Отличное обсуждение взаимосвязи между тромбофилиями и неблагоприятными акушерскими исходами)
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
Повторный визит к скринингу на тромбофилию: вопрос персонализированной медицины
Martinelli I, Bucciarelli P, Mannucci PM (2010) Факторы риска тромбообразования: основы патофизиологии. Crit Care Med 38 (2 приложения): S3 – S9. https://doi.org/10.1097/CCM.0b013e3181c9cbd9
Артикул
PubMed
Google Scholar
Lippi G, Franchini M (2008) Патогенез венозной тромбоэмболии: когда чаша переполняется.Semin Thromb Hemost 34 (8): 747–761. https://doi.org/10.1055/s-0029-1145257
Артикул
PubMed
CAS
Google Scholar
Багот К.Н., Арья Р. (2008) Вирхов и его триада: вопрос атрибуции. Br J Haematol 143 (2): 180–190. https://doi.org/10.1111/j.1365-2141.2008.07323.x
Артикул
PubMed
Google Scholar
Stricker H, Colucci G, Godio M, Mossi G, Mombelli G (2003) Влияние длительного сидячего положения на биохимические маркеры активации коагуляции у здоровых субъектов: свидетельство снижения образования тромбина.J Thromb Haemost 1 (2): 380–381
Артикул
CAS
Google Scholar
Stricker H, Colucci G, Alberio L, Mombelli G (2006) Изменение ингибиторов свертывания крови во время длительного сидения: возможные патогенетические механизмы тромбоза, связанного с путешествием. J Thromb Haemost 4 (4): 900–902. https://doi.org/10.1111/j.1538-7836.2006.01855.x
Артикул
PubMed
CAS
Google Scholar
Colucci G, Stricker H, Roggiani W, Haeberli A, Mombelli G (2004) Венозный застой и образование тромбина. J Thromb Haemost 2 (6): 1008–1009. https://doi.org/10.1111/j.1538-7836.2004.00748.x
Артикул
PubMed
CAS
Google Scholar
Singh S, Houng AK, Reed GL (2019) Фибринолиз, вызванный венозным застоем, предотвращает тромбоз у мышей: роль альфа2-антиплазмина. Кровь 134 (12): 970–978. https://doi.org/10.1182/blood.201
49
Артикул
PubMed
CAS
Google Scholar
Ruhl H, Muller J, Waschenbach J, Oldenburg J, Dewald O, Potzsch B (2014) Кратковременный венозный застой вызывает фибринолитическую активацию, но не образование тромбина. J. Atheroscler Thromb 21 (12): 1260–1270. https://doi.org/10.5551/jat.24216
Артикул
PubMed
Google Scholar
Конвей Е.М. (2015) Реинкарнация древних связей между свертыванием и дополнением.J Thromb Haemost 13 (Дополнение 1): S121 – S132. https://doi.org/10.1111/jth.12950
Артикул
PubMed
CAS
Google Scholar
Oikonomopoulou K, Ricklin D, Ward PA, Lambris JD (2012) Взаимодействие между коагуляцией и комплементом — их роль в воспалении. Семин иммунопатол 34 (1): 151–165. https://doi.org/10.1007/s00281-011-0280-x
Артикул
PubMed
CAS
Google Scholar
Андерсон Ф.А. младший, Уиллер Х. Б., Голдберг Р. Дж., Хосмер Д. В., Патвардхан Н. А., Йованович Б., Форсьер А., Дален Дж. Э. (1991). Популяционная перспектива госпитальной заболеваемости и показателей летальности при тромбозе глубоких вен и тромбоэмболии легочной артерии. Вустерское исследование DVT. Arch Intern Med 151 (5): 933–938
Статья
Google Scholar
Rosendaal FR (1999) Венозный тромбоз: многокомпонентное заболевание. Ланцет 353 (9159): 1167–1173
Артикул
CAS
Google Scholar
Morange PE, Сушон П., Трегуэ Д.А. (2015) Генетика венозного тромбоза: обновление в 2015 году. Thromb Haemost 114 (5): 910–919. https://doi.org/10.1160/Th25-05-0410
Артикул
PubMed
Google Scholar
Cohn DM, Middeldorp S (2008) Раннее завершение многоцентрового рандомизированного клинического исследования для оценки преимуществ тестирования на тромбофилию после первой венозной тромбоэмболии: исследование NOSTRADAMUS. Нед Тейдшр. Geneeskd 152 (38): 2093–2094
PubMed
CAS
Google Scholar
Middeldorp S (2011) Полезно ли тестирование на тромбофилию? Образовательная программа Hematology Am Soc Hematol 2011: 150–155. https://doi.org/10.1182/asheducation-2011.1.150
Артикул
PubMed
Google Scholar
Кон Д.М., Вансенн Ф., де Борджи, Калифорния, Миддельдорп С. (2012) Тестирование на тромбофилию для предотвращения рецидивирующей венозной тромбоэмболии. Кокрановская база данных Syst Rev 12: CD007069. https://doi.org/10.1002/14651858.CD007069.pub3
Артикул
PubMed
Google Scholar
Middeldorp S (2016) Унаследованная тромбофилия: палка о двух концах. Hematology Am Soc Hematol Educ Program 2016 (1): 1–9. https://doi.org/10.1182/asheducation-2016.1.1
Артикул
PubMed
PubMed Central
Google Scholar
Stevens SM, Woller SC, Bauer KA, Kasthuri R, Cushman M, Streiff M, Lim W., Douketis JD (2016) Руководство по оценке и лечению наследственной и приобретенной тромбофилии. J Thromb Thrombolysis 41 (1): 154–164.https://doi.org/10.1007/s11239-015-1316-1
Артикул
PubMed
PubMed Central
CAS
Google Scholar
Pernod G, Biron-Andreani C, Morange PE, Boehlen F, Constans J, Couturaud F, Drouet L, Jude B, Lecompte T, Le Gal G, Trillot N, Wahl D, французская группа на h, thrombosis, Французское общество сосудистых заболеваний (2009 г.). Рекомендации по тестированию на тромбофилию при венозной тромбоэмболической болезни: руководящие принципы французского консенсуса.J Mal Vasc 34 (3): 156–203. https://doi.org/10.1016/j.jmv.2009.02.005
Артикул
PubMed
CAS
Google Scholar
Кеарон С., Акл Э.А., Орнелас Дж., Блайвас А., Хименес Д., Боунамо Х., Хьюисман М., Кинг С.С., Моррис Т.А., Суд Н., Стивенс С.М., Винч Дж.Р., Уэллс П., Воллер С.К., Мурс Л. (2016) Антитромботическая терапия при ВТЭ: руководство CHEST и отчет экспертной группы. Сундук 149 (2): 315–352. https://doi.org/10.1016/j.chest.2015.11,026
Артикул
PubMed
Google Scholar
Egeberg O (1965) Унаследованный дефицит антитромбина, вызывающий тромбофилию. Thromb Diath Haemorrh 13: 516–530
PubMed
CAS
Google Scholar
Griffin JH, Evatt B, Zimmerman TS, Kleiss AJ, Wideman C (1981) Дефицит протеина C при врожденном тромботическом заболевании. J Clin Invest 68 (5): 1370–1373
Статья
CAS
Google Scholar
Comp PC, Esmon CT (1984) Рецидивирующая венозная тромбоэмболия у пациентов с частичным дефицитом белка S. N Engl J Med 311 (24): 1525–1528. https://doi.org/10.1056/NEJM198412133112401
Артикул
PubMed
CAS
Google Scholar
Uitte de Willige S, de Visser MC, Houwing-Duistermaat JJ, Rosendaal FR, Vos HL, Bertina RM (2005) Генетическая изменчивость гамма-гена фибриногена увеличивает риск тромбоза глубоких вен за счет снижения гамма-фибриногена в плазме. уровни.Кровь 106 (13): 4176–4183. https://doi.org/10.1182/blood-2005-05-2180
Артикул
PubMed
CAS
Google Scholar
den Heijer M, Koster T, Blom HJ, Bos GM, Briet E, Reitsma PH, Vandenbroucke JP, Rosendaal FR (1996) Гипергомоцистеинемия как фактор риска тромбоза глубоких вен. N Engl J Med 334 (12): 759–762. https://doi.org/10.1056/NEJM199603213341203
Артикул
Google Scholar
Poort SR, Rosendaal FR, Reitsma PH, Bertina RM (1996) Общая генетическая вариация в 3′-нетранслируемой области гена протромбина связана с повышенными уровнями протромбина в плазме и увеличением венозного тромбоза. Кровь 88 (10): 3698–3703
Статья
CAS
Google Scholar
Bertina RM, Koeleman BP, Koster T., Rosendaal FR, Dirven RJ, de Ronde H, van der Velden PA, Reitsma PH (1994) Мутация фактора свертывания крови V, связанная с устойчивостью к активированному протеину C.Nature 369 (6475): 64–67. https://doi.org/10.1038/369064a0
Артикул
PubMed
CAS
Google Scholar
Morange PE, Tregouet DA (2013) Текущие знания о генетике случаев венозного тромбоза. J Thromb Haemost 11 (Приложение 1): 111–121. https://doi.org/10.1111/jth.12233
Артикул
PubMed
Google Scholar
Tirado I, Mateo J, Soria JM, Oliver A, Martinez-Sanchez E, Vallve C, Borrell M, Urrutia T, Fontcuberta J (2005) Генотип группы крови ABO и уровни фактора VIII как независимые факторы риска при венозной тромбоэмболии.Thromb Haemost 93 (3): 468–474. https://doi.org/10.1160/TH04-04-0251
Артикул
PubMed
CAS
Google Scholar
Procare GG (2006) Группа крови ABO, но не генетические полиморфизмы гемостаза, значительно влияют на риск тромбоза: исследование 180 гомозигот по лейденской мутации фактора V. Br J Haematol 135 (5): 697–702. https://doi.org/10.1111/j.1365-2141.2006.06353.x
Артикул
CAS
Google Scholar
Dentali F, Sironi AP, Ageno W, Turato S, Bonfanti C, Frattini F, Crestani S, Franchini M (2012) Группа крови, отличная от O, является наиболее распространенным генетическим фактором риска ВТЭ: результаты метаанализа литературы . Semin Thromb Hemost 38 (5): 535–548. https://doi.org/10.1055/s-0032-1315758
Артикул
PubMed
Google Scholar
Germain M, Chasman DI, de Haan H, Tang W, Lindstrom S, Weng LC, de Andrade M, de Visser MC, Wiggins KL, Suson P, Saut N, Smadja DM, Le Gal G, van Hylckama VA, Di Narzo A, Hao K, Nelson CP, Rocanin-Arjo A, Folkersen L, Monajemi R, Rose LM, Brody JA, Slagboom E, Aissi D, Gagnon F, Deleuze JF, Deloukas P, Tzourio C, Dartigues JF , Berr C, Taylor KD, Civelek M, Eriksson P, Cardiogenics C, Psaty BM, Houwing-Duitermaat J, Goodall AH, Cambien F, Kraft P, Amouyel P, Samani NJ, Basu S, Ridker PM, Rosendaal FR, Kabrhel C , Folsom AR, Heit J, Reitsma PH, Tregouet DA, Smith NL, Morange PE (2015) Мета-анализ 65 734 человек идентифицирует TSPAN15 и SLC44A2 как два локуса восприимчивости к венозной тромбоэмболии.Am J Hum Genet 96 (4): 532–542. https://doi.org/10.1016/j.ajhg.2015.01.019
Артикул
PubMed
PubMed Central
CAS
Google Scholar
Tregouet DA, Morange PE (2018) Что в настоящее время известно о генетике венозной тромбоэмболии на заре технологий секвенирования следующего поколения. Br J Haematol 180 (3): 335–345. https://doi.org/10.1111/bjh.15004
Артикул
PubMed
Google Scholar
Даунс К., Меги К., Дуарте Д., Фрис М., Гебхарт Дж., Хофер С., Шамардина О., Деви СВВ, Стивенс Дж., Мапета Р., Тунец С., Аль-Хассо Н., Бессер М. В., Купер Н., Догерти Л., Глидалл Н., Грин Д., Хаймел М., Мартин Х., Пападиа С., Ревель-Вилк С., Сивапаларатнам С., Саймингтон Е., Томас В., Тис С., Толиос А., Пенкетт С. Дж., Биоресурс N, Оувеханд WH, Аббс С., Лаффан М. А., Турро Е., Симеони I, Мамфорд AD, Henskens YMC, Pabinger I, Gomez K, Freson K (2019) Диагностическое высокопроизводительное секвенирование 2396 пациентов с кровотечениями, тромботическими и тромбоцитарными нарушениями.Кровь 134 (23): 2082–2091. https://doi.org/10.1182/blood.20188
Артикул
PubMed
PubMed Central
CAS
Google Scholar
Rees DC, Cox M, Clegg JB (1995) Мировое распределение фактора V Лейден. Ланцет 346 (8983): 1133–1134. https://doi.org/10.1016/s0140-6736(95)
Артикул
PubMed
CAS
Google Scholar
Rosendaal FR, Doggen CJ, Zivelin A, Arruda VR, Aiach M, Siscovick DS, Hillarp A, Watzke HH, Bernardi F, Cumming AM, Preston FE, Reitsma PH (1998) Географическое распределение 20210 G к варианту протромбина.Thromb Haemost 79 (4): 706–708
Артикул
CAS
Google Scholar
Андерсон Ф.А. младший, Спенсер Ф.А. (2003) Факторы риска венозной тромбоэмболии. Тираж 107 (23 Дополнение 1): I9 – I16. https://doi.org/10.1161/01.CIR.0000078469.07362.E6
Артикул
PubMed
Google Scholar
Vossen CY, Walker ID, Svensson P, Souto JC, Scharrer I, Preston FE, Palareti G, Pabinger I, van der Meer FJ, Makris M, Fontcuberta J, Conard J, Rosendaal FR (2005) Повторение частота после первого венозного тромбоза у пациентов с семейной тромбофилией.Артериосклер Thromb Vasc Biol 25 (9): 1992–1997. https://doi.org/10.1161/01.ATV.0000174806.76629.7b
Артикул
PubMed
CAS
Google Scholar
Kenet G, Nowak-Gottl U (2012) Венозная тромбоэмболия у новорожденных и детей. Передовая практика, Res Clin Haematol 25 (3): 333–344. https://doi.org/10.1016/j.beha.2012.07.001
Артикул
PubMed
Google Scholar
Паркер Р.И. (2010) Тромбоз в педиатрической популяции. Crit Care Med 38 (2 приложения): S71 – S75. https://doi.org/10.1097/CCM.0b013e3181c9cce9
Артикул
PubMed
Google Scholar
Young G, Albisetti M, Bonduel M, Brandao L, Chan A, Friedrichs F, Goldenberg NA, Grabowski E, Heller C, Journeycake J, Kenet G, Krumpel A, Kurnik K, Lubetsky A, Male C , Manco-Johnson M, Mathew P, Monagle P, van Ommen H, Simioni P, Svirin P, Tormene D, Nowak-Gottl U (2008) Влияние наследственной тромбофилии на венозную тромбоэмболию у детей: систематический обзор и метаанализ наблюдательные исследования.Тираж 118 (13): 1373–1382. https://doi.org/10.1161/CIRCULATIONAHA.108.789008
Артикул
PubMed
Google Scholar
Holzhauer S, Goldenberg NA, Junker R, Heller C, Stoll M, Manner D, Mesters R, Krumpel A, Stach M, Nowak-Gottl U (2012) Унаследованная тромбофилия у детей с венозной тромбоэмболией и семейной риск тромбоэмболии: обсервационное исследование. Кровь 120 (7): 1510–1515. https://doi.org/10.1182/blood-2012-01-405514
Артикул
PubMed
PubMed Central
CAS
Google Scholar
Nowak-Gottl U, van Ommen H, Kenet G (2018) Тестирование на тромбофилию у детей: что и когда следует тестировать? Thromb Res 164: 75–78. https://doi.org/10.1016/j.thromres.2018.02.136
Артикул
PubMed
CAS
Google Scholar
Варга Е.А., Куйович Ю.Л. (2012) Ведение наследственной тромбофилии: руководство для генетиков. Clin Genet 81 (1): 7–17. https://doi.org/10.1111/j.1399-0004.2011.01746.x
Артикул
PubMed
CAS
Google Scholar
Goldberg RJ, Seneff M, Gore JM, Anderson FA, Jr, Greene HL, Wheeler HB, Dalen JE (1987) Оккультное злокачественное новообразование у пациентов с тромбозом глубоких вен. Arch Intern Med 147 (2): 251–253
Статья
CAS
Google Scholar
Prandoni P, Lensing AW, Buller HR, Cogo A, Prins MH, Cattelan AM, Cuppini S, Noventa F, ten Cate JW (1992) Тромбоз глубоких вен и частота последующего симптоматического рака. N Engl J Med 327 (16): 1128–1133
Статья
CAS
Google Scholar
Delluc A, Antic D, Lecumberri R, Ay C, Meyer G, Carrier M (2017) Скрининг скрытого рака у пациентов с венозной тромбоэмболией: руководство SSC ISTH. J Thromb Haemost 15 (10): 2076–2079. https://doi.org/10.1111/jth.13791
Артикул
PubMed
CAS
Google Scholar
Carrier M, Lazo-Langner A, Shivakumar S, Tagalakis V, Zarychanski R, Solymoss S, Routhier N, Douketis J, Danovitch K, Lee AY, Le Gal G, Wells PS, Corsi DJ, Ramsay T. , Coyle D, Chagnon I, Kassam Z, Tao H, Rodger MA, Investigators S (2015) Скрининг оккультного рака при неспровоцированной венозной тромбоэмболии.N Engl J Med 373 (8): 697–704. https://doi.org/10.1056/NEJMoa15606623
Артикул
PubMed
CAS
Google Scholar
Colucci G, Tsakiris DA (2017) Скрининг на тромбофилию: универсальный, выборочный или ни один? Clin Appl Thromb Hemost 23 (8): 893–899. https://doi.org/10.1177/1076029616683803
Артикул
PubMed
Google Scholar
Ocal IT, Sadeghi A, Press RD (1997) Риск венозного тромбоза у носителей общей мутации регуляторного фермента гомоцистеина метилентетрагидрофолатредуктазы.Мол диагностика 2 (1): 61–68. https://doi.org/10.1054/MODI00200061
Артикул
PubMed
CAS
Google Scholar
Симоне Б., Де Стефано В., Леонсини Е., Зачо Дж., Мартинелли И., Эммерих Дж., Росси Е., Фолсом А.Р., Альмави В.Й., Скарабин П.Й., ден Хейер М., Кушман М., Пенко С., Вая А., Angchaisuksiri P, Okumus G, Gemmati D, Cima S, Akar N, Oguzulgen KI, Ducros V, Lichy C, Fernandez-Miranda C, Szczeklik A, Nieto JA, Torres JD, Le Cam-Duchez V, Ivanov P, Cantu-Brito C, Шмелева В.М., Стегнар М., Огунеми Д., Эйд С.С., Николотти Н., Де Фео Э, Риккарди В., Бочча С. (2013) Риск венозной тромбоэмболии, связанный с одиночным и комбинированным действием фактора V Лейдена, протромбина 20210A и метилентетрайдрофолат редуктазы C677T : метаанализ с участием более 11 000 случаев и 21 000 контрольных точек.Eur J Epidemiol 28 (8): 621–647. https://doi.org/10.1007/s10654-013-9825-8
Артикул
PubMed
PubMed Central
CAS
Google Scholar
Connors JM (2017) Тестирование на тромбофилию и венозный тромбоз. N Engl J Med 377 (12): 1177–1187. https://doi.org/10.1056/NEJMra1700365
Артикул
PubMed
Google Scholar
Simpson EL, Стивенсон MD, Rawdin A, Papaioannou D (2009) Тестирование на тромбофилию у людей с венозной тромбоэмболией: систематический обзор и анализ экономической эффективности.Оценка медицинских технологий 13 (2): 1–91. https://doi.org/10.3310/hta13020
Артикул
Google Scholar
Wu O, Robertson L, Twaddle S, Lowe G, Clark P, Walker I, Brenkel I, Greaves M, Langhorne P, Regan L, Greer I, Thrombosis R, Economic Assessment of Thrombophilia Screening S (2005) ) Скрининг на тромбофилию в ситуациях высокого риска: метаанализ и анализ экономической эффективности. Br J Haematol 131 (1): 80–90. https: // doi.org / 10.1111 / j.1365-2141.2005.05715.x
Артикул
PubMed
Google Scholar
Wu O, Robertson L, Twaddle S, Lowe GD, Clark P, Greaves M, Walker ID, Langhorne P, Brenkel I, Regan L, Greer I (2006) Скрининг на тромбофилию в ситуациях высокого риска: систематический обзор и анализ экономической эффективности. Тромбоз: риск и экономическая оценка исследования скрининга на тромбофилию (TREATS). Оценка медицинских технологий 10 (11): 1–110.https://doi.org/10.3310/hta10110
Артикул
PubMed
CAS
Google Scholar
Creinin MD, Lisman R, Strickler RC (1999) Скрининг лейденской мутации фактора V перед назначением комбинированных оральных контрацептивов. Fertil Steril 72 (4): 646–651. https://doi.org/10.1016/s0015-0282(99)00318-0
Артикул
PubMed
CAS
Google Scholar
Favaloro EJ (2014) Бесполезность тестирования на тромбофилию.Clin Chem Lab Med 52 (4): 499–503. https://doi.org/10.1515/cclm-2013-0560
Артикул
PubMed
CAS
Google Scholar
Ормешер Л., Simcox LE, Tower C, Greer IA (2017) «Тестировать или не тестировать», аргументы за и против тестирования на тромбофилию в акушерстве. Акушерская медицина 10 (2): 61–66. https://doi.org/10.1177/1753495X17695696
Артикул
PubMed
PubMed Central
Google Scholar
Croles FN, Nasserinejad K, Duvekot JJ, Kruip MJ, Meijer K, Leebeek FW (2017) Беременность, тромбофилия и риск первого венозного тромбоза: систематический обзор и байесовский метаанализ. BMJ 359: j4452. https://doi.org/10.1136/bmj.j4452
Артикул
PubMed
PubMed Central
Google Scholar
Джованни Л., Мария Л.Г., Мауро Р., Карлотта М., Федерика Р., Фабрицио П., Шеба Дж., Джузеппе Д.П., Алессандро Б., Элио С., Герберт В. (2011) Тромбофилия и повреждение почек во время беременности.J Prenat Med 5 (4): 78–82
PubMed
PubMed Central
Google Scholar
Tektonidou MG, Andreoli L, Limper M, Amoura Z, Cervera R, Costedoat-Chalumeau N, Cuadrado MJ, Dorner T, Ferrer-Oliveras R, Hambly K, Khamashta MA, King J, Marchiori F, Meroni PL, Mosca M, Pengo V, Raio L, Ruiz-Irastorza G, Shoenfeld Y, Stojanovich L, Svenungsson E, Wahl D, Tincani A, Ward MM (2019) Рекомендации EULAR по управлению антифосфолипидным синдромом у взрослых.Энн Рум Дис 78 (10): 1296–1304. https://doi.org/10.1136/annrheumdis-2019-215213
Артикул
PubMed
CAS
Google Scholar
Tripodi A (2012) Проблемы и решения для тестирования тестов гемостаза, когда пациенты принимают антикоагулянты. Semin Thromb Hemost 38 (6): 586–592. https://doi.org/10.1055/s-0032-1319769
Артикул
PubMed
CAS
Google Scholar
Ortel TL (2010) Факторы риска тромботических заболеваний в отделениях интенсивной терапии. Crit Care Med 38 (2 приложения): S43 – S50. https://doi.org/10.1097/CCM.0b013e3181c9ccc8
Артикул
PubMed
Google Scholar
Kearon C (2004) Долгосрочное ведение пациентов после венозной тромбоэмболии. Тираж 110 (9 приложение 1): I10 – I18. https://doi.org/10.1161/01.CIR.0000140902.46296.ae
Артикул
PubMed
CAS
Google Scholar
Prandoni P, Noventa F, Ghirarduzzi A, Pengo V, Bernardi E, Pesavento R, Iotti M, Tormene D, Simioni P, Pagnan A (2007) Риск рецидива венозной тромбоэмболии после прекращения антикоагуляции у пациентов с острым проксимальным тромбозом глубоких вен или легочная эмболия. Проспективное когортное исследование с участием 1626 пациентов. Haematologica 92 (2): 199–205. https://doi.org/10.3324/haematol.10516
Артикул
PubMed
Google Scholar
Baglin T, Luddington R, Brown K, Baglin C (2003) Частота рецидивов венозной тромбоэмболии в связи с клиническими и тромбофильными факторами риска: проспективное когортное исследование. Ланцет 362 (9383): 523–526. https://doi.org/10.1016/S0140-6736(03)14111-6
Артикул
PubMed
Google Scholar
White RH (2003) Эпидемиология венозной тромбоэмболии. Тираж 107 (23 Приложение 1): I4 – I8. https://doi.org/10.1161/01.CIR.0000078468.11849.66
Артикул
PubMed
Google Scholar
McRae S, Tran H, Schulman S, Ginsberg J, Kearon C (2006) Влияние пола пациента на риск рецидива венозной тромбоэмболии: метаанализ. Ланцет 368 (9533): 371–378. https://doi.org/10.1016/S0140-6736(06)69110-1
Артикул
PubMed
Google Scholar
Heit JA, Mohr DN, Silverstein MD, Petterson TM, O’Fallon WM, Melton LJ 3rd (2000) Предикторы рецидива после тромбоза глубоких вен и тромбоэмболии легочной артерии: популяционное когортное исследование.Arch Intern Med 160 (6): 761–768. https://doi.org/10.1001/archinte.160.6.761
Артикул
PubMed
CAS
Google Scholar
Galli M, Luciani D, Bertolini G, Barbui T (2003) Волчаночные антикоагулянты являются более сильными факторами риска тромбоза, чем антикардиолипиновые антитела при антифосфолипидном синдроме: систематический обзор литературы. Кровь 101 (5): 1827–1832. https://doi.org/10.1182/blood-2002-02-0441
Артикул
PubMed
CAS
Google Scholar
De Stefano V, Simioni P, Rossi E, Tormene D, Za T., Pagnan A, Leone G (2006) Риск рецидивирующей венозной тромбоэмболии у пациентов с наследственной недостаточностью природных антикоагулянтов, антитромбина, протеина C и протеина S. Haematologica 91 ( 5): 695–698
PubMed
Google Scholar
Segal JB, Brotman DJ, Necochea AJ, Emadi A, Samal L, Wilson LM, Crim MT, Bass EB (2009) Прогностическое значение фактора V Лейдена и протромбина G20210A у взрослых с венозной тромбоэмболией и у членов семьи тех, у кого есть мутация: систематический обзор.JAMA 301 (23): 2472–2485. https://doi.org/10.1001/jama.2009.853
Артикул
PubMed
CAS
Google Scholar
De Stefano V, Martinelli I, Mannucci PM, Paciaroni K, Chiusolo P, Casorelli I, Rossi E, Leone G (1999) Риск повторного тромбоза глубоких вен среди гетерозиготных носителей как фактора V Лейдена, так и Мутация протромбина G20210A. N Engl J Med 341 (11): 801–806. https://doi.org/10.1056/NEJM199
Артикул
PubMed
Google Scholar
Palareti G, Cosmi B, Legnani C, Tosetto A, Brusi C, Iorio A, Pengo V, Ghirarduzzi A, Pattacini C, Testa S, Lensing AW, Tripodi A, Investigators P (2006) Тестирование D-димера для определения продолжительности антикоагулянтной терапии. N Engl J Med 355 (17): 1780–1789. https://doi.org/10.1056/NEJMoa054444
Артикул
PubMed
CAS
Google Scholar
Cosmi B, Legnani C, Tosetto A, Pengo V, Ghirarduzzi A, Testa S, Prisco D, Poli D, Tripodi A, Marongiu F, Palareti G, Investigators P (2010) Полезность повторяющегося D-димера тестирование после прекращения антикоагуляции при первом эпизоде неспровоцированной венозной тромбоэмболии: проспективное исследование PROLONG II.Кровь 115 (3): 481–488. https://doi.org/10.1182/blood-2009-08-237354
Артикул
PubMed
CAS
Google Scholar
Palareti G, Legnani C, Antonucci E, Cosmi B, Poli D, Testa S, Tosetto A, Ageno W, Falanga A, Ferrini PM, Pengo V, Prandoni P, Investigators D (2019) D-димер Для оценки индивидуального риска рецидива венозной тромбоэмболии у пациентов обоих полов не пожилого возраста: апостериорный анализ исследования DULCIS.Intern Emerg Med. https://doi.org/10.1007/s11739-019-02216-y
Артикул
PubMed
Google Scholar
Kyrle PA, Minar E, Hirschl M, Bialonczyk C, Stain M, Schneider B, Weltermann A, Speiser W, Lechner K, Eichinger S (2000) Высокие уровни фактора VIII в плазме и риск рецидива венозного тромбоэмболия. N Engl J Med 343 (7): 457–462. https://doi.org/10.1056/NEJM200008173430702
Артикул
PubMed
CAS
Google Scholar
Ensor J, Riley RD, Moore D, Snell KI, Bayliss S, Fitzmaurice D (2016) Систематический обзор прогностических моделей рецидивирующей венозной тромбоэмболии (ВТЭ) после лечения первой неспровоцированной ВТЭ. BMJ Open 6 (5): e011190. https://doi.org/10.1136/bmjopen-2016-011190
Артикул
PubMed
PubMed Central
Google Scholar
Franco Moreno AI, Garcia Navarro MJ, Ortiz Sanchez J, Martin Diaz RM, Madronal Cerezo E, de Ancos Aracil CL, Cabello Clotet N, Perales Fraile I, Gimeno Garcia S, Montero Hernandez C, Zapatero Gaviria A , Ruiz Giardin JM (2016) Оценка риска для прогнозирования рецидива у пациентов с неспровоцированной венозной тромбоэмболией (DAMOVES).Eur J Intern Med 29: 59–64. https://doi.org/10.1016/j.ejim.2015.12.010
Артикул
PubMed
CAS
Google Scholar
Bahl V, Hu HM, Henke PK, Wakefield TW, Campbell DA Jr, Caprini JA (2010) Проверочное исследование ретроспективного метода оценки риска венозной тромбоэмболии. Энн Сург 251 (2): 344–350. https://doi.org/10.1097/SLA.0b013e3181b7fca6
Артикул
Google Scholar
Larciprete G, Gioia S, Angelucci PA, Brosio F, Barbati G, Angelucci GP, Frigo MG, Baiocco F, Romanini ME, Arduini D, Cirese E (2007) Единичные наследственные тромбофилии и неблагоприятные исходы беременности. Журнал J Obstet Gynaecol Res 33 (4): 423–430. https://doi.org/10.1111/j.1447-0756.2007.00550.x
Артикул
PubMed
CAS
Google Scholar
Тернбулл С., Скотт Р. Х., Томас Е., Джонс Л., Муругэсу Н., Претти Ф. Б., Халаи Д., Бапл Е., Крейг С., Хамблин А., Хендерсон С., Патч С, О’Нил А., Деверо А. Смит К., Мартин А. Р., Сосинский А., МакДонах Е. М., Султана Р., Мюллер М., Смедли Д., Томс А., Дин Л., Фаулер Т., Бейл М., Хаббард Т., Рендон А., Хилл С., Колфилд М. Дж., Геномы П (2018) Проект «100 000 геномов»: доведение секвенирования всего генома до NHS.BMJ 361: k1687. https://doi.org/10.1136/bmj.k1687
Артикул
PubMed
Google Scholar
Crous-Bou M, Harrington LB, Kabrhel C (2016) Экологические и генетические факторы риска, связанные с венозной тромбоэмболией. Semin Thromb Hemost 42 (8): 808–820. https://doi.org/10.1055/s-0036-1592333
Артикул
PubMed
PubMed Central
Google Scholar
Crous-Bou M, De Vivo I, Camargo CA Jr, Varraso R, Grodstein F, Jensen MK, Kraft P, Goldhaber SZ, Lindstrom S, Kabrhel C (2016) Взаимодействие установленных факторов риска и оценки генетического риска на основе GWAS о риске венозной тромбоэмболии. Thromb Haemost 116 (4): 705–713. https://doi.org/10.1160/Th26-02-0172
Артикул
PubMed
PubMed Central
Google Scholar
Состояния гиперкоагуляции — AMBOSS
Последнее обновление: 29 марта 2021 г.
Сводка
Состояние гиперкоагуляции, т.е.е., тромбофилия, характеризуется повышенной предрасположенностью к образованию тромбов. В зависимости от этиологии могут быть задействованы один или несколько факторов из триады Вирхова (застой, гиперкоагуляция, повреждение эндотелия). Гиперкоагуляция может быть приобретенной или унаследованной и может влиять на вены и / или артерии. Наиболее частыми проявлениями являются рецидивирующие тромбозы глубоких вен нижних конечностей и тромбоэмболия легочной артерии. Поражение артерий увеличивает риск инфаркта миокарда, инсульта и самопроизвольного аборта.Оценка гиперкоагуляции включает оценку потенциальных факторов риска (например, иммобилизация, курение, использование оральных контрацептивов и злокачественность) и лабораторные тесты для оценки аномалий каскада свертывания крови (например, фактор V Лейден, синдром антифосфолипидных антител). Лечение основано на основном состоянии и обычно включает снижение факторов риска и / или прием антикоагулянтов.
Этиология
Этиология тромбофилии можно разделить на две категории:
Клинические признаки
Тромбофилия характеризуется рецидивирующей тромбоэмболией.
- Венозная тромбоэмболия (наиболее частая)
- Артериальная тромбоэмболия
Наследственная тромбофилия
| Патофизиология наследственной тромбофилии [1] [2] [3] | В общей популяции |
Устойчивость к активированному протеину C (APC-R) Фактор V Лейден |
|---|---|---|
| Повышенный уровень фактора VIII | ||
| Дефицит протеина C | ||
| Дефицит антитромбина III | ||
|
Гипермия |
∼ 5–7% |
|
Приобретенная тромбофилия
Диагностика
- История
- Лабораторные испытания
- Визуализация: при подозрении на злокачественное новообразование рассмотрите возможность компьютерной томографии
Лечение
Подход
Особые соображения
Риск венозной тромбоэмболии снижается с помощью антикоагулянта (например,g., гепарин) после операции!
Каталожные номера: [7]
Профилактика
Рассмотрите возможность профилактики в следующих группах высокого риска:
- Послеоперационные пациенты
- Длительная иммобилизация или госпитализация
- Злокачественные новообразования
- Ортопедические состояния
Ссылки
-
Colman RW. Гемостаз и тромбоз: основные принципы и клиническая практика .
Липпинкотт Уильямс и Уилкинс
; 2006 г. -
Ден Бур, Северная Каролина, Ван дер Хайден С., Лейнсе Б., Суверейн Дж. Х.М. Клиническая химия: обзор
.
Пленум Пресс
; 1989 г. -
Кумар А., Африн С., Мохд Юсуф, Гупта А. Механизм и патофизиология активированного протеина С-связанного фактора V лейдена при венозном тромбозе. Азиатский журнал науки о переливании крови . 2012; 6
(1): с.47.
DOI: 10.4103 / 0973-6247.95053. | Открыть в режиме чтения QxMD -
Ким Дж.Й., Хаванин Н., Рамбачан А. и др. Длительность операции и риск венозной тромбоэмболии. JAMA Surg . 2015; 150
(2): с.110-117.
DOI: 10.1001 / jamasurg.2014.1841. | Открыть в режиме чтения QxMD -
Блохин ИО, Ленц СР. Механизмы тромбоза при ожирении. Curr Opin Hematol . 2015; 20
(5): с.437-444.
DOI: 10,1097 / MOH.0b013e3283634443. | Открыть в режиме чтения QxMD -
Эсмон CT. Основные механизмы и патогенез венозного тромбоза. Кровь Ред. . 2009; 23
(5): стр.225–229.
DOI: 10.1016 / j.blre.2009.07.002. | Открыть в режиме чтения QxMD -
Чайковский С.Н., Розинг Дж. Механизмы эстроген-индуцированной венозной тромбоэмболии. Тромб Res . 2010; 126
(1): стр. 5-11.
DOI: 10.1016 / j.thromres.


