Скрытый железодефицит: как с ним бороться? | 161.ru
Железодефицитное состояние – это самая распространенная патология. По некоторым данным, дефицит железа есть более чем у 1,5 млрд жителей нашей планеты. Сама по себе железодефицитная анемия не является заболеванием, но она может стать симптомом серьезной патологии.
Недостаток железа и развивающаяся вслед за ним тканевая и гемическая гипоксия приводят к значительным трофическим изменениям волос, их истончению, усиленному выпадению и даже раннему поседению. Наряду с этим появляется ломкость ногтей, их поперечная исчерченность, зазубренность ногтевого края, искривление ногтевой пластинки, уплощение или вогнутость ногтей вплоть до ложкообразных. Иногда железодефицит приводит к атрофии слизистой оболочки языка, ангулярному стоматиту, глосситу, кариесу зубов, мышечной слабости, болям в спине. Проявлением дефицита железа может стать даже повышение температуры до субфебрильных цифр.
Болит все
Чтобы понять, почему так происходит, вспомним, что железодефицитную анемию отличает пониженное содержание в крови гемоглобина, являющегося транспортом для кислорода. Человек с низким содержанием гемоглобина может дышать чистейшим воздухом в сосновом бору, но кислород в необходимом количестве не будет попадать в клетки, потому что недостаточно транспорта – гемоглобина. В свою очередь кислород – это окислитель, благодаря которому совершаются обменные процессы. Если его мало, то в них накапливаются недоокисленные продукты обмена, по существу – яд, отравляющий организм и нарушающий его функционирование.
Человек с низким содержанием гемоглобина может дышать чистейшим воздухом в сосновом бору, но кислород в необходимом количестве не будет попадать в клетки, потому что недостаточно транспорта – гемоглобина. В свою очередь кислород – это окислитель, благодаря которому совершаются обменные процессы. Если его мало, то в них накапливаются недоокисленные продукты обмена, по существу – яд, отравляющий организм и нарушающий его функционирование.
Отсюда и слабость, и вялость, как при отравлении, и повышенная мышечная утомляемость. А если учесть, что к гипоксии наиболее чувствительна нервная ткань, то находит объяснение и странная на первый взгляд жалоба больных на то, что «болит все».
Пациенты идут к неврологу, гастроэнтерологу или кардиологу, у них отмечаются расстройства сердечно-сосудистой системы, миокардиодистрофии, возникают вегетососудистые и вестибулярные нарушения. Люди страдают от частых простуд и ОРЗ, проблем со стороны пищеварительной системы и почек. Они лечатся, выполняют назначения специалистов, но обнаруживают, что ожидаемого выздоровления и улучшения качества жизни нет, или они кратковременны. И все это только потому, что не выявлена главная причина – железодефицитное состояние. В таких случаях помочь может только терапевт, который должен провести все необходимые исследования и выявить истинные причины недомогания.
И все это только потому, что не выявлена главная причина – железодефицитное состояние. В таких случаях помочь может только терапевт, который должен провести все необходимые исследования и выявить истинные причины недомогания.
Скрытая угроза
Железодефицитная анемия: причины, профилактика и лечение
Хроническую усталость, бледность кожи и головокружение можно связать с переутомлением. Однако безобидные на первый взгляд симптомы могут оказаться сигналом серьёзных неполадок в организме. По данным Всемирной организации здравоохранения с железодефицитной анемией (далее – ЖДА) сталкивается порядка 20 % женщин во всём мире. Важно знать, что среди населения широко распространен латентный (скрытый) дефицит железа, частота которого колеблется от 20 до 30%.
Суточная потребность в железе у мужчин составляет 10 мг, у женщин – 15 мг (20–25 мг для беременных и кормящих), а для детей – 5-15 мг в зависимости от возраста.
О железодефицитной анемии говорит низкий уровень гемоглобина, а вот латентное состояние – это когда уровень гемоглобина еще нормальный, а запасы железа в организме уже истощены.
Различают три стадии железодефицитного состояния в организме:
1. Предлатентный дефицит железа — скрытый дефицит железа, когда организм аккумулирует железо при помощи ферритина — железосодержащего белка. Если показатель ферритина в биохимическом анализе крови низкий, это говорит о предлатентном дефиците железа.
2. Латентный дефицит железа — на данной стадии, наряду с ферритином, истощаются тканевые запасы железа при оптимальных показателях гемоглобина, не наблюдается клинических симптомов дефицита железа, в кишечнике происходит компенсаторное повышение всасывания железа, активность железосодержащих ферментов постепенно снижается.
3. Явный дефицит железа характеризуется уменьшением числа эритроцитов и снижением уровня гемоглобина, который входит в состав эритроцитов и представляет собой вещество, транспортирующее кислород к тканям организма из легких, развитием дистрофических изменений в органах и тканях, а также повышенным количеством протопорфирина в эритроцитах.
От концентрации железа в крови зависят окислительно-восстановительные процессы, снабжение клеток кислородом. Несмотря на то, что столкнуться с проблемой железодефицитной анемии могут лица разного пола и возраста, анемию считают «женской» патологией, точнее болезнью женщин в возрасте 15–45 лет.
Порядка 50 до 86% женщин в различных популяциях имеют факторы риска развития анемии. Причина тому — патологические менструации (длительные или обильные), беременность и лактация. Во время беременности расходование железа резко повышается на потребности плода и плаценты, кровопотерю при родах и лактацию. Баланс железа в этот период находится на грани дефицита, и различные факторы, уменьшающие поступление или увеличивающие расход железа, могут приводить к развитию ЖДА.
Причины развития анемии
ЖДА нередко развивается при желудочно-кишечных (геморрой, язвенная болезнь) и маточных (миома матки) кровотечениях или связана с хроническими заболеваниями: воспалением поджелудочной железы или двенадцатиперстной кишки, бронхитом, болезнью почек. Нарушение усвоения этого микроэлемента — ещё одна причина, по которой он не используется организмом по назначению. В этом случае спровоцировать проблему может, например, хронический гастрит.
Нарушение усвоения этого микроэлемента — ещё одна причина, по которой он не используется организмом по назначению. В этом случае спровоцировать проблему может, например, хронический гастрит.
Растительные или кисломолочные диеты также способствуют развитию анемии. Дело в том, что железо лучше усваивается из пищи животного происхождения — мяса, рыбы, морепродуктов, а молочная пища богата кальцием, который препятствует всасыванию железа.
Сухая кожа, трещины в уголках рта (ангулярный стоматит), ломкие волосы и ногти, одышка, головокружение, снижение работоспособности, а также желание попробовать мел и глубоко вдохнуть запах свежей краски или бензина — симптомы, указывающие на нехватку железа в организме. Однако этих симптомов недостаточно для постановки диагноза. Для подтверждения ЖДА нужно сдать общий и биохимический анализы крови. Гемоглобин отвечает за циркуляцию кислорода в крови. В случае железодефицита его уровень обычно снижен — менее 115–120 г/л (у женщин). При этом на ранних стадиях болезни гемоглобин может быть в норме. Не допустить ошибки в постановке диагноза позволяет лабораторное определение уровня сывороточного железа, а также трансферина и ферритина — белков, ответственных за перенос железа к органам и тканям и создание запаса микроэлемента в организме. Эти показатели являются маркерами анемии на начальном этапе и их низкий уровень свидетельствует о проблеме.
При этом на ранних стадиях болезни гемоглобин может быть в норме. Не допустить ошибки в постановке диагноза позволяет лабораторное определение уровня сывороточного железа, а также трансферина и ферритина — белков, ответственных за перенос железа к органам и тканям и создание запаса микроэлемента в организме. Эти показатели являются маркерами анемии на начальном этапе и их низкий уровень свидетельствует о проблеме.
Чтобы выяснить причину заболевания, потребуется пройти дополнительное обследование — в первую очередь проверить работу желудочно-кишечного тракта (при помощи гастроскопии, рентгенографии желудка, колоноскопии) и органы репродуктивной системы.
Эксперты сходятся во мнении: сбалансированное питание, включающее продукты с высоким содержанием железа, — лучшая профилактика железодефицита. Среди рекордсменов по количеству ценного микроэлемента — мясо (говядина, баранина), рыба и морепродукты, гречка, кунжут, тыквенные семечки и яблоки. Следует помнить, что железо не может нормально усваиваться при дефиците витамина С и фолиевой кислоты. Всасыванию железа также препятствуют полифенолы и фитаты, содержащиеся в чае, кофе, цельнозерновых и молочных продуктах. Важно учитывать и тот факт, что чем дольше продукт подвергался термической обработке, тем меньше железа в нём осталось. Согласно последним данным, биодоступность железа из обычного рациона взрослого человека составляет не более 10%, а в развивающихся странах данный показатель ниже 5%.
Всасыванию железа также препятствуют полифенолы и фитаты, содержащиеся в чае, кофе, цельнозерновых и молочных продуктах. Важно учитывать и тот факт, что чем дольше продукт подвергался термической обработке, тем меньше железа в нём осталось. Согласно последним данным, биодоступность железа из обычного рациона взрослого человека составляет не более 10%, а в развивающихся странах данный показатель ниже 5%.
Поэтому, если железодефицитнаяя анемия уже возникла, то справиться с ней при помощи одной диеты невозможно. Для профилактики ЖДА женщинам фертильного возраста врачи также рекомендуют не только правильно питаться, но и дополнительно принимать лекарственные препараты, содержащие железо.
Лечение железодефицитной анемии дело, хоть и несложное, но достаточно длительное. Принцип лечения предельно прост: ликвидация причины вызвавшей дефицит железа и прием препаратов железа. Основная ошибка, встречающаяся в практике – назначение препарата железа на короткий срок. Даже незначительный дефицит железа восполняется не менее двух месяцев. При выраженном дефиците железа лечение может длиться шесть месяцев и более. В подавляющем большинстве случаев препараты железа назначаются в форме препаратов для приема внутрь (капсулах или таблетках).
Даже незначительный дефицит железа восполняется не менее двух месяцев. При выраженном дефиците железа лечение может длиться шесть месяцев и более. В подавляющем большинстве случаев препараты железа назначаются в форме препаратов для приема внутрь (капсулах или таблетках).
Лекарственное средство ФЕРРОФОЛ в капсулах – комбинированное противоанемическое средство на основе железа в комбинации с фолиевой кислотой.
В составе Феррофола: элементарного железа – 50,00 мг (в виде железа II сульфата), кислоты фолиевой – 0,50 мг.
Важные преимущества Феррофола:
Кому рекомендуем и как принимать Феррофол?
Взрослые старше 18 лет принимают Феррофол до или во время приема пищи. Капсулы нужно глотать целиком.
Капсулы нужно глотать целиком.
При легкой железодефицитной анемии и скрытом (латентном) дефиците железа с дефицитом фолиевой кислоты или для профилактики дефицита железа и дефицита фолиевой кислоты: 1 капсула в день.
При тяжелом дефиците железа и фолиевой кислоты (не у беременных):1 капсула 2-3 раза в день.
Во время беременности для профилактики и устранения дефицита железа и дефицита фолиевой кислоты: максимальная доза 2 капсулы в день.
Феррофол относится к препаратам двухвалентного железа, обладает хорошей биодоступностью, способен значительно поднять уровень гемоглобина уже через 2–4 недели после начала приема.
Необходимо помнить, что многие продукты питания и лекарственные средства (например, антациды) ухудшают всасывание железа. Учитывая это, Феррофол необходимо принимать за один час до еды или через два часа после еды. Если вы принимаете другие лекарственные препараты, то интервал между ними должен составить не менее двух часов до или четырех часов после приема. Запивать Феррофол следует водой, можно запивать яблочным или апельсиновым соком.
Запивать Феррофол следует водой, можно запивать яблочным или апельсиновым соком.
Основные побочные эффекты при приеме препаратов железа связаны с желудочно-кишечным трактом: запоры, диарея, тошноты, металлический вкус во рту. Если при приеме Феррофола наблюдаются подобные побочные эффекты, не нужно прекращать прием препаратов, а следует проконсультироваться с врачом, вероятно, вам будет рекомендовано уменьшить дозу препарата для однократного приема, что позволит избежать негативных эффектов. Важно знать, что препараты железа могут окрашивать стул в черный цвет, это не является признаком желудочно-кишечного кровотечения, а нормальная реакция кишечного содержимого на взаимодействие с железом.
Препараты солей железа принимаются под контролем врача. Доза и продолжительность лечения индивидуальны, зависят от степени дефицита железа и фолиевой кислоты.
ПЕРЕД ПРИМЕНЕНИЕМ ЛЕКАРСТВЕННОГО СРЕДСТВА ОЗНАКОМЬТЕСЬ С ИНСТРУКЦИЕЙ. Имеются медицинские противопоказания и побочные действия.
Имеются медицинские противопоказания и побочные действия.
Железодефицитная анемия:Причины,Симптомы,Лечение | doc.ua
Причины
- Избыток железа в организме откладывается в депо, которым служит костный мозг, печень, селезенка. Если его поступает с пищей недостаточно, это может быть причиной обеднения запасов железа и развитием анемии у взрослого и ребенка. Плод накапливает железо на всех сроках беременности, особенно, в последний триместр (40%), что является важным фактором развития болезни у недоношенных. Развивается анемия железодефицитная на фоне фетоплацентарной недостаточности, многоплодной беременности.
- Организм нуждается в железе больше, чем в обычных условиях. Особая потребность в железе развивается в пубертатный период, у девочек с появлением менструаций, у беременных, кормящих матерей. При респираторно-вирусных заболеваниях отмечается повышенный расход железа.
- Недостаточное всасывание железа в кишечнике человека. В двенадцатиперстной кишке с помощью ферментов всасывается наибольшая часть железа.
 Лучше всего железо усваивается из телятины, печени, куриного мяса, значительно меньше из яиц, и растительных продуктов. Фитаты и фосфаты тормозят абсорбцию железа.
Лучше всего железо усваивается из телятины, печени, куриного мяса, значительно меньше из яиц, и растительных продуктов. Фитаты и фосфаты тормозят абсорбцию железа. - Потери железа организмом, превышающие его необходимое поступление.
Встречается железодефицитная анемия, причины которой трудно установить, а иногда и после дополнительного обследования причина остается невыясненной.
Классификация
Степень тяжести:
- Легкая: гемоглобин 90-110 г/л; эритроциты 3,0-3,5 х 1012 /л;
- Средняя: гемоглобин 70-90 г/л; эритроциты 2,5-3,0 х 1012 /л;
- Тяжелая: гемоглобин менее 70 г/л; эритроциты менее 2,5 х 1012 /л.
Симптомы
Суточная потребность в железе -8-10 мг.
Признаки железодефицитной анемии бывают скрытыми (скрытый дефицит) и явными. Если есть скрытый дефицит железа симптомы, характерные для анемии не так выражены, единичные и отмечаются не всегда. Нормальные цифры гемоглобина в крови не настораживают, и только пониженный уровень сывороточного железа помогает выявить это состояние.
Железодефицитная анемия, симптомы которой выражены, имеет при этом пониженный уровень гемоглобина в крови. Все симптомы, встречающиеся при данном заболевании, развиваются на фоне гипоксии тканей. Можно выделить следующие синдромы:
- эпителиальный – кожа бледная, сухая, дистрофические изменения ногтей;
- астеноневротический синдром – тахикардия, приглушенность тонов сердца, функциональный систолический шум;
- сердечно-сосудистый синдром — раздражительность, снижение аппетита, извращение вкуса, утомляемость;
- гепатолиенальный – увеличение печени, селезенки;
- иммунодефицит.
По частоте встречаемости симптомов на первом месте – бледность, затем по мере убывания — частые респираторные заболевания, раздражительность, извращение вкуса.
Железодефицитная анемия у детей проявляется вышеописанными симптомами. На первом месте также бледность кожи, частые респираторные заболевания, нарушения поведения и аппетита. Наибольшая вероятность развития анемии у недоношенных детей.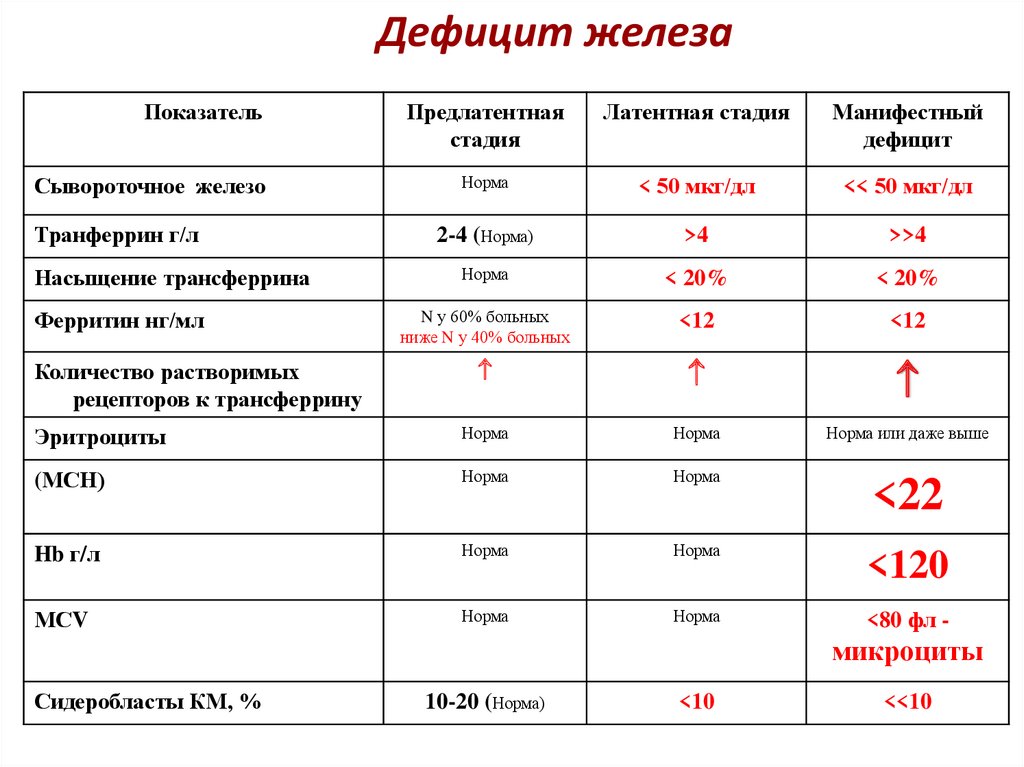 Дети, вскармливаемые искусственно коровьим молоком, также имеют высокие шансы развития анемии.
Дети, вскармливаемые искусственно коровьим молоком, также имеют высокие шансы развития анемии.
У детей можно выделить следующие особенности. На первом году жизни железодефицитная анемия, признаки которой подтверждены лабораторными данными, может быть вариантом нормы, что обусловлено особенностями кроветворения в этом возрасте. Снижение показателей в этом случае возникает в возрасте 3 месяцев и в 6 месячном возрасте.
Для того, чтобы оценить состояние ребенка надо интерпретировать анализ крови с учетом изменяющихся (и не один раз) возрастных показателей.
Диагностика
Диагноз железодефицитной анемии основывается, прежде всего, на результатах анализов крови. Снижение гемоглобина, эритроцитов — признаки анемии. Для анемии характерно выявление гипохромии, анизоцитоза. Увеличение показателя ретикулоцитов свидетельствует об активном кроветворении в костном мозге.
Диагноз подтверждается, если сывороточное железо менее 12 мкмоль/л, общая железосвязывающая способность сыворотки выше 64 мкмоль/л.
Для выявления причины анемии больной осматривается гинекологом, терапевтом, при необходимости хирургом, онкологом, гематологом. Проводятся дополнительные исследования для обнаружения болезни, ставшей причиной анемии – УЗИ, МРТ, РЭГ.
Лечение
Если удается выяснить причину анемии, ее надо устранить.
Лечение железодефицитной анемии проводится с применением медикаментозных средств, при выявлении любой ее степени. Предпочтение отдается препаратам трехвалентного железа. Наиболее популярны феррум-лек, мальтофер. Хорошо переносится и дает высокий лечебный эффект сорбифер, ферроплекс, актиферрин.
Препараты железа могут быть в форме таблеток, сиропа и ампул для внутривенного введения.
В коплексе с препаратами железа принимают поливитамины, содержащие аскорбиновую и фолиевую кислоту.
Переливание крови как метод лечения сейчас не применяется. При необходимости могут внутривенно переливать компоненты крови (эритроцитарную массу).
Железодефицитная анемия, лечение которой проводится без медикаментозных средств, длительно сопровождается своими симптомами, так как получить железо в достаточном количестве извне, не прибегая к помощи лекарств невозможно.
Биологическая доступность железа из пищи невелика. Несмотря на это в питание необходимо включать продукты, богатые железом, из которых оно наиболее полно усваивается (говядина, телятина, печень, рыба, яичный желток). Детям мясной прикорм вводится с 6 месяцев.
Пациенты с железодефицитной анемией находятся под диспансерным наблюдением, что позволяет врачу следить за их состоянием и вносить необходимые коррективы в лечение и обследование. Лечение проводится в течение нескольких месяцев, о его эффективности судят по нормализации показателей в анализах крови.
Железо и железодефицитная анемия | Shanti Food
Чуть ли не каждая вторая моя клиентка имеет жалобы на что-то из следующего: недостаток энергии, раздражительность, перепады настроения, слабость и головокружения, снижение концентрации внимания и памяти, низкий иммунитет и многие другие неспецифические симптомы. Причины могут быть различными, но часто дело в скрытом железодефиците. Уверена, эта тема актуальна для многих, поэтому я и решила написать для вас эту статью.
Уверена, эта тема актуальна для многих, поэтому я и решила написать для вас эту статью.
Скрытый железодефицит — это очень распространенное состояние, особенно если речь идет о женщинах детородного возраста, обильно менструирующих, и женщинах после родов. У мужчин железодефицит бывает реже, но тоже встречается.
Для начала, рассмотрим сам элемент железа — зачем он нам нужен и какие функции выполняет.
Функции железа в организме
В нашем организме в норме содержится около 4,5 г железа. Железо входит в состав гемоглобина и миоглобина. Основная функция: перенос кислорода из лёгких в органы и ткани, включая кожу. Железо участвует в процессе дыхания, состоит в порядка 100 различных ферментов и поэтому опосредованно влияет на реакции окисления, иммунный ответ, энергетический баланс, холестериновый обмен, синтез ДНК и др.
Железо в нашем организме может быть:
- В клетках (внутриклеточное) — например, в составе гемоглобина, миоглобина, и т.
 д.
д. - Вне клеток (внеклеточное) — железо сыворотки, участвует в транспорте железа (например, трасферрин)
- Запасное — например, всем известный ферритин
Почему нам так часто не хватает железа?
Из пищи мы получаем около 10-20 мг железа, но усвоение крайне низкое — около 10-20 % (у годовалых детей лучше — до 70 %, к 10 годам усвоение падает до примерно тех же значений, что у взрослых). При этом, мы тратим его довольно-таки много — порядка 2 мг у женщин и 0,6 мг у мужчин. Основные потери: с кровью (в т.ч. менструальной), потом, калом, слущенным эпидермисом. Кормящие женщины теряют железо с молоком. Таким образом, чтобы возместить запасы с учетом низкой всасываемости, нам нужно съедать достаточно много продуктов, его содержащих.
Источники железа: мясо животных, субпродукты, птица, рыба, хлеб и крупы, орехи, зелень, сухофрукты. Но важно понимать, что железо — железу рознь. Различают гемовое железо (в животных продуктах), которое, как видно из статистики ниже, усваивается лучше, и железо в растительных продуктах, которое усваивается гораздо хуже.
Так, железо из мясных продуктов усваивается на 20-30 %, из яиц и рыбы – на 10-15 %, из растительных источников – на 1-5 %. Поэтому такие распространенные попытки поднять железо с помощью яблок (0,1 мг Fe на 100 г) и гречки (2 мг Fe на 100 г) , если у Вас диагностировали железодефицитную анемию, — вариант с нулевой эффективностью.
Хорошая новость: железо неплохо накапливается в организме (если этому процессу не мешать). Наличие в пище фитиновой кислоты (сухие завтраки, растительные продукты), кофеина и танина (кофе, чай, другие кофеинсодержащие напитки), фосфатов (яйца, молоко, сыр), оксалатов (растительные продукты) ухудшает всасывание железа, т. к. образуются нерастворимые комплексы. Также мешают усвоению кальций, алкоголь, болезни ЖКТ, глисты, инфекции, гипоацидность (низкая кислотность желудка).
Что помогает усвоению:
- сокращение кофеина
- замачивание зерновых и бобовых
- витамин В12
- фолиевая кислота (В9)
- витамин С
- медь
- марганец
Показатели уровня железа в крови
С пищевыми продуктами и усвоением разобрались. Теперь предлагаю поговорить о диагностике железодефицита и научиться, наконец, разбираться во всех этих многочисленных лабораторных показателях.
Теперь предлагаю поговорить о диагностике железодефицита и научиться, наконец, разбираться во всех этих многочисленных лабораторных показателях.
Гемоглобин:
Существует представление: если гемоглобин в норме, то и с уровнем железа все ОК. Увы, но все несколько сложнее, да и нормы по гемоглобину — понятия в наших лабораториях очень растяжимые.
Гемоглобин — это железосодержащий белок в эритроцитах, который переносит в ткани кислород. Молекула гемоглобина может нести до 4 молекул кислорода. В легких кислорода много, там он соединяется с гемоглобином, который затем переносит его в другие ткани, где кислорода мало, и где он высвобождается и вступает в окислительные процессы. Освобожденный от кислорода гемоглобин забирает с собой водород и углекислый газ обратно в легкие.
Количество гемоглобина растет при повышении содержания эритроцитов. Низкий гемоглобин — признак анемии, однако, по нему одному невозможно судить о ее причинах. Свободный (вне эритроцитов) гемоглобин токсичен для организма (возникает тканевая гипоксия).
Сывороточное железо:
Это второй анализ, по которому часто пытаются исключить анемию и железодефицит. Железо сыворотки — это внеклеточное железо, которое очень непостоянно и меняется в течение дня. Именно поэтому рассматривать этот показатель отдельно от других анализов не стоит.
Трансферрин:
Трансферрин — это белок плазмы крови, который осуществляет перенос железа. С трансферрином связано около 0,1% всех ионов железа (порядка 4 мг), одна молекула переносит сразу два иона трёх-валентного железа. Трансферрин производится в основном в печени, а также в мозге и некоторых других тканях. Главная роль трансферрина — доставка железа из центра поглощения в двенадцатиперстной кишке и переваривания эритроцитов макрофагами ко всем тканям. Особенно важна его роль при активном делении клеток (например, при кроветворении).
Трансферрин участвует в обеспечении врожденного иммунитета (в слизистых защищает от бактерий). Концентрация трансферрина снижается при воспалении, нефротическом синдроме, циррозе печени, гемохроматозе и др. Часто железодефицитная анемия сопровождается повышением уровня трансферрина — это компенсаторный ответ организма на снижение количества железа, за счет которого увеличенное количество трансферрина связывается с низким количеством Fe в сыворотке крови. В норме же всего 1/3 железосвязывающих центров будет заполнена.
Часто железодефицитная анемия сопровождается повышением уровня трансферрина — это компенсаторный ответ организма на снижение количества железа, за счет которого увеличенное количество трансферрина связывается с низким количеством Fe в сыворотке крови. В норме же всего 1/3 железосвязывающих центров будет заполнена.
Ферритин:
Это железопротеид (комплекс белка + Fe), основная роль которого — хранение запаса железа внутри клеток. Одна молекула ферритина может содержать до 4000 атомов железа! Содержится почти во всех органах и тканях (макрофагах печени, селезенке, костном мозге, эритроцитах, даже в митохондриях) и является донором железа клеткам, которые в нем нуждаются.
Свободные атомы железа токсичны для организма, а благодаря ферритину, они находятся в растворенной и нетоксичной форме. В случае нехватки железа (кровопотеря, дефицит железа в пище) организм начинает добывать железо из клеток, вследствие чего уровень ферритина снижается. Если ситуация с нехваткой поступления железа затягивается, запасы истощаются.
Таким образом, по уровню ферритина можно судить о железодефиците задолго до симптомов полноценной анемии. Вслед за сниженным ферритином, рано или поздно снизится и гемоглобин, но надо понимать, что гемоглобин будет снижаться последним, т.к. организм сделает всё, чтобы защитить его как жизненно-важный элемент. Однако, высокий ферритин (>150 нг/мл) может являться признаком воспаления. Также, при заболеваниях печени, алкоголизме, приеме контрацептивов уровень ферритина не будет показательным для исключения железодефицита.
Общая
железосвязывающая способность сыворотки (ОЖСС):
Данный показатель помогает определит т.н. «Fe-голодание» сыворотки (степень нехватки железа в сыворотке) и говорит о том, сколько железа может в принципе переносить транферрин, косвенно говоря и о количестве самого трансферрина. При определении ОЖСС в исследуемую сыворотку добавляют определённое количество железа. Часть добавленного Fe связывается в сыворотке с белками-переносчиками, а железо, которое не связалось с белками, удаляют из сыворотки и определяют его количество. При железодефицитных анемиях сыворотка связывает больше железа, чем в норме, о чем и будет свидетельствовать увеличение ОЖСС (хотя показатель также вариабелен).
При железодефицитных анемиях сыворотка связывает больше железа, чем в норме, о чем и будет свидетельствовать увеличение ОЖСС (хотя показатель также вариабелен).
Латентная
железосвязывающая способность сыворотки (ЛЖСС):
Это показатель, отражающий потенциальную способность сыворотки крови к связыванию дополнительного количества железа (т.е., оставшиеся 2/3 центров в трансферрине). При нехватке железа ЛЖСС будет расти, при избытке, соответственно, падать.
Стадии железодефицита
Прелатентный железодефицит: депо железа истощается.
В анализах мы увидим: ферритин снижен, остальные показатели пока в норме. Клиника (жалобы) может отсутствовать.
Латентный железодефицит: активность тканевых ферментов снижается.
Симптомы: извращение вкуса, тяга к острой, соленой, пряной пище, мышечная слабость, дистрофические изменения кожи и придатков и др.
Анализы: низкий ферритин + снижение запасов Fe в сыворотке и в белках-переносчиках (трансферрин, гемоглобин), снижение насыщения трансферрина железом (<20%).
Железодефицитная анемия: бывает скрытая (обычно начальная) и явная (более поздняя стадия). При скрытой (латентной) железодефицитной анемии клиника включает: общую слабость, недомогание, снижение работоспособности (+ может быть всё то, что свойственно латентному железодефициту), а также сухость и пощипывания языка, нарушения глотания с ощущением инородного тела в горле (синдром Пламмера-Винсона), сердцебиение, одышку, сонливость, трудности с концентрацией внимания, головные боли переутомления, головокружения.
Симптомы железодефицитной анемии
При железодефицитной анемии ухудшается состояние кожи, волос и ногтей, может возникнуть жжение и зуд вульвы. Может быть красный и сглаженный язык, атрофия вкусовых сосочков, «заеды» в углах рта. Кожа бледная, иногда с зеленоватым оттенком, с легко возникающим румянцем щек, сухая, дряблая, шелушащаяся, порой с трещинами. Ногти тонкие, плоские и матовые, имеют исчерченность, легко расслаиваются, ломаются. Волосы сухие и ломкие, без блеска, сереют, редеют и седеют (раньше срока). Также часто наблюдается снижение иммунитета.
Волосы сухие и ломкие, без блеска, сереют, редеют и седеют (раньше срока). Также часто наблюдается снижение иммунитета.
В анализах будет: снижение гемоглобина и эритроцитов, изменение морфологии эритроцитов (уменьшенный размер эритроцитов, снижение гемоглобина в эритроците и пр.), низкий ферритин и сывороточное железо, повышенный ОЖСС и уменьшение насыщения трансферрина железом.
Для постановки четкого диагноза лучше обратиться к специалисту, т.к. нужна дополнительная дифференциальная диагностика с другими видами гипохромных анемий (например, железоперераспределительной или железонасыщенной анемией).
Причины низкого железа и железодефицитной анемии
- Кровопотери. У женщин детородного возраста на первом месте — обильные менструации. Также, сюда можно отнести любые иные кровопотери (например, операции, травмы, роды), а также хронические кровотечения в ЖКТ (особенно актуально для мужчин, у которых, в принципе, железодефицитная анемия бывает редко), при геморрое и др.

- Высокая потребность в железе. К этой категории можно отнести детей и беременных и кормящих женщин. Практически все мои рожавшие клиентки имеют как минимум низкий ферритин. Кроме того, при активных занятиях спортом, когда происходит набор мышечной массы, потребность в железе также будет выше, чем у средне-статистического человека.
- Низкое содержание железа в рационе питания — например, на гипокалорийных диетах (однако, редко только это может служить причиной), либо его плохое усвоение в ЖКТ (а вот это гораздо чаще).
С третьим пунктом предлагаю разобраться чуть подробнее, т.к. обычно именно из-за этого бывает так сложно накопить или удержать запасы железа в организме.
Почему железо не усваивается (самые частые варианты):
- Низкая кислотность желудочного сока (гипоацидность), либо какие-либо патологические процессы в желудке
- Сниженная ферментативная активность ЖКТ
- Нехватка ко-факторов (белок, витамины В9, В12, С, цинк, медь, марганец)
- Употребление продуктов, богатых железом, или препаратов железа вместе с пищей, содержащей много его конкурентов (например, кальций) или веществ, препятствующих его всасыванию (танинов, фитиновой кислоты, оксалатов, фосфатов и др.
 — всё, что мы обсуждали выше)
— всё, что мы обсуждали выше) - Кандидоз. Кандида очень любит полакомиться не только халявным сахаром, но и железом (и многим другим, не менее важным). Сюда же можно отнести наличие паразитов (глисты).
Частые вопросы и проблемы при коррекции нехватки железа
Итак,
что сдавать, чтобы узнать свой уровень железа (и убедиться, что оно оптимально
усваивается):
- В первую очередь, ферритин: он покажет РЕАЛЬНЫЕ запасы железа в организме. Норма: 50-100 нг/мл (ниже 50 — повод сделать более глубокую диагностику, ниже 30 — очень похоже на железодефицитную анемию (но нужно смотреть в комплексе с другими показателями, а за диагнозом обратиться к врачу), а выше 150 — повод начать искать воспаление, с учетом соответствующей «клиники»).
Если ферритин в анализах низкий, имеет смысл определить, насколько сильно это уже проявляется в организме, и есть ли железодефицитная анемия.
Поэтому можно сдать:
2. ОАК (общий или клинический анализ крови): он покажет, есть ли анемия, на которую укажут:
ОАК (общий или клинический анализ крови): он покажет, есть ли анемия, на которую укажут:
- Низкий гемоглобин (у женщин ниже 135 нг/мл, у мужчин — ниже 140 нг/мл = мкг/л).
- Снижение уровня эритроцитов, их среднего объема, повышение тромбоцитов
3. Сывороточное железо (оптимально 20-25 мкмоль/л)
4. Трансферрин, ОЖСС и ЛЖСС — их повышение также будет говорить о железодефицитной анемии
Если Вы давно не проверяли свои запасы железа и при этом у Вас есть определенные подозрения, что Вам его не хватает, я рекомендую сдавать сразу все 4 пункта. Так Вы (или специалист, которому Вы покажете результаты анализов) сразу получите более полную картину.
Если по клиническим симптомам и анализам у Вас выявлена нехватка железа, либо железодефицитная анемия, то нужно не просто начинать пить препараты железа, а искать причину нехватки. Потому что можно сколько угодно долго пить препараты железа, а усваиваться и запасаться оно не будет!
Поэтому,
при выраженной клинике и плохих результатах в ОАК, имеет смысл дополнительно
оценить количество общего белка (хорошо, если он от 75 до 78 г/л) и запасы
витамина В9 (фолиевая кислота) и В12 (оба — оптимально — по верхней границе
референса), т. к. нехватка этих веществ также может приводить к анемии (не
к. нехватка этих веществ также может приводить к анемии (не
только железодефицитной). Иногда стоит оценить и кислотность желудочного сока
(при низком рН железо плохо усваивается).
Как часто проверять железо и ферритин?
С моей точки зрения, раз в год будет оптимально, если в принципе у Вас с железом все ОК. Если же Вы принимаете препараты железа, то контроль лучше согласовать со специалистом, который Вас ведет.
Обычно препарат пьется не менее 3 месяцев. Каждый месяц-полтора, после небольшого периода отмены (5-7 дней), сдается контрольный анализ (как правило, ферритин + ОАК), чтобы оценить, хорошо ли усваивается данный препарат (т.к. они все разные, и состояние ЖКТ у всех разное). Общая длительность курса приема препарата Fe зависит и от препарата (насколько он сильный), и от стадии дефицита, и от кишечника конкретного человека, и от кофакторов, участвующих в процессе усвоения железа (например, того же витамина С или белка).
Как
рассчитать дозировку препарата железа?
Дозировка рассчитывается индивидуально и зависит от стадии дефицита железа и состояния человека. Если диагностирована железодефицитная анемия, то необходима лечебная дозировка, которую нужно согласовать с Вашим врачом. Если до анемии пока не дошло, можно пробовать поднимать уровень железа профилактическими дозировками с помощью БАД. Также, не забываем про устранение причин железодефицита и ко-факторы усвоения железа!
Если диагностирована железодефицитная анемия, то необходима лечебная дозировка, которую нужно согласовать с Вашим врачом. Если до анемии пока не дошло, можно пробовать поднимать уровень железа профилактическими дозировками с помощью БАД. Также, не забываем про устранение причин железодефицита и ко-факторы усвоения железа!
Как улучшить работу ЖКТ, чтобы железо хорошо усваивалось и накапливалось?
Самостоятельно оценить работу своего ЖКТ не всегда удается, лучше всего обратиться за консультацией к врачу или диетологу-нутрициологу. Для восстановления функции ЖКТ и особенно — кишечника, в котором происходит максимальное всасывание и усвоение питательных веществ, оптимально подходит программа 4R — комплексное восстановление работы кишечника и нормализации работы ЖКТ. Подробнее о программе Вы можете почитать здесь.
Что стоит учесть, если необходимо поднимать уровень железа
Важные
моменты:
- Накопление ферритина в депо — это история не на 1 месяц ( — в случае с таблетками, с внутривенным приемом — быстрее, но это чисто стационарная история!). Сроки, как всегда, индивидуальны, но обычно это от 3 до 6 месяцев, или даже больше.
- Наша цель — не только повышение гемоглобина до нормы, а оптимальный запас ферритина (цифра должна быть хотя бы равна вашему весу).
- Не сдавать анализы во время месячных (кровопотери исказят результат).
- Также, рекомендуется выдержать 5-7 дней без препарата железа, если сдаете повторно во время коррекции.
- Стоит максимально разносить по времени (минимум 3-4 часа) прием моно-препаратов Fe и моно-препараты кальция, магния, ИПП, антибиотики, гормоны, чтобы они не мешали друг другу.
- Не все препараты могут хорошо переноситься. Во-первых, из-за дозы (чем выше, тем больше риск побочных эффектов типа тошноты и пр.), во-вторых, из-за формы. Так, сульфат железа переносится хуже, чем хелатные формы. В некоторых случаях потребуется внутривенное восполнение, это только в стационаре и под присмотром врачей, никакой самодеятельности!
- Во время приема препарата железа могут обостряться хронические проблемы ЖКТ — обязательно сообщите об этом врачу/специалисту, с которым работаете, чтобы изменить тактику.
- Оптимизируйте усвоение препарата железа (не смешивайте его с молоком, кофеин-содержащими напитками и т.д.).
P.S.: Если Вам нужна индивидуальная консультация, подробнее — здесь.
Понравилась статья? Буду благодарна, если поделитесь ей в соц. сетях со своими друзьями.
Чтобы ничего не пропустить, присоединяйтесь к моим группам в Инстаграм, Facebook и ВКонтакте, а также подписывайтесь на рассылку новостей блога (в правом столбце).
Дефицит железа в организме — чем грозит железодефицитная анемия, симптомы и способы восполнения
Организм человека содержит в среднем всего 4 грамма железа. Но даже небольшая его нехватка влияет на работу мозга и внутренних органов. Сегодня разберёмся, как распознать железодефицит и как с ним справиться.
Ключевая функция железа в организме — синтез гемоглобина. Этот белок отвечает за транспортировку кислорода через кровь к тканям и обеспечивает нормальную работу органов. Железо во многом определяет состояние кожи, костей, мышц и сухожилий.
Как проявляется железодефицит?
Выделяют три стадии железодефицита. На первой запас вещества практически иссякает, но концентрация железа в крови остаётся нормальной. На второй стадии проявляются внешние изменения:
- Появляется ощущение постоянной слабости.
- Кожа становится бледнее и суше.
- Ногти становятся вогнутыми и ломкими.
- Треугольник под носом и ладони становятся желтоватыми: из-за нехватки железа проявляется нарушение обмена каротина.
- Появляется нездоровая синева под глазами.
- Волосы становятся ломкими, секущимися, начинают выпадать.
- Изменяются вкусовые ощущения: появляется желание есть мел, сухие крупы, глину, нюхать жидкости с сильным запахом.
- Страдает слизистая дыхательных путей и пищевода. Снижается кислотность желудочного сока, появляется гастрит.
Третья стадия — синдром железодефицитной анемии. К вышеперечисленным симптомам добавляются обмороки, ослабевает иммунитет, человек чаще и дольше болеет.
Как бороться с дефицитом железа?
В организм железо поступает с пищей. Его ежедневная норма разнится в зависимости от возраста и общего состояния организма: от 1 мг/л у детей до 5 мг/л у беременных женщин.
Продукты, содержащие большие дозы витамина C, усиливают усваиваемость железа. Оно в больших количествах содержится в мясе, печени, овсяной крупе, гранате. Важно: молоко не только содержит мало железа, но и затрудняет его всасываемость.
Впрочем, серьёзный дефицит железа невозможно исправить исключительно изменением рациона. Медики доказали, что организм человека не может получить больше 2,5 мг железа в сутки из пищи. На этот факт стоит обратить внимание беременным женщинам, среди которых почти все к концу срока беременности страдают скрытым дефицитом железа. В таком случае помогут только препараты.
Железосодержащие таблетки или сиропы усвоятся в разы лучше. Но даже в таком случае результаты лечения проявятся приблизительно через месяц. При незначительном железодефиците измените рацион и добавьте в него гематоген.
Социальный проект, приуроченный ко Всемирному дню борьбы с дефицитом железа
#тынежелезная – новый социальный проект, приуроченный ко Всемирному дню борьбы с дефицитом железа
26 ноября во всем мире проводится ежегодный День борьбы с железодефицитом. В этот день важно актуализировать информацию о проблеме железодефицитной анемии (ЖДА), а также о скрытом (латентном) дефиците железа (ЛЖД). В первую очередь проблема актуальна для женщин репродуктивного возраста, а также для детей.
Чтобы помочь российским женщинам узнать больше о проблеме железодефицита и способах его ранней диагностики, в компании «ЭГИС-РУС» в День борьбы с дефицитом железа запустили социальный проект #тынежелезная. Проект имеет социальную и образовательную ценность. Получить актуальную информацию о дефиците железа в организме в скором времени можно будет на одноименном сайте проекта. На сайте также планируется проведение социальных акций в партнерстве с медицинскими учреждениями, например по проверке уровня ферритина и получению консультаций специалистов.
Поддерживая День борьбы с железодефицитом, компания «ЭГИС-РУС» проводит несколько мероприятий и для своих сотрудников, включая скрининг для женщин и образовательный вебинар. Диагностические и информационные мероприятия «ЭГИС», приуроченные ко Дню борьбы с дефицитом железа, обусловлены актуальностью проблемы латентного железодефицита в современном обществе. Его коварность в том, что показатели гемоглобина у женщины могут быть в пределах нормы, но запасы железа в органах при этом уже истощены. И именно концентрация ферритина в крови, согласно рекомендациям ВОЗ, используется для диагностики его дефицита. Это своеобразный резерв, за формирование и «хранение» которого отвечает белок ферритин. Снижение концентрации этого белка в крови указывает на истощение и позволяет выявить железодефицит уже на ранних стадиях.
Одним из инструментов привлечения внимания к проблеме скрытого железодефицита стал тематический флешмоб #тынежелезная в Facebook. Его цель – поделиться на своей страничке постом о том, насколько важно как можно раньше предотвратить истощение запасов железа в тканях, чтобы не дать развиться железодефицитной анемии. Присоединиться к флешмобу может каждый желающий по хештегу #тынежелезная. Это один из самых простых способов помочь многим женщинам распознать тревожный симптом дефицита железа и побудить их проверить уровень ферритина, чтобы исключить ЛЖД. Этот шаг не будет лишним и при отсутствии ярко выраженных симптомов железодефицита, и является обязательным при их наличии. При обнаружении симптомов и сниженном ферритине следует как можно скорее обратиться к терапевту или гинекологу.
«Будучи социально ответственной компаниeй, мы считаем повышение качества жизни наших пациентов и сотрудников своим главным приоритетом. Тема железодефицита достойна самого широкого освещения, и именно так, рассказывая о коварном недуге и методах борьбы с ним, а также проводя различные диагностические мероприятия, мы еще на один шаг приближаемся к более здоровому будущему для нас и наших детей. Давайте ударим по железодефициту вместе!» – говорит Елена Бершадская, менеджер по связям с общественностью ООО «ЭГИС-РУС».
#тынежелезная – новый социальный проект, приуроченный ко Всемирному дню борьбы с дефицитом железа
26 ноября во всем мире проводится ежегодный День борьбы с железодефицитом. В этот
день важно актуализировать информацию о проблеме железодефицитной анемии (ЖДА), а
также о скрытом (латентном) дефиците железа (ЛЖД). В первую очередь проблема
актуальна для женщин репродуктивного возраста, а также для детей.
Чтобы помочь российским женщинам узнать больше о проблеме железодефицита и
способах его ранней диагностики, в компании «ЭГИС-РУС» в День борьбы с дефицитом
железа запустили социальный проект #тынежелезная. Проект имеет социальную и
образовательную ценность. Получить актуальную информацию о дефиците железа в
организме в скором времени можно будет на одноименном сайте проекта. На сайте также
планируется проведение социальных акций в партнерстве с медицинскими учреждениями,
например по проверке уровня ферритина и получению консультаций специалистов.
Поддерживая День борьбы с железодефицитом, компания «ЭГИС-РУС» проводит
несколько мероприятий и для своих сотрудников, включая скрининг для женщин и
образовательный вебинар. Диагностические и информационные мероприятия «ЭГИС»,
приуроченные ко Дню борьбы с дефицитом железа, обусловлены актуальностью проблемы
латентного железодефицита в современном обществе. Его коварность в том, что
показатели гемоглобина у женщины могут быть в пределах нормы, но запасы железа в
органах при этом уже истощены. И именно концентрация ферритина в крови, согласно
рекомендациям ВОЗ, используется для диагностики его дефицита. Это своеобразный
резерв, за формирование и «хранение» которого отвечает белок ферритин. Снижение
концентрации этого белка в крови указывает на истощение и позволяет выявить
железодефицит уже на ранних стадиях.
Одним из инструментов привлечения внимания к проблеме скрытого железодефицита стал
тематический флешмоб #тынежелезная в Facebook. Его цель – поделиться на своей
страничке постом о том, насколько важно как можно раньше предотвратить истощение
запасов железа в тканях, чтобы не дать развиться железодефицитной анемии.
Присоединиться к флешмобу может каждый желающий по хештегу #тынежелезная. Это
один из самых простых способов помочь многим женщинам распознать тревожный
симптом дефицита железа и побудить их проверить уровень ферритина, чтобы исключить
ЛЖД. А в случае пониженного уровня ферритина – обратиться к врачу.
«Будучи социально ответственной компаний, мы считаем повышение качества жизни
наших пациентов и сотрудников своим главным приоритетом. Тема железодефицита
достойна самого широкого освещения, и именно так, рассказывая о коварном недуге и
методах борьбы с ним, а также проводя различные диагностические мероприятия, мы
еще на один шаг приближаемся к более здоровому будущему для нас и наших детей.
Давайте ударим по железодефициту вместе!» – говорит Елена Бершадская, менеджер
по связям с общественностью ООО «ЭГИС-РУС».
Хронический дефицит железа Статья
Непрерывное образование
Хронический дефицит железа — самый распространенный дефицит питательных веществ в мире и значительная распространенная причина анемии во всем мире. Это в основном вызвано неправильным питанием, кровотечением и нарушением всасывания. В этом упражнении рассматриваются обследование и лечение хронического дефицита железа.
Целей:
- Рассмотрите этиологию хронической недостаточности железа.
- Опишите общие результаты физикального обследования, связанные с хроническим дефицитом железа.
- Обобщите доступные варианты лечения хронической недостаточности железа.
- Подчеркните важность сотрудничества и общения между межпрофессиональной командой для улучшения результатов для пациентов с хроническим дефицитом железа.
Введение
Железо необходимо для множества биологических функций организма.Он необходим для синтеза гемоглобина, миоглобина, регуляции / пролиферации клеток, синтеза ДНК и транспорта электронов в митохондриях. [1]
Почти две трети железа в организме содержится в циркулирующих эритроцитах как часть гемоглобина, а оставшееся железо присутствует в форме запаса (костный мозг, печень и т. Д.) Миоглобина и многих ферментов, участвующих в различных физиологических функциях [2]. ]
Дефицит железа или сидеропения — это состояние, при котором общие запасы железа в организме недостаточны для поддержания нормальных метаболических функций.Железо является наиболее распространенной пищевой недостаточностью во всем мире и является наиболее частой причиной анемии среди примерно 2 миллиардов человек во всем мире. [3]
Дефицит железа может быть абсолютным или функциональным. Особому риску подвержены женщины репродуктивного возраста и дети в возрасте от 0 до 5 лет.
Поскольку не существует четко установленных диагностических критериев дефицита железа без анемии, а симптомы расплывчаты, это легко не заметить. Клиницисты должны подозревать хронический дефицит железа у пациентов с нормальным общим анализом крови, у которых наблюдаются симптомы, сходные с симптомами анемии, и у которых низкий уровень ферритина.Этих пациентов необходимо обследовать на предмет наличия дефицита железа и узнать о кровопотере в истории болезни.
Этиология
Поскольку большая часть железа в организме присутствует в эритроцитах, кровотечение из любого участка может вызвать дефицит железа. Это наиболее частая причина дефицита железа в развитых странах. Открытые причины кровотечения, такие как гематемезис, меноррагия, многоплодная беременность, роды и т. Д., Можно легко распознать, основываясь только на анамнезе.Другие причины, такие как скрытое желудочно-кишечное кровотечение, паразитарные инфекции, такие как анкилостомы, и частое донорство крови, можно легко не заметить. Частая сдача крови — важная причина дефицита железа, особенно у женщин. [4]
Неадекватное питание редко встречается в развитых странах. Есть две формы диетического железа; Гемовое железо, которое присутствует в животных источниках, легче усваивается организмом, чем негемовое железо из растительной пищи. Люди из бедных социально-экономических слоев, вегетарианцы / веганы и пожилые люди, которые не придерживаются сбалансированной диеты, склонны к развитию дефицита железа.У детей младшего возраста чрезмерное потребление молока или сока, длительное кормление из бутылочки и перекусы способствуют дефициту железа [5].
Нарушение всасывания железа возникает при целиакии, атрофическом гастрите, инфекции Helicobacter pylori и бариатрической хирургии. Пониженное всасывание железа также может присутствовать в сочетании с некоторыми диетическими элементами, такими как дубильные вещества, фосфаты, фитаты, оксалаты и кальций.
Некоторые лекарства могут влиять на всасывание железа. Примеры включают препараты, подавляющие кислотность желудочного сока, антибиотики, леводопа, левотироксин, ибандронат.[6]
Дефицит железа также встречается при хронических заболеваниях, таких как хроническая болезнь почек (ХБП), хроническая сердечная недостаточность, воспалительное заболевание кишечника, некоторые злокачественные новообразования, ревматоидный артрит и т. Д.
мутация SLC11A2 и IRIDA (железорезистентная железодефицитная анемия. ) из-за мутации TMPRSS6 являются редкими наследственными состояниями, связанными с дефицитом железа.
Эпидемиология
Согласно проекту ВОЗ «Глобальное бремя болезней 2000» (GBD 2000), дефицит железа является причиной 841 000 смертей во всем мире, причем основное бремя смертности наблюдается в Африке и некоторых частях Азии.[7]
В США дефицит железа наблюдается у 9% детей ясельного возраста в возрасте от 1 до 2 лет. По сравнению с белыми малышами, латиноамериканские малыши в два раза чаще страдают дефицитом железа. Распространенность среди девочек-подростков и женщин репродуктивного возраста составляет от 9% до 11%. Это наиболее часто встречается у повторнородящих женщин из групп меньшинств с низким доходом. У мужчин это наблюдается примерно у 1% населения с несколько более высокой распространенностью — от 2% до 4% у мужчин среднего и старшего возраста [8] [5].
Существует положительная корреляция между ожирением и риском развития дефицита железа.[9]
Патофизиология
Поддержание гомеостаза железа происходит за счет баланса абсорбции и потерь железа. Всасывание в тонком кишечнике является основным регулирующим фактором содержания железа в организме. Железо абсорбируется в двухвалентной форме энтероцитами через переносчик двухвалентного металла (DMT1). После всасывания он секвестрируется в ферритин, если в организме достаточно запасов. Если уровень железа низкий, железо связывается с трансферрином ферропортином.После загрузки в трансферрин железо транспортируется в клетки для метаболизма. Гепсидин — это пептид, который ингибирует ферропортин и снижает всасывание железа в кровоток. [10]
Железо входит в клетки после того, как трансферрин связывается с рецептором трансферрина (TfR). Уровни железа дополнительно контролируются железо-регуляторными белками 1 и 2 (IRP1 и IRP2), которые оптимизируют доступность клеточного железа за счет усиления экспрессии нескольких генов. [11]
Дефицит железа происходит в три стадии.На пре-латентной стадии запасы железа низкие или отсутствуют, но концентрация железа в сыворотке в норме. На латентной стадии насыщение трансферрина и сывороточное железо снижаются в дополнение к низкому уровню ферритина. Последняя стадия отмечена падением гемоглобина вместе с истощением запасов железа и снижением сывороточного железа и насыщения трансферрина. [12]
История и физика
Большинство симптомов являются неспецифическими, включая, помимо прочего, общую слабость, утомляемость, плохую концентрацию внимания, раздражительность, головные боли, одышку при физической нагрузке и снижение способности к физической нагрузке.Это связано с низкой доставкой кислорода к тканям и пониженной активностью железосодержащих ферментов.
Пика встречается примерно у половины этих пациентов, а пагофагия (тяга ко льду) весьма специфична для дефицита железа. [13] У пациентов в анамнезе могут быть сухость во рту, выпадение волос, дисфагия, ломкость ногтей и синдром беспокойных ног.
Бетурия — это находка, которая не специфична для дефицита железа, но чаще встречается у этих людей. Это результат изменения функции желудочно-кишечного тракта из-за тяжелого дефицита железа.Моча становится красной после употребления свеклы. [14]
Медицинский осмотр может быть нормальным или может выявить сухость кожи, выпадение волос, атрофический глоссит, хейлоз, бледность, ломкость ногтей и койлонихию (ногти в форме ложки). Аускультация сердца может выявить систолический шум. [15]
Оценка
Диагноз дефицита железа основывается в основном на анамнезе, обследовании и лабораторных исследованиях. В неосложненных случаях для оценки следует использовать сывороточное железо, трансферрин, ферритин, TIBC и TSAT.Уровень железа в сыворотке крови меняется в течение дня и зависит от диеты. Образец следует брать утром натощак. [12] Абсолютный дефицит железа диагностируется при уровне сывороточного ферритина менее 30 нг / мл [16].
TSAT рассчитывается как отношение сывороточного железа к TIBC. Это один из самых ранних биомаркеров дефицита железа, который полезен, когда уровень ферритина в сыворотке однозначен. Уменьшение (менее 20%) указывает на дефицит железа, абсолютный или функциональный. [15] [3]
Гемоглобин не снижается до тех пор, пока не истощится значительный процент железа в организме.Следовательно, нормальный гемоглобин не исключает дефицита железа.
Другие исследования железа, доступные для оценки дефицита железа:
- Растворимый рецептор трансферрина (sTfR) и индекс sTfR-ферритина — sTfR повышается при дефиците железа из-за повышенной регуляции рецепторов трансферрина. Он может помочь различить абсолютный (повышенный sTfR) и функциональный ID (нормальный sTfR). [3] [17] [3]
- Соотношение протопорфирин цинка / гем — Снижение поступления железа для образования гемоглобина приводит к увеличению использования цинка и увеличению отношения ZPP / H; это предпочтительнее инвазивной аспирации костного мозга.[17]
- Содержание гемоглобина в ретикулоцитах — обеспечивает оценку доступности железа для производства эритроцитов за несколько дней до теста. Таким образом, это полезный индикатор раннего дефицита железа, и последовательные измерения также могут помочь определить ответ на парентеральную терапию железом. Воспаление не влияет на этот параметр и полезно для определения статуса железа у пациентов с ХБП. [17] [18]
Лечение / менеджмент
Пациентам с неосложненным дефицитом железа без сопутствующих заболеваний следует назначать пероральную терапию железом.Пероральное железо доступно, недорого, эффективно, безопасно и удобно. Некоторые из доступных составов включают сульфат железа, фумарат железа и глюконат железа. Декстран с высоким молекулярным весом был исключен из-за высокой частоты серьезных анафилактических реакций. [10]
Побочные эффекты со стороны желудочно-кишечного тракта (ЖКТ) возникают у 70% пациентов, принимающих пероральное железо, что приводит к несоблюдению режима лечения. Симптомы со стороны желудочно-кишечного тракта можно свести к минимуму с помощью хелатных форм железа. Таблетки с энтеросолюбильным покрытием плохо всасываются и не подходят.[16] [17] [19]
Внутривенное железо доступно во многих формах, таких как карбоксимальтоза трехвалентного железа, глюконат трехвалентного железа, сахароза трехвалентного / железа, ферумокситол и низкомолекулярный декстран железа. Ответ на внутривенное введение железа заслуживает наблюдения, чтобы установить необходимость в дополнительных добавках через шесть-восемь недель после первоначальной замены железа. [3]
Все препараты железа, вводимые внутривенно, имеют низкий риск аллергических реакций. Премедикация антигистаминными препаратами не предотвращает инфузионных реакций и не должна применяться.Пациенты с астмой или лекарственной аллергией в анамнезе должны получать стероиды перед инфузией.
Во время беременности пероральное железо назначают в качестве добавки в течение первого триместра, поскольку безопасность внутривенного введения железа в первом триместре остается неустановленной. Обычно пероральное железо назначают беременным женщинам, если они могут его переносить. Исключение составляют женщины с тяжелой анемией, женщины с воспалительным заболеванием кишечника и те, кто перенес бариатрическую операцию. У этих пациентов предпочтительнее внутривенное введение железа. Все внутривенные формы обладают одинаковой эффективностью и безопасностью, за исключением некоторых составов глюконата железа, в которых бензиловый спирт используется в качестве консерванта, и их следует избегать из-за возможности причинения вреда плоду.
Дифференциальная диагностика
Дифференциальный диагноз дефицита железа без анемии широк, поскольку большинство симптомов неспецифичны и наблюдаются при многих других состояниях. Они могут включать причины усталости, например фибромиалгию, синдром хронической усталости, депрессию / расстройства настроения, хронические заболевания, гипотиреоз и т. Д. Дифференциальные диагнозы также включают другие причины пика, например, расстройства пищевого поведения, психические расстройства, недоедание и причины беспокойного состояния. неврологические состояния, похожие на синдром ног, и беременность.
Прогноз
Дефицит железа — это легко поддающееся лечению состояние с отличным прогнозом в неосложненных случаях без сопутствующих заболеваний.
Если не лечить, это связано со значительной заболеваемостью и смертностью, особенно у пожилых людей и людей с сопутствующими хроническими заболеваниями, например сердечной недостаточностью, ХБП [1].
Осложнения
При отсутствии лечения дефицит железа связан со значительными когнитивными нарушениями и низким качеством жизни.
Во время беременности нелеченный дефицит железа может повлиять на созревание мозга плода, вызвать низкий вес при рождении и предрасположить ребенка к развитию дефицита железа. Неблагоприятные исходы для матери включают депрессию, повышенный риск сепсиса и материнскую смертность. [2] [20]
У пациентов, перенесших операцию на сердце или брюшной полости, предоперационный дефицит железа коррелирует с плохими результатами [16].
У пациентов с сердечной недостаточностью хронический дефицит железа связан с увеличением смертности.
Сдерживание и обучение пациентов
Пациентам следует проконсультироваться по поводу употребления продуктов, богатых железом, фруктов и овощей с высоким содержанием витамина C.
У младенцев, рожденных от железодефицитных матерей, отсроченное пережатие пуповины может помочь предотвратить дефицит железа у новорожденных. [20]
У младенцев после шести месяцев грудного вскармливания железо следует дополнять зерновыми продуктами, обогащенными железом, и смесями.Детям с паразитарными инфекциями следует давать противоглистные препараты. В регионах, где распространен дефицит железа, женщины репродуктивного возраста должны ежедневно принимать добавки железа. [10] [2]
Жемчуг и другие выпуски
Дефицит железа можно предотвратить. Скрининг может выявить дефицит железа на ранней стадии и улучшить результаты. Целесообразно проводить ежегодный скрининг с помощью клинического анализа крови и исследований железа в группах высокого риска. E.g., женщины с меноррагией, низким потреблением железа или дефицитом железа в анамнезе. Как правило, женщины репродуктивного возраста могут каждые пять лет проходить скрининг на гемоглобин или гематокрит. Может быть разумным проверять мужчин и женщин в постменопаузе один или несколько раз, если присутствуют какие-либо факторы риска.
Улучшение результатов команды здравоохранения
Хронический дефицит железа — глобальная проблема здравоохранения. Это легко упустить из виду, поскольку изложение часто бывает расплывчатым и неспецифическим.В развивающихся странах недостаточное питание является основной причиной хронического дефицита железа, тогда как кровотечение является основной причиной хронического дефицита железа в развитых странах. Причины дефицита железа могут быть связаны с различными гинекологическими, акушерскими, метаболическими и желудочно-кишечными причинами. Медицинский осмотр часто бывает нормальным, и причину невозможно определить без лабораторных исследований.
Лечащий врач всегда должен оказывать помощь пациенту.При необходимости важно проконсультироваться с гематологом, акушером-гинекологом или гастроэнтерологом. Диетолог может сыграть важную роль в первичной профилактике дефицита железа путем корректировки диеты. Лабораторные технологи играют жизненно важную роль в диагностике хронического дефицита железа. Фармацевты могут помочь выбрать подходящие препараты железа для перорального или внутривенного введения, которые лучше всего соответствуют потребностям пациента. Медсестры не только обучают пациентов, но и помогают проводить лечение. Эффективное сотрудничество и общение между медицинскими работниками может обеспечить оптимальные результаты для всех пациентов.[Уровень 5]
(Щелкните изображение, чтобы увеличить)
Ретикулоциты, анемия, ЖДА, железодефицитная анемия, гематопатология, микроцитоз, гипохромия
Предоставлено Эдом Усманом (CC by 2.0) https://creativecommons.org/licenses/by/2.0/
(Щелкните изображение, чтобы увеличить)
Железодефицитная анемия
Изображение предоставлено S Bhimji MD
Скрытый дефицит железа — насколько пустых запасов железа достаточно для постановки правильного диагноза?
Международные исследования показали, что уровень ферритина менее 30 является эталонным значением для диагностики латентного дефицита железа.Такое значение также используется, например, во многих местах Финляндии [1] [2]. В Эстонии медицинский персонал также должен следовать тем же инструкциям, но все зависит от врача и его знаний о латентном дефиците железа. Часто строго соблюдаются лабораторные контрольные значения, тогда как нижнее контрольное значение в Эстонии для взрослых женщин составляет всего 10 [3]. В таких случаях без внимания остаются люди с симптомами дефицита железа, страдающие латентным дефицитом железа, не говоря уже о тех, у кого симптомы отсутствуют.
Всегда ли есть симптомы скрытого дефицита железа?
Все зависит от человека — все мы по-разному переносим дефицит железа. Есть люди, у которых есть симптомы с уровнем ферритина ниже 30 и даже выше, но есть также люди, у которых уровень ферритина очень низкий без каких-либо симптомов. Это делает скрытый дефицит железа крайне опасным — без знания уровня ферритина у человека невозможно правильно оценить его или ее запасы железа. Тест на ферритин — один из важнейших анализов при диагностике дефицита железа [3].
В исследовании 2018 года, в котором измерялись гематологические параметры детей из разных возрастных групп, анализировались нижние пределы референсных значений значений ферритина, когда гематологические параметры детей больше не менялись или не улучшались. В этом исследовании предлагалось принять во внимание следующие значения ферритина у детей для диагностики латентного дефицита железа: от 4 месяцев до 13 лет 26 мкг / л и от 13 до 19 лет (в т.ч.) 39 мкг / л.
Доктор Неве Вендт и доктор Хели Грюнберг из Детской клиники больницы Тартуского университета провели исследование среди детей в возрасте 9–12 месяцев в Эстонии, страдающих латентным дефицитом железа и железодефицитной анемией. Также врачи из клиники Тартуского университета подчеркнули важность того, что измерения гемоглобина недостаточны для диагностики дефицита железа. Для предотвращения железодефицитной анемии важно правильно диагностировать скрытый дефицит железа [5].
Вреден ли скрытый дефицит железа? Что происходит в нашем организме при скрытом дефиците железа?
- Международное исследование показало, что мозг страдает от дефицита железа, когда уровень ферритина снижается ниже 35 мкг / л -> вредный неврологический эффект, нарушения развития мозга [4]
- детей с низким запасом железа чаще страдают от трудностей в обучении и концентрации внимания, нарушений когнитивного и моторного развития [6]
- взрослых и детей страдают снижением физической выносливости и работоспособности [6]
Доктор Вендт и доктор Грюнберг из Эстонии также отметили, что в случае латентного дефицита железа наш организм страдает физиологическими нарушениями мозга, крови и мышц [5]. Когда латентный дефицит железа уже развился и на дефицит железа не обращают внимания, мозг может страдать от необратимых неврологических нарушений в виде поведенческих нарушений, которые уже невозможно исправить с помощью лечения железом [4]. Таким образом, латентный дефицит железа чрезвычайно вреден для младенцев и детей, мозг которых все еще развивается. Лечение железом в случае правильно диагностированного дефицита железа очень важно, но еще важнее предотвращение латентного дефицита железа, чтобы предотвратить необратимое повреждение детского мозга и железодефицитную анемию. Самым критическим временем для младенцев и детей ясельного возраста являются первые 1000 дней, когда мозг развивается очень быстро [4].
Группы риска латентного дефицита железа?
- растущих детей, в основном в возрасте 6–24 месяцев: Повышенная потребность в железе во время фаз роста является одним из факторов риска дефицита железа. Железо из пищи не компенсирует повышенную потребность в железе в эти периоды. Узнайте больше о дефиците железа у детей ясельного возраста из ЗДЕСЬ .
- младенцы с массой тела при рождении менее 3 кг и недоношенные дети -> низкие запасы железа уже при рождении
- женщины фертильного возраста : железо выходит из организма в основном через кровь. Женщины фертильного возраста входят в группу риска из-за менструации. При нормальной менструации женщины теряют примерно 25–45 мл крови, а верхний предел кровопотери составляет около 80 мл. Обильные менструации при кровопотере более 80 мл [7]. 1 мл крови = 0,5 мг железа, следовательно, 30 мл кровопотери означает потерю железа 15 мг.Чтобы компенсировать эту сумму в течение 3–4 недель (до начала новой менструации), мы должны съесть 1,5 кг красного мяса, а здесь мы учли только 30 мл кровопотери. Многие женщины страдают от кровопотери гораздо большей, чем 30 мл. Часто причиной является не небольшое количество железа из пищи, а отрицательный баланс железа во время менструации. Нельзя лечить железодефицитную анемию (анемию) пищей! Мы писали больше о менструации и утюге из ЗДЕСЬ .
- беременных : повышенная потребность в железе во время беременности также является одним из факторов риска.Железо из пищи не компенсирует повышенную потребность во время беременности, и Всемирная организация здравоохранения (ВОЗ) рекомендует принимать 30–60 мг железа в день с начала до конца беременности [8]. Подробнее о беременности и дефиците железа читайте в ЗДЕСЬ .
- пожилые люди : несбалансированное питание и хронические заболевания являются фактором риска дефицита железа. Хронические и инфекционные заболевания ослабляют всасывание железа. Это связано с гормоном гепсидином, о котором мы говорили ЗДЕСЬ .Пожилые люди также часто страдают кишечной кровопотерей.
- веганы и вегетарианцы : веганы и вегетарианцы находятся в группах риска, когда диета несбалансирована и гемовое железо не компенсируется хорошими негемовым источником железа, такими как цельнозерновые продукты, бобовые, орехи, семена, сухофрукты, гречневая крупа. Поглощение гемового железа составляет около 25% и 10% для негемового железа, но источники негемового железа часто содержат во много раз больше элементарного железа на 100 г по сравнению с мясом. Источники негемового железа также содержат витамин С, который способствует усвоению железа.Таким образом, не следует недооценивать важность негемового железа в нашем рационе [9]. Мы писали о негемовом и гемовом железе ЗДЕСЬ .
- человек, потребляющих много молочных продуктов : молочные и молочные продукты содержат много кальция и белка, называемого казеином. Кальций и казеин ослабляют усвоение железа. Подробнее о коровьем молоке анемии от ЗДЕСЬ .
Источники:
[1] F. Ebeling et al. Raudanpuute ilman anemiaa — miten ferritiiniarvoa tulkitaan? Lääkärilehti 8/2019.[2] Goodnough LT, Nemet E. Дефицит железа и связанные с ним расстройства. Кирьясса: Грир Дж. П., Арбер Д. А., Глэдер Б. Э., Лист А. Ф., Означает РТ, Роджерс Г. М., тоим. Wintrobe’s Clinical Hematology, 14. painos. Wolters Kluwer Health 2018: 615–43. [3] Synlab Eesti. Ферритиин. [4] Cusick SE, Georgieff MK, Rao R. Подходы к снижению риска дисфункции мозга у детей, вызванной дефицитом железа в раннем возрасте. Питательные вещества. 2018; 10 (2): 227. Опубликовано 17 февраля 2018 г. [5] Н. Вендт и Х. Грюнберг. Kuidas Diagnoosida ja ennetada rauapuudust imikutel? Eesti Arst 2009.88 (7-8): 481-484. [6] Arcanjo FP, Arcanjo CP, Сантос PR. Школьники с трудностями в обучении имеют низкий уровень железа и высокую распространенность анемии. J Nutr Metab. 2016; 2016: 7357136. [7] Günekoloog Ivi Saar — Valvekliinik. [8] КТО. Ежедневный прием добавок железа и фолиевой кислоты во время беременности. [9] ] А. Аро, М. Мутанен, М. Ууситупа. Ravitsemustiede, 4. – 7. том, 2017.
У меня диагностировали дефицит железа, что теперь?
Дефицит железа — наиболее распространенный дефицит питательных веществ в развитом мире, которым страдает примерно каждая третья женщина репродуктивного возраста.
Это может развиться, когда потребление железа или скорость его абсорбции не в состоянии удовлетворить потребности организма в железе, вызывая слабость, утомляемость, плохую концентрацию внимания, головные боли и непереносимость физических упражнений.
Читать далее:
Почему железо так важно в вашем рационе
Дефицит железа имеет несколько стадий серьезности и диагностируется с помощью анализа крови, показывающего уровень сывороточного ферритина (белка, который накапливает железо в организме) и / или гемоглобина (белка, ответственного за транспортировку кислорода в крови).
Если уровень ферритина в сыворотке ниже 30 мкг / л (микрограмм на литр), то запасы железа истощаются (первая стадия или истощение запасов железа).
При уровнях ферритина в сыворотке менее примерно 20 мкг / л ткани и клетки не получают железо, необходимое для правильного функционирования (вторая стадия или скрытый дефицит железа).
Последняя и наиболее тяжелая стадия — железодефицитная анемия. На этом этапе красные кровяные тельца больше не могут переносить достаточное количество кислорода по телу, что вызывает крайнюю слабость и усталость.
Причины
Для врачей и медицинских работников важно попытаться определить причину дефицита железа, поскольку это может быть побочным эффектом серьезного основного заболевания. Это может быть сложно, так как существует множество возможных причин, например:
-
Кровопотеря, часто в результате обильных или продолжительных менструаций, кровотечений или частого донорства крови
-
Быть вегетарианцем, веганом или придерживаться диеты с недостаточным усвоением железа
-
Нарушение всасывания питательных веществ из кишечника, вызванное такими состояниями, как целиакия или синдром раздраженного кишечника
-
Повреждение красных кровяных телец из-за экстремальных тренировок, часто встречается у профессиональных спортсменов
-
Генетическая предрасположенность.
Дополнение
Несмотря на причину, начальное лечение всегда должно включать добавку железа, чтобы помочь быстро улучшить статус железа и предотвратить прогрессирование железодефицитной анемии.
Добавки в высоких дозах могут вызывать побочные эффекты со стороны желудочно-кишечного тракта.
MIA Studio / Shutterstock
Текущие клинические руководства рекомендуют добавку в высоких дозах 80-105 мг элементарного железа. Но клинические испытания также показали, что 60 мг может быть достаточно для эффективного лечения женщин с дефицитом железа.
Врачи часто рекомендуют безрецептурное лечение железом в форме сульфата железа, например Ferro-Gradumet. Некоторые составы содержат витамин С, который может улучшить усвоение дополнительного железа.
Добавки железа в высоких дозах, как правило, рекомендуются только до тех пор, пока запасы железа у человека не будут пополнены, и это будет подтверждено анализом крови, через три-шесть месяцев после начала приема.
Высокодозированные добавки железа могут иметь побочные эффекты, включая тошноту, запор и вздутие живота.Это может затруднить прием добавок, поэтому лечение должно быть только краткосрочным.
Читать далее:
Проверка здоровья: могут ли витамины дополнить плохой рацион?
Побочные эффекты могут быть уменьшены путем приема добавки во время еды, а не натощак, или путем противодействия запорам с помощью пищевых добавок. Но оба из них, вероятно, уменьшат усвоение железа из добавки. Если у вас действительно возникают проблемы с переносимостью добавок железа в высоких дозах, поговорите со своим врачом или фармацевтом о вариантах с более низкими дозами или альтернативных формах.
Сколько железа вам нужно?
В долгосрочной перспективе важно устранить причину дефицита железа, что может означать увеличение потребления и усвоения железа.
Менструирующим женщинам (в возрасте 19–50 лет) требуется около 18 мг железа в день, что более чем вдвое превышает рекомендуемое количество для австралийских мужчин (8 мг). Многим женщинам может быть трудно добиться этого только с помощью диеты, но это можно сделать, если посоветовать правильный рацион.
Женщинам требуется вдвое больше железа, чем мужчинам.Стейси Розеллс
Это было показано в исследовании, в котором женщины с дефицитом железа были рандомизированы для получения либо высоких доз железа (105 мг в день), либо диетического консультирования для достижения диеты с высоким содержанием железа. Хотя добавка железа привела к более быстрому восстановлению запасов железа по сравнению с группой, получавшей диету, группа с высоким содержанием железа продолжала улучшать свой статус железа в течение длительного периода времени.
В качестве бонуса группа, потребляющая диету с высоким содержанием железа, увидела более значительные улучшения в отношении здоровья и благополучия, таких как психическое здоровье и жизнеспособность.
Что такое диета с высоким содержанием железа?
Высокое общее потребление железа с пищей не гарантирует хорошего уровня железа. Это связано с тем, что усвоение пищевого железа является сложным и зависит от многих диетических факторов.
Самый важный из них — это тип диетического железа, которых два. Гемовое железо содержится в мясе, рыбе и птице. Негемное железо поступает из хлеба и круп, овощей и фруктов.
Из кишечника всасывается 25-35% гемового железа по сравнению с 2-15% негемного железа, поэтому вам нужно съесть значительно больше негемного железа, чтобы поглотить такое же количество.Следовательно, употребление в пищу красного мяса (которое содержит больше всего гемового железа), рыбы или птицы действительно может повысить усвоение железа.
Также важно употреблять разнообразные продукты, не содержащие гема, для хорошего долгосрочного содержания железа. Хорошие источники включают бобы, чечевицу, тофу, макаронные изделия, хлопья для завтрака (многие из которых обогащены железом), хлеб, рис, яйца, сухофрукты, орехи и овощи, такие как брокколи, цветная капуста, капуста, горох и бобы. Фактически, большая часть пищевого железа поступает из негемных источников, таких как хлеб и крупы.
Читать далее:
Почему вы должны придерживаться растительной диеты, но это не значит, что вы вегетарианец
Австралийское руководство по здоровому питанию рекомендует женщинам потреблять пять порций овощей, две порции фруктов, шесть порций хлеба и круп, 2,5 порции мяса и альтернативы и 2,5 порции молочных продуктов в день. Вы, вероятно, получите рекомендованные 18 мг железа, если будете придерживаться этих рекомендаций, и включите в них: обогащенные железом хлопья для завтрака в качестве одной порции хлеба / хлопьев; одна порция зеленых листовых овощей, таких как шпинат; и одна порция мяса, курицы или рыбы в категории «мясо / альтернативы».
Еще одна ключевая стратегия — повысить вашу способность усваивать железо. Продукты, богатые витамином С, хорошо известны своей способностью повышать усвоение железа, поэтому включайте их в каждый прием пищи в виде свежих фруктов, овощей и салатов. К другим ускорителям всасывания железа относятся лимонный сок, уксус и алкоголь.
Продукты, богатые витамином С, помогают усваивать железо.
Люк Майкл
Помимо того, что красное мясо, рыба и птица являются хорошим источником гемового железа, они также содержат особое соединение, которое усиливает всасывание негемного железа.Итак, идеальная еда для хорошего усвоения железа — это небольшой кусок нежирного мяса, курицы или рыбы с заправленным салатом и бокалом вина, дополненный свежими фруктами.
Чего следует избегать
В продуктах питания и напитках также содержатся вещества, которые препятствуют всасыванию железа, связывая его в кишечнике, поэтому оно проходит через желудочно-кишечный тракт, не всасываясь. К ним относятся: дубильные вещества и полифенолы, содержащиеся в чае и кофе; оксалаты, содержащиеся в шпинате; и фитаты, содержащиеся в продуктах с высоким содержанием клетчатки и бобовых.
Хотя многие из них очень полезны по другим причинам, тем, кто придерживается вегетарианской диеты, особенно необходимо знать об их эффектах. Вы можете бороться с ними, добавляя большое количество усилителей всасывания железа во время еды и воздерживаясь от чая или кофе в течение как минимум часа после еды.
И последнее, что следует учитывать, это то, что другие минералы, в частности кальций и цинк, могут конкурировать с железом за усвоение. Хотя это не большая проблема в контексте сбалансированной диеты, прием другой минеральной добавки может повлиять на усвоение железа.Поэтому посоветуйтесь с врачом или диетологом по поводу любых добавок, которые вы принимаете.
% PDF-1.4
%
16654 0 объект
>
эндобдж
xref
16654 85
0000000016 00000 н.
0000003680 00000 н.
0000003821 00000 н.
0000004135 00000 п.
0000004183 00000 п.
0000004360 00000 н.
0000004708 00000 п.
0000005790 00000 н.
0000005986 00000 н.
0000007766 00000 н.
0000008865 00000 н.
0000009948 00000 н.
0000010154 00000 п.
0000010352 00000 п.
0000011453 00000 п.
0000012538 00000 п.
0000013632 00000 п.
0000014722 00000 п.
0000015798 00000 п.
0000016871 00000 п.
0000017957 00000 п.
0000019063 00000 п.
0000020152 00000 п.
0000021238 00000 п.
0000022335 00000 п.
0000023432 00000 п.
0000024525 00000 п.
0000024550 00000 п.
0000042321 00000 п.
0000042521 00000 п.
0000042546 00000 п.
0000054154 00000 п.
0000054347 00000 п.
0000054372 00000 п.
0000077279 00000 н.
0000077482 00000 п.
0000077507 00000 п.
0000088268 00000 п.
0000088476 00000 п.
0000088501 00000 п.
0000100437 00000 н.
0000100634 00000 н.
0000100658 00000 н.
0000106661 00000 п.
0000106853 00000 п.
0000106878 00000 н.
0000115738 00000 н.
0000115945 00000 н.
0000115970 00000 н.
0000135484 00000 н.
0000135673 00000 н.
0000135698 00000 п.
0000141474 00000 н.
0000141661 00000 н.
0000141686 00000 н.
0000153565 00000 н.
0000153763 00000 н.
0000153788 00000 н.
0000162645 00000 н.
0000162859 00000 н.
0000162884 00000 н.
0000176688 00000 н.
0000177783 00000 н.
0000177808 00000 н.
0000194176 00000 н.
0000195255 00000 н.
0000195280 00000 н.
0000222727 00000 н.
0000223822 00000 н.
0000223847 00000 н.
0000229644 00000 н.
0000229836 00000 н.
0000229861 00000 н.
0000238539 00000 н.
0000238742 00000 н.
0000238766 00000 н.
0000242013 00000 н.
0000242223 00000 н.
0000242248 00000 н.
0000251509 00000 н.
0000251721 00000 н.
0000251745 00000 н.
0000255263 00000 н.
0000255468 00000 н.
0000002051 00000 н.
трейлер
] >>
startxref
0
%% EOF
16738 0 объект
> поток
;.6tawO & 7iȫh «6; 4Qn% D01Ԍ9d
+ M c * — # l / Vk ְ Vfd37hp & UGºk
Диагностическое обследование пациентов с анемией: роль дефицита железа
Цели
Диагностика нарушений метаболизма железа может быть сложной задачей, если оно сопровождается воспалением. Для улучшения классификации анемий были созданы новые диагностические инструменты, такие как «график Томаса» (TP) (связь растворимого рецептора трансферрина [sTfR] / log ферритина с содержанием гемоглобина в ретикулоцитах [RET-H e ]).Целью этого ретроспективного исследования было оценить дополнительную диагностическую ценность TP при лечении анемии.
Методы
Пациенты с декабря 2016 года по сентябрь 2018 года с общим анализом крови, статусом железа, RET-H e и sTfR были вручную классифицированы по четырем квадрантам TP на основе обычных маркеров железа. Ручные классификации и классификации на основе алгоритмов сравнивались с использованием перекрестных таблиц, диаграмм с усами-усами, а также рабочих характеристик приемника (ROC) для расчета диагностической точности с использованием анализа площади под кривой (AUC).
Результаты
Всего можно было обследовать 3745 пациентов с обычным статусом железа, включая 1721 TP. В 70% случаев ручная классификация была идентична ТП, в 10% она была отклоняющейся. 20% не могут быть четко классифицированы, в основном из-за воспалительных состояний. В отсутствие воспалительного заболевания ферритин был надежным параметром для определения дефицита железа (ID) (AUC 0,958). При наличии воспаления значение индекса ферритина (AUC 0.917) и RET-H e (AUC 0,957) увеличились.
Выводы
TP может быть полезен для выявления причин анемии в сложных случаях. Желательны дальнейшие исследования с акцентом на особые группы пациентов, например, онкологические или ревматические пациенты.
Введение
Дефицит железа является наиболее частой причиной анемии как минимум в 50% всех случаев [1]. Диагностика у молодых пациентов без сопутствующих заболеваний достаточно проста путем определения анализа крови и ферритина.Однако как диагностика, так и лечение нарушений метаболизма железа являются сложной задачей, если они возникают в контексте почечной анемии или в сочетании с острыми или хроническими воспалительными заболеваниями, инфекциями или злокачественными опухолями [2]. Эта так называемая «анемия хронического заболевания» (ACD) является второй по частоте анемией после железодефицитной анемии (ЖДА) и, вероятно, наиболее частой причиной у госпитализированных пациентов [3]. Патофизиология основана на многочисленных иммуно-опосредованных ответах, которые влияют на метаболизм железа и приводят к неадекватной выработке эритропоэтина, к снижению реакции костного мозга на эритропоэтин, на индуцированное цитокинами ингибирование эритропоэза, на индуцированное гепсидином удержание железа в ретикулоэндотелиальной системе ( RES), а также для сокращения выживаемости эритроцитов [4], [5], [6], [7], [8].Следовательно, может быть трудно отличить ЖДА от ACD во время острой фазовой реакции (APR), обычные параметры железа (ферритин, трансферрин, насыщение трансферрина (TSAT) нечувствительны и имеют ограниченное применение [2], [9], [10].
Для более дифференцированной диагностики функционального дефицита железа (FID) в контексте ACD в течение нескольких лет доступны дополнительные гематологические маркеры. К ним относятся растворимый рецептор трансферрина (sTfR) и, полученный из ферритина и sTfR, индекс ферритина как индикатор запаса железа, а также гемоглобин ретикулоцитов (RET-H e ) как показатель текущей потребности в железе для эритропоэза. .Если оба биомаркера объединены, для классификации и оценки анемии получается диаграмма на основе алгоритма («график Томаса» [TP]). Можно выделить четыре стадии метаболизма железа (рис. 1) [9], [11].
Рисунок 1:
Диагностическая диаграмма (TP) с четырьмя квадрантами для определения различных состояний метаболизма железа. Классификация выполняется в соответствии со значениями порогового значения для конкретного метода для индекса ферритина: 14 (Beckman Coulter DxI 800) и RET-H e : 28 пг (Sysmex XN-2000).
Клинические симптомы ACD и IDA идентичны и характеризуются утомляемостью, физической слабостью и снижением умственной работоспособности [2]. Дефицит железа препятствует работе митохондрий, клеточному метаболизму, активности ферментов и синтезу нейромедиаторов [12]. Кроме того, дефицит железа может вызвать повышенную восприимчивость к инфекциям и сердечной недостаточности [13]. Многочисленные исследования пришли к выводу, что замещение железа может улучшить симптомы, физическую работоспособность и качество жизни с приемлемыми побочными эффектами [14], [15].Вышеупомянутые симптомы часто связывают с основным заболеванием, особенно в случае существующей ACD. Поэтому во многих случаях дальнейшая диагностика наличия FID не начинается [8]. Распространенность реального дефицита железа в сочетании с АКД колеблется от 20 до 85% [2], [, 3, 1617].
Целью этого исследования было ретроспективно зарегистрировать распространенность анемии в больнице с максимальным уходом, а также сравнить и оценить диагноз с использованием обычных параметров железа и TP.Рациональным для этого исследования было то, что это сравнение до сих пор в основном проводилось в условиях исследования только с тщательно отобранными пациентами или в ретроспективных исследованиях с довольно низким числом случаев. Таким образом, неоднородность когорты пациентов напоминала нормальную популяцию пациентов. Таким образом, можно было оценить, применимы ли «новые» параметры в повседневной клинической практике и могут ли они повысить диагностическую и терапевтическую ценность. Помимо улучшения результатов лечения пациентов, это также включает экономические аспекты в отношении использования концентратов эритроцитов, препаратов железа для внутривенного введения и агентов, стимулирующих эритроциты (ESA).
Материалы и методы
Субъекты
Это исследование проводилось в больнице максимального ухода на юго-западе Германии (Marienhospital Stuttgart, Germany). В первую очередь, это включало всех пациентов, которые проходили анализ крови в отделении лабораторной медицины в период с декабря 2016 года по сентябрь 2018 года. Сюда входили стационарные и амбулаторные пациенты из всех отделений больницы. Кроме того, в Институте были проанализированы образцы крови из внешних практик, включая нефрологическую практику с примерно 150 пациентами на диализе в квартал.Использовались только данные взрослых пациентов, и никаких дополнительных ограничений не накладывалось для получения реалистичной картины когорты пациентов. Для генерации данных был выполнен систематический и анонимный запрос данных о пациентах и лабораторных данных из лабораторной информационной системы (ЛИС) LabCentre (i-solutions Health, Мангейм, Германия). Протокол исследования был одобрен Комитетом по этике II Гейдельбергского университета (медицинский факультет Мангейма), Германия.
Методы
Для анализа использовались следующие параметры крови EDTA: гемоглобин (Hb), эритроциты, средний корпускулярный объем (MCV), средний корпускулярный гемоглобин (MCH), лейкоциты, тромбоциты и эквивалент ретикулоцитов и гемоглобина (RET-H e ).Параметры анализа крови определяли с помощью прибора XN-2000 (Sysmex Corporation, Гамбург, Германия). Кроме того, были оценены следующие параметры сыворотки: ферритин, трансферрин и сывороточное железо, из которого происходит TSAT, C-реактивный белок (CRP), креатинин, лактатдегидрогеназа (LDH), витамин B12 и sTfR. Определение сывороточного железа, ЛДГ, креатинина и СРБ было выполнено Architect ci8200 от Abbott (Висбаден, Германия). Ферритин, sTfR и витамин B12 определяли с помощью автоматического иммуноанализа с использованием UniCel DxI 800, а трансферрин — с помощью нефелометрии на Immage (оба — Beckman Coulter, Крефельд, Германия).Индекс ферритина рассчитывали по формуле sTfR / декадный логарифм (log) ферритина.
Анализ данных был выполнен с помощью SPSS Statistics версии 25.0 (IBM, Чикаго, Иллинойс, США). В анализ был включен только хронологически первый полный набор данных по каждому пациенту. Дальнейшая классификация и оценка были основаны на значениях контрольного диапазона, перечисленных в таблице 1.
Таблица 1:
Референсные диапазоны лабораторных тестов, использованных в данном исследовании.
| Установка | Секс | Диапазон значений | |
|---|---|---|---|
| Гемоглобин | г / дл | м | 13.0–17,5 |
| f | 12,0–16,0 | ||
| MCV | fL | 80–96 | |
| МСН | стр. | 28–33 | |
| Эритроциты | × 10 12 / л | м | 4,5–5,9 |
| f | 4.1–5.1 | ||
| Лейкоциты | × 10 6 / л | 3,5–9,8 | |
| Тромбоциты | × 10 6 / л | 130–400 | |
| Ретикулоциты | % | 0,7–2,5 | |
| Ферритин | нг / мл | м | 15–275 |
| f | 10–204 | ||
| Трансферрин | мг / дл | 202–336 | |
| Насыщение трансферрина | % | 16–45 | |
| Сыворотка железа | мкг / дл
(× 0.1791 = мкмоль / л) |
м | 40–120 |
| f | 39–149 | ||
| Ret-H e | стр. | > 28 | |
| СТФР | нмоль / л
(× 0,0737 = мг / л) |
12,16–27,25 | |
| Витамин B12 | пг / мл | 187–883 | |
| LDH | U / L | м | 135–225 |
| f | 135–214 | ||
| Креатинин | мг / дл
(× 88.4 = мкмоль / л) |
0,7–1,3 | |
| CRP | мг / л | <10 |
Пациенты исключались из дальнейшего обследования, если уровень ферритина превышал 1000 нг / мл или TSAT превышал 50%. В этих случаях было невозможно определить, присутствовала ли ятрогенная перегрузка железом или она была частью основного гематологического заболевания.Кроме того, не рассматривались случаи с MCV> 96 мкл без исключения дефицита витамина B12 и случаи с доказанным дефицитом витамина B12. Пациенты с би- или трицитопенией как показанием к наличию основного гематологического заболевания или недавней химиотерапии также были исключены. Каждый случай был вручную отнесен к одной из четырех категорий ТП. Согласно критериям ВОЗ, анемия у женщин характеризовалась значением Hb <12 г / дл, а у мужчин <13 г / дл [18].
Исследователь был ослеплен по параметрам sTfR, ферритинового индекса и RET-H e .
Классификация проводилась согласно следующим условиям:
-
IDA (квадрант 3): уровни ферритина <10 нг / мл у женщин и <15 нг / мл у мужчин или уровни ферритина <100 нг / мл и TSAT <15% при CRP <10 мг / л.
-
Скрытый дефицит железа (Latent ID) (квадрант 2): гемоглобин в пределах нормы, но уровни ферритина <10 нг / мл у женщин и <15 нг / мл у мужчин.
-
ACD (квадрант 1): Hb снижен, MCV, MCH и ретикулоциты в пределах нормы, уровни ферритина> 10 или> 15 нг / мл, TSAT> 15 и <50%, CRP> 10 мг / л или креатинин> 1 .3 мг / дл.
-
FID / ACD (квадрант 4): MCV и / или MCH снижены, TSAT <15% и CRP / лейкоциты в пределах нормы, уровни ферритина нормальные или повышенные, дополнительная почечная недостаточность или онкологическое заболевание как индикатор ACD.
Если пациенты не могли быть классифицированы на основе вышеупомянутых критериев, они классифицировались следующим образом:
-
Здоровое или возможное хроническое заболевание без текущей анемии: Hb, MCH, MCV, ферритин и TSAT в пределах нормы, CRP и / или креатинин в норме или повышен.
-
Неясные случаи: уровни ферритина нормальные или повышенные, TSAT <15% и повышенный CRP как индикатор APR; MCV / MCH низкий или нормальный.
Статистический анализ
Данные были в первую очередь проанализированы описательно, чтобы сделать выводы о распространенности и распределении анемий в когорте. Для оценки нормальности использовался тест Колмогорова-Смирнова, при этом нормальное распределение выражалось как среднее ± стандартное отклонение (SD), а ненормальные распределения — как медиана и межквартильный размах (IQR) (25-й и 75-й процентиль).Перекрестные таблицы использовались для сравнения и количественной оценки результатов ручного распределения и результатов TP. Индивидуальные лабораторные параметры были отображены графически с помощью диаграмм-усов. Было проведено различие между ясными случаями (ручное распределение и идентичные TP) и первично неоднозначными случаями. Для дальнейшей оценки степени, в которой лабораторный параметр может различать IDA и ACD, истинно-положительные и ложноположительные случаи были нанесены на кривые рабочих характеристик приемника (ROC).Впоследствии была рассчитана AUC, включая 95% доверительный интервал. Опять же, неясные случаи оценивались отдельно.
Результаты
С декабря 2016 года по сентябрь 2018 года общий анализ крови был определен у 70 956 пациентов. Около трети пациентов страдали анемией по критериям ВОЗ. У 2 211 из 20 589 пациентов с анемией (10,7%) дальнейшая диагностика проводилась путем определения показателей сывороточного железа; у 895 из этих пациентов была запрошена TP.Пациенты без анемии получили дальнейшую диагностику в 1534 из 50 367 случаев (3%). В целом, 3745 пациентов с определением параметров железа, в том числе 1721 пациент с TP, могли быть включены в дальнейшую оценку. Средний возраст этих пациентов составлял 71 год (IQR 55–79, диапазон 18–105 лет), из них 48% мужчин и 52% женщин.
Примерно в 80% случаев нефрологическая практика и отделения внутренней медицины, включая отделение неотложной помощи, инициировали дальнейшую диагностику анемии.На нефрологическую практику приходится наибольшая доля всех ТП (около 70%), за ней следуют отделения внутренней медицины (28%). В других ведомствах ТП запрашивалась только спорадически.
Согласно ручной классификации ACD была наиболее частой причиной анемии с 16%, за ней следовала ЖДА с 10%. ACD с подозрением на FID было очень редко — 0,3%. Однако на данном этапе анализа было невозможно определить, сколько случаев могло быть упущено из виду, исходя из обычных параметров железа.В 764 из 3745 случаев (20,4%) четкое распределение на основе обычных параметров железа было невозможно. В 294 из этих 764 случаев (38,5%) дальнейшая дифференциация была инициирована с помощью TP. У 30% пациентов не было анемии, и около 20% случаев пришлось исключить. В основном это произошло из-за отклонений от нормы лабораторных показателей, которые нельзя было интерпретировать без дополнительной клинической информации. Таким образом, количество ТЦ, подлежащих оценке, уменьшилось с 1721 до 1459 (Таблица 2).
Таблица 2:
Результаты ручной классификации на основе общепринятых параметров железа (левые столбцы: абсолютное число [n] и процент [%], правые столбцы — количество пациентов с ТП).
| Ручная классификация на основе стандартных параметров железа | Всего | Томас-участок осуществлен | ||
|---|---|---|---|---|
| n | % | Да, | Нет, | |
| n | n | |||
| IDA | 356 | 9.5 | 127 | 229 |
| Скрытый идентификатор | 82 | 2,2 | 46 | 36 |
| ACD | 617 | 16,5 | 377 | 240 |
| FID / ACD | 12 | 0,3 | 9 | 3 |
| Нет анемии | 1 123 | 30.0 | 606 | 517 |
| Неоднозначное | 764 | 20,4 | 294 | 470 |
| Исключено | 791 | 21,1 | – | – |
| Итого | 3,745 | 100 | 1,459 | |
Все протестированные лабораторные параметры показали ненормальное распределение.Отдельные результаты, разделенные на категории анемии на основе ручного распределения и скрытые для параметров TP, представлены в таблице 3. Особый интерес вызвали характеристики неоднозначных случаев. Это были пациенты с анемией (медиана Hb 10,2 г / дл, IQR 8,9–11,7) с нормоцитарной (медиана MCV 83,5 мкл, IQR 79,3–87,9), довольно гипохромной (медиана MCH 27,6 пг, IQR 26,0–29,3) анемией. Ферритин был в пределах нормы или слегка повышен (в среднем 188 нг / мл; IQR 47,25–252), TSAT был снижен или находился в низко-нормальном диапазоне (медиана 14.5%; IQR 10.1–21.2). Однако оба параметра оказались бесполезными из-за дополнительных воспалительных состояний (среднее значение СРБ 30 мг / л; IQR 8,8–82,1).
Таблица 3:
Обзор протестированных лабораторных параметров, разделенных в соответствии с ручной классификацией по категориям анемии, слепым для Ret-H e и sTfR.
| Hb, г / дл | Эритроциты, × 10 12 / л | MCV, фЛ | CRP, нг / мл | Ферритин, нг / мл | Трансферрин, мг / дл | TSAT,% | sTfR, нмоль / л | Ферритиновый индекс, sTfR / log ферритина | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Медиана | Pct | Медиана | Pct | Медиана | Pct | Медиана | Pct | Медиана | Pct | Медиана | Pct | Медиана | Pct | Медиана | Pct | Медиана | Pct | |
| МАР
n = 67 |
10.0 | 8,3
10,9 |
4,0 | 3,5
4,4 |
77,5 | 72,1
83,1 |
3,7 | 1,3
7,4 |
10,5 | 6,5
17,3 |
304,0 | 265,0
343,0 |
7,02 | 4,27
10,85 |
34,07 | 26.12
44,94 |
32,84 | 22,88
52,30 |
| ACD
n = 73 |
11,0 | 9,8
11,7 |
3,7 | 3,3
3,9 |
89,7 | 86,3
93,3 |
5,7 | 1,9
18,4 |
129,0 | 58,8
306,0 |
192 | 154.0
230,0 |
25,8 | 20,90
32,50 |
17,06 | 14,17
20,93 |
8,66 | 6,65
11,24 |
| Функциональный идентификатор / ACD
n = 12 |
10,1 | 8,5
11,1 |
3,7 | 3,1
4,7 |
87,1 | 75,0
89.8 |
4,0 | 1,8
7,2 |
36,2 | 29,9
77,2 |
237 | 219,0
315,0 |
12,2 | 7,87
14,05 |
21,62 | 19,74
25,33 |
13,31 | 10,79
17,82 |
| Скрытый идентификатор
n = 82 |
13.1 | 12,5
13,9 |
4,7 | 4,4
4,9 |
84,9 | 82,4
88,5 |
1,4 | 0,7
3,6 |
11,5 | 9,4
20,4 |
299,0 | 265,0
338,0 |
13,7 | 11,20
21,25 |
22,0 | 18.58
25,33 |
19,12 | 16,42
23,68 |
| Здоров / нет анемии
n = 1123 |
13,9 | 13,2
14,9 |
4,7 | 4,4
5,0 |
87,6 | 85,0
90,4 |
1,7 | 0,8
4,3 |
84,7 | 45,5
157.0 |
233 | 212,0
258,0 |
28,6 | 22,90
35,10 |
16,44 | 14,08
19,59 |
8,83 | 7,27
10,91 |
| Неоднозначные случаи
n = 764 |
10,2 | 8,9
11,7 |
3,8 | 3,3
4,3 |
83.5 | 79,3
87,9 |
30,1 | 8,8
82,1 |
108,0 | 47,45
252,0 |
194 | 153,0
236,0 |
14,5 | 10,10
21,20 |
22,49 | 17,55
30,34 |
12,15 | 8,62
17,41 |
| Исключено
n = 791 |
10.6 | 8,7
12,9 |
3,6 | 3,0
4,3 |
89,7 | 84,3
95,6 |
8,2 | 2,3
34,5 |
197,0 | 76,2
468,0 |
179 | 137,0
222,0 |
33,2 | 18,60
56,70 |
17,46 | 13.28
25,21 |
8,23 | 5,74
11,62 |
После классификации на основе обычных параметров железа все 1459 случаев были отнесены к квадранту в TP с использованием индекса ферритина и RET-H e (рис. 2).
Рисунок 2:
Томас-сюжет всего 1459 дел. Пороговое значение для индекса ферритина: 14, пороговое значение для RET-H и : 28 пг.Квадрант вверху слева: ACD, квадрант вверху справа: скрытый ID, квадрант внизу справа: IDA, квадрант внизу слева: FID / ACD.
Перекрестная таблица использовалась для сравнения результатов ручной классификации и классификации на основе алгоритмов (таблица 4). В 1 014 из 1459 случаев (около 70%) ручное распределение было идентично TP. За исключением 294 случаев (20%), которые нельзя было четко классифицировать вручную, оставшиеся 151 случай (10%) не попали в ту же категорию.
Таблица 4:
Перекрестная таблица, сравнивающая ручную и автоматическую классификацию на основе TP.
| Ручная классификация на основе обычных параметров железа | Классификация на основе графика Томаса | ||||
|---|---|---|---|---|---|
| IDA | Скрытый идентификатор | ACD / без анемии | FID / ACD | Всего | |
| IDA | 77 | 50 | 0 | 0 | 127 |
| Скрытый идентификатор | 5 | 39 | 2 | 0 | 46 |
| ACD | 1 | 35 | 341 | 0 | 377 |
| FID / ACD | 0 | 5 | 1 | 3 | 9 |
| Нет анемии | 0 | 52 | 554 | 0 | 606 |
| Неоднозначное | 43 | 80 | 142 | 29 | 294 |
| Итого | 126 | 261 | 1040 | 32 | 1459 |
После применения TP к неоднозначным 294 случаям ACD был обнаружен в 142 случаях (48.3%), латентный ID в 80 случаях (27,2%), IDA в 43 случаях (14,6%) и FID / ACD в 29 случаях (10%).
Графики
«прямоугольные усы» использовались для иллюстрации различных значений четырех категорий анемии для ферритина, TSAT, sTfR и индекса ферритина (рис. 3A – H). В то время как значения ферритина, как и ожидалось, были ниже в контексте дефицита железа (A), значения в неясных случаях почти всегда были в пределах нормы или даже были повышены (B). Следовательно, значение ферритина не позволяло надежно отнести к категории анемии из-за больших диапазонов и, как следствие, совпадений.В то время как TSAT с нормальным CRP различались между состояниями дефицита железа и ACD (C), различия исчезли во всех категориях во время APR (D). Распределение медиан и IQR sTfR было одинаковым в обеих группах; повышен при дефиците железа и в пределах нормы при ACD (E, F). Не было совпадений в диапазоне IQR внутри категорий, независимо от наличия APR. Для того, чтобы надежно различать IDA и ACD, индекс ферритина был использован в качестве «золотого стандарта» в настоящем исследовании.Следовательно, в этом отношении существовали четкие различия между состояниями дефицита железа и ACD (G, H).
Рисунок 3:
Графики Box – Whisker, представляющие различные значения ферритина, TSAT, sTfR и индекса ферритина в четырех категориях анемии. Различие между ясными случаями (ручное назначение и TP идентично) (левая панель: A, C, E, G) и неоднозначными случаями (правая панель: B, D, F, H). Прямоугольники представляют 25-й и 75-й процентили, усы — 5-й и 95-й процентили.Обратите внимание на логарифмическую шкалу для ферритина и индекса ферритина.
AUC показали, что индекс ферритина показал самую высокую диагностическую точность (AUC 0,969) в чистых случаях, за ним следовали концентрация ферритина (AUC 0,958) и TSAT (AUC 0,931). Однако в неопределенных случаях ферритин (AUC 0,691) и TSAT (AUC 0,628) играли лишь второстепенную роль. Диагностическая точность других параметров (трансферрин, железо, MCV, MCH) была низкой в обоих случаях. Напротив, RET-H e (AUC 0.957) стал более значимым в группе неоднозначных случаев. Вместе с индексом ферритина (AUC 0,917) оба показали самую высокую диагностическую точность для отличия IDA от ACD во время APR. Диагностическая точность sTfR (AUC 0,88 и 0,9) была одинаковой в обеих группах (таблица 5).
Таблица 5:
AUC и 95% -ный ДИ отдельных лабораторных параметров для различения IDA и ACD, разделенных на ясные (ручная классификация и TP идентичны) и неоднозначные случаи.
| Ящики | Неоднозначные случаи | |||
|---|---|---|---|---|
| AUC | 95% -CI | AUC | 95% -CI | |
| sTfR / лог ферритин | 0.969 | 0,96–0,979 | 0,917 | 0,882–0,951 |
| Ферритин | 0,958 | 0,948–0,969 | 0,691 | 0,600–0,782 |
| TSAT | 0,931 | 0,912–0,949 | 0,628 | 0,513–0,742 |
| СТФР | 0,884 | 0.858–0,911 | 0,897 | 0,860–0,933 |
| RET-H e | 0,883 | 0,859–0,908 | 0,957 | 0,933–0,982 |
| Трансферрин | 0,856 | 0,823–0,889 | 0,571 | 0,469–0,673 |
| Сыворотка железа | 0,852 | 0.825–0,878 | 0,596 | 0,481–0,711 |
| МСН | 0,831 | 0,8–0,863 | 0,711 | 0,603–0,819 |
| MCV | 0,83 | 0,797–0,862 | 0,67 | 0,56–0,781 |
Обсуждение
Целью этого исследования было ретроспективно оценить диагностику анемии с использованием обычных параметров железа и новых гематологических маркеров, в частности TP.Для этой цели представлялась подходящей оценка рутинной лабораторной диагностики в больнице с максимальным уходом в течение 20 месяцев. Из-за ретроспективного дизайна этого исследования его возможности могут быть ограничены неоднородным временем сбора, особенно TSAT, поскольку на расчет влияют пищевые и циркадные колебания сывороточного железа [19].
Классификация причин анемии была произведена одним экспертом по аналогии с другими исследованиями с различной степенью определения различных когорт [20].Как и в других исследованиях, наша классификация основана на заранее определенных критериях включения и исключения с четкими пороговыми значениями [21], [22]. Такой подход казался наиболее подходящим для оптимизации объективности. Некоторые авторы настаивают на сравнении со статусом железа в костном мозге как на золотом стандарте для оценки параметров железа [23]. Однако исследования с таким сравнением смогли включить максимальное количество случаев 176 пациентов только из-за инвазивности и стоимости [24].Кроме того, неоднократно критиковалось, что даже определение статуса железа в мазке из костного мозга, окрашенном берлинским синим, в значительной степени зависит от исследователя и, следовательно, не является объективным [23], [25]. В исследовании, сопоставимом с представленным здесь, классификация пациентов проводилась двумя независимыми исследователями с целью повышения объективности без окрашивания костного мозга [26]. Тем не менее, оставалось неясным, какие критерии использовались в качестве основы для их оценки.
Как и в литературе, наиболее частой причиной анемии в клинических условиях была ACD, за которой следовала ЖДА [3].Доля пациентов с анемией с ACD и FID (квадрант 4) была очень редкой — всего 32 случая (4%), тогда как в других исследованиях эта доля составляла ~ 10% [26] или 20% [27]. Это может быть связано с предвзятостью в отношении высокой доли нефрологических пациентов, а также с неполным диагнозом в 470 других неоднозначных случаях. В 29 из 294 неопределенных случаев (10%) ACD с FID не было бы замечено без TP. Если предположить, что в других неясных случаях еще приблизительно 10% не были обнаружены, ожидаемая доля будет составлять около 50 дополнительных случаев с ACD и FID.
Хотя при запросе данных было получено множество наборов данных, только в 10,7% случаев анемии требовалась дальнейшая и полная диагностика метаболизма железа. Причины низкой диагностики остаются неясными. В некоторых случаях это может быть связано с тем, что легкая анемия (Hb 10–12 г / дл) без клинических симптомов допустима, особенно у пожилых пациентов [28]. В других случаях причина анемии могла быть уже известна или диагностическое исследование анемии не относилось к соответствующей медицинской специальности.В то время как диагностика анемии в значительной степени ограничивалась областью внутренней медицины, доля ТП, выполненных только нефрологической практикой, составляла 70%. Следовательно, значение результатов, относящихся к общеклинической полезности TP, ограничено. Доля ТП, проведенных онкологическим (1%) и ревматологическим больным (7%), была крайне низкой. Особенно в отношении ожидаемого ACD с дополнительным FID около 20% [9], было бы желательно более высокое соотношение этих групп пациентов.В последние годы критикуется частое переливание концентратов эритроцитов и, в свою очередь, довольно ограниченное использование ЭСС и внутривенного железа у онкологических пациентов. Вероятно, это частично связано с диагностической неопределенностью. Международные руководящие принципы поддерживают использование ESA у пациентов с опухолями, проходящих химиотерапию [29], [30]. Более частое применение TP может привести к более эффективной диагностике и лечению, но необходимы дальнейшие исследования с акцентом на этих группах пациентов.
TP уже обсуждался как золотой стандарт диагностики сложных железных анемий [31]. Однако стандартизация аналитических методов все еще продолжается и гарантирует использование пороговых значений для конкретных методов для классификации. Введение рекомбинантного эталонного стандарта ВОЗ для sTfR повысило бы диагностическую ценность sTfR и, следовательно, индекса ферритина [32]. Гемоглобин ретикулоцитов можно оценить по двум различным принципам (CHr и RET-H e ), что добавляет еще одну неопределенность к классификации [33].
Определение только RET-H e у пациентов, находящихся на диализе, может снизить использование внутривенного железа по сравнению с определением только ферритина и TSAT [34]. Тем не менее, 791 пациент был исключен из дальнейшей оценки в нашем исследовании, потому что общий решающий фактор в оценке метаболизма железа — это не изолированное рассмотрение лабораторных показателей, а включение всей клинической информации о диагнозах и предыдущих методах лечения.
В заключение, в большинстве случаев обычные параметры железа оказываются достаточно эффективными в повседневной клинической практике для диагностики состояний дефицита железа (70% идентичное распределение).Тем не менее, по крайней мере, в 20% случаев TP оказался полезным для сужения причин анемии в сложных случаях. У 10% наших пациентов он предоставил дополнительную информацию с медицинскими последствиями. Дальнейшие исследования с упором на особые группы пациентов с риском дефицита железа, например желательны онкологические или ревматические пациенты.
Список литературы
1. Онкопедия. Onkopedia leitlinien. Eisenmangel und Eisenmangelanämie 2018. Доступно по адресу: https://www.onkopedia.com/de/onkopedia/guidelines/eisenmangel-und-eisenmangelanaemie/@@view/html/index.html. [Доступ 1 сентября 2019 г.]. Искать в Google Scholar
2. Камашелла, С. Железодефицитная анемия. N Engl J Med 2015; 372: 1832–43. https://doi.org/10.1056/nejmra1401038. Искать в Google Scholar
3. Weiss, G, Goodnough, LT. Анемия хронического заболевания. N Engl J Med 2005; 352: 1011–23. https://doi.org/10.1056/nejmra041809. Искать в Google Scholar
4. Ганц, Т., Немет, Э. Гепсидин и гомеостаз железа. Biochim Biophys Acta 2012; 1823: 1434–43.https://doi.org/10.1016/j.bbamcr.2012.01.014. Искать в Google Scholar
5. Ла Ферла, К., Рейманн, К., Йелкманн, В., Хелвиг-Бургель, Т. Ингибирование передачи сигналов экспрессии гена эритропоэтина включает факторы транскрипции gata-2 и nf-kappab. FASEB J 2002; 16: 1811–3. https://doi.org/10.1096/fj.02-0168fje. Искать в Google Scholar
6. Каццола, М., Пончио, Л, де Бенедетти, Ф, Равелли, А, Рости, В, Бегин, Й и др. Недостаток железа для эритропоэза и адекватная выработка эндогенного эритропоэтина при анемии, связанной с системным юношеским хроническим артритом. Кровь 1996; 87: 4824–30. https://doi.org/10.1182/blood.v87.11.4824.bloodjournal87114824. Искать в Google Scholar
7. Пападаки, HA, Kritikos, HD, Valatas, V, Boumpas, DT, Eliopoulos, GD. Анемия хронического заболевания при ревматоидном артрите связана с повышенным апоптозом эритроидных клеток костного мозга: улучшение после терапии антителами против фактора некроза опухоли альфа. Кровь 2002; 100: 474–82. https://doi.org/10.1182/blood-2002-01-0136. Искать в Google Scholar
8.Weiss, G, Ganz, T, Goodnough, LT. Анемия воспаления. Кровь 2019; 133: 40–50. https://doi.org/10.1182/blood-2018-06-856500. Искать в Google Scholar
9. Thomas, L, Thomas, C, Heimpel, H. Neue Parameter zur Diagnostik von Eisenmangelzuständen: retikulozytenhämoglobin und löslicher Transferrinrezeptor. Dtsch Ärztebl 2005; 102: A 580–6. Ищите в Google Scholar
10. Камашелла, К. Новое понимание железодефицитной и железодефицитной анемии. Blood Rev. 2017; 31: 225–33.https://doi.org/10.1016/j.blre.2017.02.004. Искать в Google Scholar
11. Thomas, C, Kirschbaum, A, Boehm, D, Thomas, L. Диагностический сюжет. Med Oncol 2006; 23: 23–36. https://doi.org/10.1385/mo:23:1:23. Искать в Google Scholar
12. Мукенталер, М.Ю., Ривелла, С., Хентце, М.В., Гали, Б. Красная дорожка метаболизма железа. Cell 2017; 168: 344–61. https://doi.org/10.1016/j.cell.2016.12.034. Искать в Google Scholar
13. Cleland, JG, Zhang, J, Pellicori, P, Dicken, B, Dierckx, R, Shoaib, A, et al.Распространенность и исходы анемии и гематиновой недостаточности у пациентов с хронической сердечной недостаточностью. JAMA Cardiol 2016; 1: 539–47. https://doi.org/10.1001/jamacardio.2016.1161. Искать в Google Scholar
14. Анкер, С.Д., Комин Колет, Дж., Филиппатос, Г., Вилленхеймер, Р., Дикштейн, К., Дрекслер, Х, и др. Карбоксимальтоза железа у пациентов с сердечной недостаточностью и дефицитом железа. N Engl J Med 2009; 361: 2436–48. https://doi.org/10.1056/nejmoa0
5. Искать в Google Scholar
15.Haddad, S, Wang, Y, Galy, B, Korf-Klingebiel, M, Hirsch, V, Baru, AM, et al. Белки, регулирующие железо, обеспечивают доступность железа в кардиомиоцитах для предотвращения сердечной недостаточности. Eur Heart J 2017; 38: 362–72. https://doi.org/10.1093/eurheartj/ehw333. Искать в Google Scholar
16. Каппеллини, доктор медицины, Комин-Колет, Дж., Де Франсиско, А., Дигнасс, А., Дохнер, В., Лам, К.С. и др. Дефицит железа при хронических воспалительных состояниях: мнение международных экспертов по определению, диагностике и лечению. Am J Hematol 2017; 92: 1068–78. https://doi.org/10.1002/ajh.24820. Искать в Google Scholar
17. Пуннонен, К., Ирьяла, К., Раджамаки, А. Рецептор трансферрина сыворотки и его соотношение к ферритину сыворотки при диагностике дефицита железа. Кровь 1997; 89: 1052–7. https://doi.org/10.1182/blood.v89.3.1052. Искать в Google Scholar
18. Всемирная организация здравоохранения. Концентрации гемоглобина для диагностики анемии и оценки степени тяжести 2011 г. Доступно по адресу: https: // www.who.int/vmnis/indicators/haemoglobin/en/. [Доступ 31 августа 2019 г.]. Искать в Google Scholar
19. Heimpel, H, Riedel, M, Wennauer, R, Thomas, L. Die Plasmaisenbestimmung — nützlich, unnötig oder irführend? Мед Клин 2003; 98: 104–7. https://doi.org/10.1007/s00063-003-1234-4. Поиск в Google Scholar
20. Скикне, Б.С., Пуннонен, К., Калдрон, П.Х., Беннет, М.Т., Реху, М., Гасиор, Г.Х. и др. Улучшенная дифференциальная диагностика анемии хронического заболевания и железодефицитной анемии: проспективная многоцентровая оценка растворимого рецептора трансферрина и индекса ферритина stfr / log. Am J Hematol 2011; 86: 923-7. https://doi.org/10.1002/ajh.22108. Искать в Google Scholar
21. Shin, DH, Kim, HS, Park, MJ, Suh, IB, Shin, KS. Полезность доступа к растворимому рецептору трансферрина (stfr) и индекс ферритина stfr / log в диагностике железодефицитной анемии. Ann Clin Lab Sci 2015; 45: 396–402. Искать в Google Scholar
22. Suega, K, Kandarini, Y, Tubung, J. Роль растворимого рецептора трансферрина и индекса ферритина рецептора трансферрина в выявлении железодефицитной анемии у пациентов, регулярно находящихся на гемодиализе. Открытый доступ Maced J Med Sci 2019; 7: 97–102. https://doi.org/10.3889/oamjms.2019.012. Искать в Google Scholar
23. Braga, F, Infusino, I, Dolci, A, Panteghini, M. Растворимые рецепторы трансферрина при осложненной анемии. Clin Chim Acta 2014; 431: 143–7. https://doi.org/10.1016/j.cca.2014.02.005. Искать в Google Scholar
24. Ханиф, Э, Айюб, М., Анвар, М., Али, В., Башир, М. Оценка концентрации рецепторов трансферрина в сыворотке при диагностике и дифференциации железодефицитной анемии от анемии хронических заболеваний. J Pakistan Med Assoc 2005; 55: 13–6. Искать в Google Scholar
25. Кулаузидис, А., Саид, Э, Коттье, Р., Саид, А.А. Растворимые рецепторы трансферрина и дефицит железа — шаг за пределы ферритина. Систематический обзор. J Gastrointestin Liver Dis 2009; 18: 345–52. Искать в Google Scholar
26. Леерс, М. П., Керен, Дж. Ф., Остерхейс, В. П.. Значение диаграммы Томаса в диагностике пациентов с анемией, направленных врачами общей практики. Int J Lab Hematol 2010; 32: 572–81.https://doi.org/10.1111/j.1751-553x.2010.01221.x. Искать в Google Scholar
27. Thomas, C, Thomas, L. Биохимические маркеры и гематологические показатели в диагностике функционального дефицита железа. Clin Chem 2002; 48: 1066–76. https://doi.org/10.1093/clinchem/48.7.1066. Поиск в Google Scholar
28. Людвиг, Х., Ван Белль, С., Барретт-Ли, П., Биргегард, Г., Бокемейер, К., Гаскон, П. и др. Европейское обследование онкологической анемии (ecas): крупное многонациональное проспективное обследование, определяющее распространенность, заболеваемость и лечение анемии у онкологических больных. Eur J Canc 2004; 40: 2293–306. https://doi.org/10.1016/j.ejca.2004.06.019. Искать в Google Scholar
29. Bohlius, J, Bohlke, K, Castelli, R, Djulbegovic, B, Lustberg, MB, Martino, M, et al. Управление канцерогенной анемией с помощью средств, стимулирующих эритропоэз: обновление руководства по клинической практике asco / ash. J Clin Oncol 2019; 37: 1336–51. https://doi.org/10.1200/jco.18.02142. Искать в Google Scholar
30. Аапро, М., Бегин, Й, Бокемейер, К., Дикато, М., Гаскон, П., Гласпи, Дж. И др.Управление анемией и дефицитом железа у онкологических больных: руководство по клинической практике ESMO. Энн Онкол 2018; 29: iv96–110. https://doi.org/10.1093/annonc/mdx758. Искать в Google Scholar
31. Бругнара, К. Гематологический «золотой стандарт» для состояний дефицита железа? Clin Chem 2002; 48: 981–2. https://doi.org/10.1093/clinchem/48.7.981. Поиск в Google Scholar
32. Хармс, К., Кайзер, Т. За пределами растворимого рецептора трансферрина: старые проблемы и новые горизонты. Best Practices Clin Endocrinol Metabol 2015; 29: 799–810. https://doi.org/10.1016/j.beem.2015.09.003. Искать в Google Scholar
33. Бругнара, С., Шиллер, Б., Моран, Дж. Ретикулоцитарный эквивалент гемоглобина (ret he) и оценка состояний дефицита железа. Clin Lab Haematol 2006; 28: 303–8. https://doi.org/10.1111/j.1365-2257.2006.00812.x. Искать в Google Scholar
34. Fishbane, S, Shapiro, W, Dutka, P, Valenzuela, OF, Faubert, J. Рандомизированное испытание стратегий тестирования дефицита железа у пациентов, находящихся на гемодиализе. Kidney Int 2001; 60: 2406–11. https://doi.org/10.1046/j.1523-1755.2001.00077.x. Искать в Google Scholar
Поступила: 2020-05-23
Принято: 18.06.2020
Опубликовано в сети: 07.08.2020
Опубликовано в печати: 25.09.2020
© 2020 Meiser Daniela et al., Опубликовано De Gruyter, Берлин / Бостон
Это произведение находится под лицензией Creative Commons Attribution 4.0 Международная лицензия.
(PDF) Скрытый дефицит железа как маркер негативных симптомов у пациентов с первым эпизодом расстройства шизофренического спектра
Nutrients 2018,10, 1707 10 из 11
37.
Schimmelmann, B.G .; Huber, C.G .; Lambert, M .; Хлопок, S .; McGorry, P.D .; Conus, P. Влияние продолжительности
нелеченого психоза на характеристики до лечения, исходных данных и исходов в эпидемиологической когорте
психозов с первым эпизодом.J. Psychiatr. Res. 2008, 42, 982–990. [CrossRef] [PubMed]
38.
Kay, S.R .; Fiszbein, A .; Оплер, Л.А. Шкала позитивных и негативных синдромов (PANSS) для шизофрении.
Schizophr. Бык. 1987, 13, 261–276. [CrossRef] [PubMed]
39.
Yi, J.S .; Ahn, Y.M .; Шин, Х.К .; Ан, С.К .; Joo, Y.H .; Kim, S.H .; Юн, Д.Дж .; Jho, K.H .; Koo, Y.J .; Ли, Дж.
Надежность и валидность корейской версии шкалы положительных и отрицательных синдромов.J. Korean
Neuropsychiatr. Доц. 2001,40, 1090–1105.
40.
Emsley, R .; Rabinowitz, J .; Торреман, М. Факторная структура шкалы положительных и отрицательных синдромов
(PANSS) при недавно начавшемся психозе. Schizophr. Res. 2003,61, 47–57. [CrossRef]
41.
Addington, D .; Addington, J .; Шиссель, Б. Шкала оценки депрессии для шизофреников. Schizophr. Res.
1990,3, 247–251. [CrossRef]
42.
Ким, С.W .; Kim, S.J .; Yoon, B.H .; Kim, J.M .; Shin, I.S .; Hwang, M.Y .; Юн, Дж. Диагностическая валидность
шкал оценки депрессии у больных шизофренией. Psychiatry Res.
2006
, 144, 57–63. [CrossRef]
[PubMed]
43.
Американская психиатрическая ассоциация. Диагностическое и статистическое руководство по психическим расстройствам-IV-TR;
Американская психиатрическая ассоциация: Вашингтон, округ Колумбия, США, 2000.
44.
Джон М.; Ю, Т .; Lee, J.Y .; Kim, S.Y .; Kim, J.M .; Shin, I.S .; Уильямс, L .; Берк, М .; Yoon, J.S .; Ким, С.
Гендерные факторы риска низкой минеральной плотности костей у пациентов, принимающих антипсихотические препараты от психоза.
Hum. Psychopharmacol. 2018,33. [CrossRef] [PubMed]
45.
Bakerman, S .; Bakerman, P .; Strausbauch, Азбука интерпретации лабораторных данных П. Бакермана, 4-е изд .;
Interpretive Laboratory Data, Inc .: Скоттсдейл, Аризона, США, 2002; п. 243.
46.
Leonard, A.J .; Chalmers, K.A .; Collins, C.E .; Паттерсон, А.Дж. Исследование влияния латентного дефицита железа
на когнитивные способности: пилотное рандомизированное контролируемое исследование приема добавок железа у молодых женщин.
Питательные вещества 2014,6, 2419–2435. [CrossRef] [PubMed]
47.
Youdim, M.B. Дефицит и избыток мозгового железа; когнитивные нарушения и нейродегенерация с вовлечением
полосатого тела и гиппокампа. Нейротокс.Res. 2008 г., 14, 45–56. [CrossRef] [PubMed]
48.
Ben-Shachar, D .; Finberg, J.P .; Юдим, М. Влияние хелаторов железа на рецепторы дофамина D2. J. Neurochem.
1985,45, 999–1005. [CrossRef] [PubMed]
49.
Ben-Shachar, D .; Юдим, М. Сверхчувствительность, индуцированная нейролептиками, и железо в головном мозге: I. Дефицит железа и сверхчувствительность рецептора допамина D2, индуцированная нейролептиком
. J. Neurochem.
1990
, 54, 1136–1141.[CrossRef]
[PubMed]
50.
Pino, J.M.V .; да Луз, M.H.M .; Antunes, H.K.M .; Giampa, S.Q.C .; Мартинс, В.Р .; Ли, К.С. Диета с ограничением железа
влияет на уровень ферритина в мозге, метаболизм дофамина и клеточный прионный белок в зависимости от региона.
Перед. Мол. Neurosci. 2017,10, 145. [CrossRef] [PubMed]
51.
Brunelin, J .; Fecteau, S .; Суод-Шаньи, М.Ф. Аномальная передача дофамина в полосатом теле при шизофрении.
Curr.Med. Chem. 2013,20, 397–404. [PubMed]
52.
Nemeth, E .; Rivera, S .; Габаян, В .; Keller, C .; Taudorf, S .; Pedersen, B.K .; Ganz, T. IL-6 опосредует
гипоферремию воспаления, индуцируя синтез регуляторного гормона железа гепсидина.
J. Clin. Расследование. 2004, 113, 1271–1276. [CrossRef] [PubMed]
53.
Brown, A.S .; Деркиц, Э. Пренатальная инфекция и шизофрения: обзор эпидемиологических и трансляционных исследований
.Являюсь. J. Psychiatry 2010, 167, 261–280. [CrossRef] [PubMed]
54.
Corwin, E.J .; Мюррей-Колб, L.E .; Бирд, Дж. Л. Низкий уровень гемоглобина является фактором риска послеродовой депрессии.
J. Nutr. 2003, 133, 4139–4142. [CrossRef] [PubMed]
55.
Vahdat Shariatpanaahi, M .; Вахдат Шариатпанаахи, З .; Моштааги, М .; Shahbaazi, S.H .; Abadi, A.
Взаимосвязь между депрессией и уровнем ферритина в сыворотке. Евро. J. Clin. Nutr.
2007
, 61, 532–535.[CrossRef]
[PubMed]
56.
Stewart, R .; Хирани, В. Взаимосвязь между депрессивными симптомами, анемией и статусом железа у пожилых людей
из национального опроса населения. Психосом. Med. 2012,74, 208–213. [CrossRef] [PubMed]
57.
Shoja Shafti, S .; Джафарабад, M.S .; Азизи, Р. Уменьшение синдрома дефицита шизофрении с помощью ингибитора обратного захвата норэпинефрина
. Ther. Adv. Psychopharmacol. 2015,5, 263–270. [CrossRef] [PubMed]
58.
Arango, C .; Гарибальди, G .; Мардер, С. Фармакологические подходы к лечению негативных симптомов: обзор
клинических испытаний. Schizophr. Res. 2013, 150, 346–352. [CrossRef] [PubMed]
Железодефицитная анемия: современные стратегии диагностики и лечения | Кая
отзывов в здравоохранении, 2013 г .; 4 (3): 193-202
Гематология
Повествовательный обзор
Железодефицитная анемия: современные стратегии диагностики и лечения
Zühre Kaya 1
1 Отделение детской гематологии отделения педиатрии Медицинской школы Университета Гази, Анкара, Турция
Аннотация
Дефицит железа — один из самых распространенных недостатков пищевых продуктов в мире.Это многофакторное заболевание, которое может быть вызвано недостаточным потреблением пищи, потерей крови и кишечными причинами. Клинические особенности сильно различаются, и у большинства пациентов симптомы отсутствуют. Типичные лабораторные признаки железодефицитной анемии (ЖДА) включают гипохромную микроцитарную анемию, низкий уровень сывороточного железа, высокую общую железосвязывающую способность, низкий уровень сывороточного ферритина. Полезность мониторинга уровня рецепторов трансферрина в сыворотке (sTfR) и гепсидина для выявления ЖДА изучалась в нескольких исследованиях. Имеющиеся данные предполагают, что sTfR потенциально может стать ценным инструментом для регулярного тестирования пациентов в будущем.Несмотря на то, что ЖДА легко корректируется с помощью терапии железом, установить причину может быть сложно, особенно в случаях, вызванных нарушением транспорта железа. Обучение клиницистов должно быть сосредоточено на повышении осведомленности о важности отсутствия реакции на добавки железа. Целью этого обзора было обрисовать текущие стратегии диагностики и лечения ЖДА в свете последних отчетов.
Ключевые слова
Железодефицитная анемия, гомеостаз, добавки железа
Автор, ответственный за переписку
Zühre Kaya, MD
Отделение детской гематологии педиатрического отделения
Медицинская школа Университета Гази, Бешевлер, Анкара, Турция, 06500
e-mail: zuhrekaya @ gazi.edu.tr
Раскрытие информации
Автор заявляет об отсутствии конфликта интересов
Введение
Дефицит железа по-прежнему является наиболее частым дефицитом питания во всем мире [1,2]. Дефицит железа может поражать все возрастные группы, но наибольшему риску подвержены младенцы и маленькие дети, особенно в развивающихся странах. Железодефицитная анемия (ЖДА) часто встречается у детей раннего возраста и беременных женщин с распространенностью от 15% до 40%, согласно различным исследованиям и используемым определениям [1-5].Согласно отчету Всемирной организации здравоохранения, на железодефицитную анемию приходится примерно 50% всех случаев анемии [1].
В этом обзоре обобщены текущие знания о ЖДА, с особым вниманием к метаболизму железа в отношении его патогенеза и клинических особенностей, а также его диагностики и лечения.
Метаболизм и гомеостаз железа
Рисунок 1. Метаболизм и гомеостаз железа
Наибольшее количество диетического железа содержится в продуктах питания животного происхождения, включая красное мясо, рыбу и молочные продукты.Среднесуточная доза железа у здорового человека составляет 1-2 мг. Пищевое железо может существовать либо в органическом, либо в гемовом железе в виде растворимой двухвалентной формы (восстановленное Fe ++), которое содержится в животных источниках, или неорганическом или негемовом железе в виде нерастворимой трехвалентной формы (окисленное Fe +++), которая содержится в растительных источниках [6 -10].
Поглощение пищевого железа энтероцитами — сложный процесс (рис. 1).
Вкратце, пищевое двухвалентное железо поглощается непосредственно с апикальной поверхности энтероцита в цитоплазму белком DMT-1 (переносчик двухвалентных металлов) [11].Однако негемовое железо не распознается этими белками напрямую. Он должен быть восстановлен до двухвалентной формы с помощью трехвалентной редуктазы, а затем связывается с рецепторами DMT-1 в апикальной щеточной кайме энтероцитов до всасывания в двенадцатиперстной кишке. Внутриклеточное двухвалентное железо может либо храниться в виде ферритина, либо экспортироваться через базолатеральную поверхность энтероцитов в кровоток с помощью ферропортина. Перед высвобождением из энтероцита он должен быть окислен до трехвалентной формы феррооксидазой. В кровотоке трехвалентное железо осуществляется трансферрином, который способствует усвоению клеточного железа за счет взаимодействия со специфическими мембранными рецепторами трансферрина (sTfR).Примерно 80% sTfR находятся в предшественниках эритроидов в костном мозге. Железо является важным элементом, который функционирует как основной компонент (около 70%) гемоглобина, переносящего кислород, и небольшое количество окислительно-восстановительных ферментов (5%) в клеточном метаболизме, а большая часть остального (25%) хранится в виде ферритина и гемосидерина в организме. органы-мишени. Свободное железо из стареющих эритроцитов, фагоцитируемое ретикулоэндотелиальной системой, связывается с трансферрином и рециркулируется.
В этом контексте гепсидин представляет собой небольшой пептидный гормон, синтезируемый преимущественно в печени, и является ключевым регулятором системного гомеостаза железа.Гепсидин играет решающую роль в регулировании системного уровня железа, подавляя всасывание железа в кишечнике, рециркуляцию железа макрофагами и мобилизацию железа из запасов печени. На молекулярном уровне ферропортин, белок, экспортирующий железо на базолатеральной мембране энтероцитов, макрофагов и гепатоцитов, интернализируется и лизосомно разлагается под действием гепсидина. Синтез гепсидина регулируется статусом железа, гипоксией и воспалением [12-14].
Причины
Дефицит железа возникает, когда потребление с пищей не соответствует потребностям организма или когда наблюдается хроническая кровопотеря.Эти две причины вместе с мальабсорбцией составляют большинство случаев. Список всех причин ЖДА приведен в Таблице I. Вероятные причины ЖДА зависят от возраста. Распространенность ЖДА демонстрирует два пика. Первый пик наступает в младенчестве и раннем детстве из-за быстрого роста и экссудативной энтеропатии из-за коровьего молока. Второй пик наблюдается у подростков и взрослых из-за кровопотери и кишечных причин [4,5].
Потребность в железе с пищей для взрослых оценивается в 55 мг / кг и выше у младенцев и детей младшего возраста из-за их быстрого роста.Недостаточное потребление железа с пищей происходит у младенцев из-за низкой концентрации железа в молоке. Грудное молоко и коровье молоко имеют низкое содержание железа, но биодоступность железа в грудном молоке выше. Младенцы особенно предрасположены к развитию ЖДА из-за более низких запасов железа в организме, более высоких требований и уменьшения потребления из молочной диеты [15].
Во время острой кровопотери запасов железа в организме, как правило, достаточно для ускоренного эритропоэза, и последующего поглощения железа достаточно для восстановления гомеостаза железа.ЖДА развивается только в течение нескольких недель или месяцев хронической или периодической кровопотери. Причины хронической кровопотери включают чрезмерное менструальное кровотечение (меноррагию), желудочно-кишечное кровотечение (ЖКТ), гематурию и рецидивирующие носовые кровотечения. ГИС-кровотечение является результатом первичного ГИС-заболевания, включая доброкачественные или злокачественные новообразования, язвы, варикозное расширение вен пищевода, воспалительные заболевания кишечника, паразитарные инфекции, артериовенозные мальформации, безоар, лекарства, такие как нестероидные противовоспалительные агенты и стероиды. Коагулопатия, вызванная заболеваниями почек и печени, а также наследственные нарушения свертываемости крови часто связаны с ЖДА [16-19].
ЖДА может быть вызвано ятрогенным путем из-за чрезмерных флеботомий донора крови, так как регулярная сдача крови в объеме 450 мл удаляет примерно 200 мг железа из организма [20]. Наконец, сообщалось, что редкие генетические дефекты в регуляции ферропортина и гепсидина вызывают железорезистентную железодефицитную анемию (IRIDA) у людей [21].
|
Причина |
Причитается к |
|
|
Дефекты всасывания в кишечнике |
Недостаточное поглощение |
Низкая биодоступность (Heme Fe> Fe + 2> Fe + 3), антацидная терапия, дубильные вещества, фитаты, фосфаты, другие металлы (Co, Pb) |
|
Нарушение абсорбции |
Воспалительное заболевание кишечника, целиакия, постгастрэктомия, инфекция Helicobacter Pilori, длительная диарея |
|
|
Факторы питания |
Избыток коровьего молока, вегетарианская диета |
|
|
Кровопотеря |
Кишечная потеря |
Носовое кровотечение, язва, дивертикул Меккеля, энтеропатия, вызванная молоком, паразитоз, варикозное расширение вен, опухоль или полипы, воспалительное заболевание кишечника, артериовенозная мальформация, аспирин, стероид |
|
Легочная потеря |
Гемосидероз легких, туберкулез Синдром Гудпасчера, дефицит Ig A, бронхоэктазы |
|
|
Мочеполовая потеря |
Нефритический синдром (потеря трансферрина), болезнь Бергера, внутрисосудистый гемолиз (пароксизмальная ночная гемоглобинурия), менструальная потеря, опухоль, диализ |
|
|
Гепатобилиарная система |
Гематобилии |
|
|
Редкие причины |
Неадекватная презентация предшественников эритроидов |
Атрансферринемия (аутосомно-рецессивное заболевание, тяжелая гипохромная микроцитарная анемия с низким SI и SIBC), антитела к рецепторам трансферрина |
|
Аномальный внутриклеточный транспорт / утилизация |
Эритроидные дефекты транспорта железа (мутации DMT-1), дефекты синтеза гема |
|
|
Нарушения усвоения железа в кишечнике |
Железорезистентная железодефицитная анемия — IRIDA (тяжелая гипохромная микроцитарная анемия с низким SI и высоким SIBC и нормальным ферритином) |
|
|
Повышенный спрос |
Быстрый рост (низкая масса тела при рождении, недоношенность, двойня, половое созревание, беременность), цианотический врожденный порок сердца |
|
Таблица I.Причины железодефицитной анемии
Клинические особенности
Характерные клинические признаки ЖДА в гематологической, кишечной, неврологической, сердечной, мышечной и иммунологической системах обобщены в таблице II.
Существуют значительные различия в клинических проявлениях, что затрудняет раннюю диагностику. Ранняя диагностика возможна только с помощью стратегий скрининга ЖДА, позволяющих выявлять бессимптомных пациентов. Раннее выявление у детей грудного и раннего возраста важно для лечения железом, которое может привести к нормальному умственному двигательному развитию и вызвать необратимую инвалидность [22,23].Клинические и лабораторные признаки очень полиморфны и разной степени тяжести, начиная от более легких состояний, таких как бледность и изолированные аномалии микроцитоза и гипохромных эритроцитов, до тяжелых нарушений, включая нейрокогнитивные нарушения и изменения эпителия кишечника. Однако клинические признаки, вызванные исключительно анемией, не возникают до тех пор, пока анемия не станет тяжелой, и могут включать в себя вялость, снижение толерантности к физическим нагрузкам, слабость, потерю веса, задержку роста и общее недомогание. Хотя эти признаки типичны для любой анемии, развитие пика является уникальным для ЖДА.Признаки кровопотери, такие как мелена, гематурия или кровотечение из других участков, могут быть отмечены во время физического осмотра [24–29].
|
Система |
Механизм |
Клинические особенности |
|
Кишечник |
Изменения эпителия и кровотечение |
Угловой стоматит, глоссит, дисфагия, перепонка пищевода (синдром Пламмера-Винсона), койлонихия, экссудативная энтеропатия, пика (безоар), синдром мальабсорбции, мелена или гематохезия |
|
Неврологический |
Нарушение механизма нейротрансмиттера |
Снижение нейрокогнитивных функций, более низкие результаты тестов на умственное и моторное развитие по шкале Бейли, периоды задержки дыхания, летаргия, раздражительность |
|
Сердечный |
Увеличение объема плазмы |
Аритмия и систолический шум в сердце |
|
Мускулистый |
Дефицит миоглобина и цитохрома С |
Снижение толерантности к физической нагрузке, слабость, общее недомогание |
|
Иммунологический |
Нарушение лейкоцитов |
Повышенная восприимчивость к инфекции при дефиците железа |
|
Гематологический |
Снижение продукции гема, снижение количества железозависимых ферментов |
Неспецифические симптомы (бледность, слабость), спленомегалия |
Таблица II.Основные клинические проявления железодефицитной анемии
,00
Диагностика
Диагностический подход к ЖДА, включая выявление основного заболевания, вызывающего заболевание, с помощью сбора анамнеза, физического осмотра и лабораторных исследований. Следует тщательно изучить анамнез диетического питания, приема добавок железа в младенчестве и в период лактации, а также кровопотери. Стандартные лабораторные тесты для диагностики ЖДА включают общий анализ крови с количеством ретикулоцитов и мазок крови, а также уровни сывороточного железа, общую железосвязывающую способность и ферритин [30].Статус железа на разных этапах болезни обобщен в Таблице III.
|
Фазы |
Лабораторные изменения |
|
Предлатентная фаза (дефицит железа) |
|
|
Латентная фаза (дефицит железа) |
|
|
Фаза Фрэнка (железодефицитная анемия) |
|
Таблица III.Три фазы железодефицитной анемии
MCH = средний корпускулярный гемоглобин; MCHC = средняя концентрация корпускулярного гемоглобина; MCV = средний корпускулярный объем
Для подтверждения диагноза и / или исключения других причин микроцитарной анемии могут потребоваться дополнительные тесты, включая электрофорез гемоглобина, анализ мочи, анализ кала на скрытую кровь, параметры свертывания, биохимию сыворотки, эндоскопию и визуализацию брюшной полости [6-10].
Общий анализ крови и мазок крови
Анемия определяется как концентрация гемоглобина ниже нормального диапазона для возраста и пола.Показатели эритроцитов MCV (средний корпускулярный объем), MCH (средний корпускулярный гемоглобин) и MCHC (средняя концентрация корпускулярного гемоглобина) ниже нормальных значений для возраста [31]. Повышенная ширина распределения эритроцитов (RDW) полезна для отличия от малой талассемии. Морфология эритроцитов показывает гипохромный микроцитоз и анизоцитоз. Количество тромбоцитов обычно повышено, особенно у пациентов с хронической кровопотерей, в некоторых случаях превышая 1х106 / мкл. Иногда при ЖДА может развиться нейтропения из-за снижения продукции нейтрофилов.
Концентрация железа в сыворотке
Обычно он очень низкий у пациентов с ЖДА. Однако уровни сывороточного железа от умеренно низких до низких также могут наблюдаться при анемии, вызванной воспалительным заболеванием. Уровень железа в сыворотке крови может временно повышаться при внутрисосудистом лизисе эритроцитов, недавнем переливании крови и добавлении железа, что может затруднить интерпретацию лабораторных данных [32].
Общая железосвязывающая способность
Это показатель концентрации железа в плазме, которое может связываться трансферрином в плазме.Насыщение железом отражает количество железа в плазме, связанного с трансферрином, и оно низкое (<20%) в случаях ЖДА [32].
Ферритин
Уровень ферритина в сыворотке хорошо коррелирует с запасами железа в организме. Он снижается при ЖДА и увеличивается при перегрузке железом. Ферритин также является белком острой фазы, и гиперферритинемия может возникать при основном заболевании, таком как воспалительное заболевание, неоплазия, заболевания печени. Тем не менее низкие концентрации ферритина в сыворотке (<12 нг / мл) могут помочь дифференцировать ЖДА от анемии, вызванной воспалительным заболеванием [32].
Железо костного мозга
Запасы железа в организме можно качественно оценить, окрашивая костный мозг красителем берлинской лазурью. Низкое содержание железа в костном мозге — информативное, но инвазивное исследование. Таким образом, железо костного мозга остается золотым стандартом диагностики ЖДА в сложных случаях.
Уровень рецепторов трансферрина сыворотки (STfR)
Последние данные показывают, что sTfR может определять статус железа лучше, чем ранее использовавшиеся стандартные лабораторные тесты. Уровни sTfR в плазме повышаются при железодефицитной анемии.Таким образом, уровни sTfR могут быть полезным параметром для различия между анемией хронического заболевания и ЖДА, но не широко доступны [33,34].
Содержание гемоглобина в ретикулоцитах (CHr) и процент гипохромных клеток (% Hypo)
Повышенный процент гипохромных эритроцитов и пониженное содержание гемоглобина в ретикулоцитах обнаруживаются при функциональном дефиците железа. Это полезные параметры для оценки эритропоэтической активности при функциональном дефиците железа [35].
Уровни гепсидина в сыворотке
Данных об оценке гепсидина при ЖДА немного.Предыдущие исследования показали, что гепсидин увеличивается с перегрузкой железом и уменьшается с ЖДА [12-14].
Анализы на кровопотерю
Если мелена или гематохезия не очевидны и кровопотеря не может быть идентифицирована, следует провести анализ кала на скрытую кровь. Доступны различные коммерческие тесты для обнаружения скрытой крови в стуле, которая может быть не видна при визуальном осмотре. Тем не менее, ложноположительные результаты возможны при пероральном приеме добавок железа, мясной диете и, что гораздо реже, диетическом миоглобине и гемоглобине.В некоторых случаях уровни общего белка сыворотки также низкие из-за сопутствующей потери плазмы. Визуализация брюшной полости и эндоскопия рекомендуются для визуализации органов кишечника и оценки желудочно-кишечного тракта на предмет изъязвлений, новообразований или сосудистой мальформации [18,19].
Дифференциальная диагностика
Основным дифференциальным диагнозом ЖДА является талассемия и хроническая анемия [36]. Обычно хроническая анемия связана с низким SI и SIBC и высоким или нормальным уровнем ферритина в сыворотке.
В большинстве случаев отличить ЖДА от признака талассемии нетрудно. Поскольку ширина распределения эритроцитов (RDW) является нормальной у пациентов с признаками талассемии, но высока у пациентов с ЖДА. Однако дифференцировать ЖДА и признак талассемии иногда бывает сложно, особенно если они оба существуют. У пациентов, у которых MCV улучшается, но не возвращается к норме после адекватной терапии железом, признаки талассемии следует исключить с помощью электрофореза гемоглобина.
Лечение
Общие принципы лечения пациентов с ЖДА включают предотвращение дальнейшей кровопотери, коррекцию анемии, если она тяжелая, начало приема препаратов железа и лечение основного заболевания. Переливание крови может потребоваться до получения результатов диагностической оценки, если пациент страдает тяжелой анемией и демонстрирует признаки сердечной недостаточности и гипоксии. Таким образом, переливание крови показано только в случаях тяжелой анемии с последующей гипоксией тканей, для стабилизации декомпенсированного пациента или перед проведением общей анестезии и хирургическим вмешательством у пациента с умеренной и тяжелой анемией.Нет никаких конкретных указаний, указывающих, когда переливание целесообразно; Для принятия этого решения используются клинические и лабораторные оценки пациента [37,38].
Добавки железа обычно необходимы для восстановления гомеостаза железа и должны основываться на степени анемии, основной патологии, количестве эритроцитов, панели сывороточного железа и морфологии эритроцитов.
У стабильных пациентов пероральная терапия железом обычно предпочтительнее парентерального введения железа из-за ее низкой стоимости и более высокой безопасности.Доступны как двухвалентные, так и трехвалентные формы, но рекомендуется только двухвалентная форма из-за превосходной абсорбции. Сульфат железа используется наиболее часто, но также можно использовать глюконат и фумарат железа. При определении вводимой дозы необходимо обратиться к врачу, поскольку опубликованные дозы выражены либо в миллиграммах соли железа, либо в элементарном железе. Сульфат железа в дозе 3-6 мг / кг в день вводится в течение одного месяца, а затем следует поддерживающее лечение в течение 1-3 месяцев для восполнения запасов железа в организме.Пик ретикулоцитоза происходит между пятым и десятым днем, после чего происходит значительное повышение уровня гемоглобина более чем на 1 г / дл. Одним из наиболее распространенных побочных эффектов перорального приема добавок железа является раздражение кишечника, которое можно свести к минимуму, разделив дозу несколько раз в день. Признано взаимодействие с другими лекарствами, и его следует избегать [39,40].
Парентеральные формы железа, отличные от продуктов эритроцитов, можно вводить, если пероральное железо плохо переносится, или если продемонстрировано тяжелое заболевание кишечника, или если необходима терапия эритропоэтином (например,g почечный диализ). Примерно 70% декстрана железа всасывается из места инъекции в течение нескольких дней после внутримышечного введения. Сначала следует ввести небольшую дозу, иначе могут возникнуть реакции гиперчувствительности. Другие побочные эффекты внутримышечного железа включают местное раздражение и боль в месте инъекции. Простая формула, представленная на веб-странице http://www.infed.com/calcltor.htm. может использоваться для определения заместительной дозы декстрана железа.
Внутривенное (IV) железо особенно полезно у пациентов, получающих антикоагулянтные или антитромбоцитарные препараты, которым противопоказаны внутримышечные инъекции.Доступны несколько препаратов железа для внутривенного введения, включая глюконат железа, комплекс гидроксида железа, сахарозы и декстран железа. Дозировка IV формы колеблется от 1-4 мг / кг в неделю. Пациентам назначают начальную тестовую дозу, если не отмечено побочных эффектов, оставшуюся дозу вводят в течение нескольких часов. Побочные реакции от быстрой инфузии могут включать гипотензию, тахикардию, одышку и анафилактоидные реакции. Для того чтобы параметры эритроцитов вернулись к норме, может потребоваться несколько месяцев приема добавок железа, и поэтому его следует продолжать после нормализации параметров эритроцитов, поскольку для восполнения запасов железа в организме требуется гораздо больше времени [41].
Заключение
Железо является жизненно важным элементом для множества метаболических функций, в первую очередь для транспорта кислорода гемоглобином. Гомеостаз железа зависит от регулируемого поглощения железа энтероцитом, узкоспециализированной клеткой двенадцатиперстной кишки, которая координирует поглощение и транспортировку железа с пищей в организм. ЖДА обычно развивается из-за диетических факторов, кровопотери и кишечных причин после истощения запасов железа. Хотя несколько параметров железа были изучены для диагностики ЖДА, ферритин остается наиболее надежным маркером ЖДА.Однако следует помнить, что уровень ферритина повышается во время воспаления и инфекций, и это может оказаться бесполезным для оценки ЖДА по воспалительным состояниям. Другие авторы описали «нетрадиционные» маркеры, такие как гепсидин и sTfR, которые использовались в качестве инструментов исследования, но не получили широкого распространения в повседневной практике. При соответствующей терапии пациенты с ЖДА могут иметь хороший прогноз, если можно вылечить основное заболевание.
|
Обзор вкратце |
|
|
Клинический вопрос |
Обобщить текущие знания о ЖДА с особым вниманием к метаболизму железа в отношении его патогенеза и клинических особенностей, а также его диагностики и лечения |
|
Тип обзора |
Рассказ |
|
Выводы |
Хотя несколько параметров железа были изучены для диагностики ЖДА, ферритин остается наиболее надежным маркером ЖДА.При соответствующей терапии пациенты с ЖДА могут иметь хороший прогноз, если можно вылечить основное заболевание. |
Список литературы
1. Всемирная организация здравоохранения, Детский фонд ООН, Университет ООН. Железодефицитная анемия; оценка, профилактика и контроль. Доступно по адресу: http://www.who.int/nutrition/publications/micronutrients/anaemia_iron_deficiency/en (последнее посещение — июль 2004 г.)
2.Циммерманн МБ, Харрелл РФ. Недостаток пищевого железа. Lancet 2007; 370: 511-20; http://dx.doi.org/10.1016/S0140-6736(07)61235-5
3. Suskind DL. Недостаток питательных веществ при нормальном росте. Pediatr Clin N Am 2009; 56: 1035-53; http://dx.doi.org/10.1016/j.pcl.2009.07.004
4. Lozoff B., Brittenham GM, Viteri FE, et al. Дефицит развития у младенцев с дефицитом железа: влияние возраста и тяжести нехватки железа. J Pediatr 1982; 101: 948-52; http://dx.doi.org/10.1016/S0022-3476(82)80016-4
5.Злоткин С.В. Лечебное питание: 8. Роль питания в профилактике железодефицитной анемии у младенцев, детей и подростков. CMAJ 2003; 168: 59-63
6. Johnson-Wimbley TD, Graham DY. Диагностика и лечение железодефицитной анемии в 21 веке. Therap Adv Gastroenterol 2011; 4: 177-84; http://dx.doi.org/10.1177/1756283X11398736
7. Грин Р. Анемии помимо B12 и дефицит железа: ажиотаж о других проблемах B, элементарных и неэлементарных.Образовательная программа Hematology Am Soc Hematol 2012; 2012: 492-8; http://dx.doi.org/10.1182/asheducation-2012.1.492
8. Финч CA, Huebers HA. Метаболизм железа. Clin Physiol Biochem 1986; 4: 5-10
9. Кларк С.Ф. Железодефицитная анемия. Nutr Clin Pract 2008; 23: 128-41; http://dx.doi.org/10.1177/0884533608314536
10. Bermejo F, Garcia Lopez S. Руководство по диагностике железодефицитной и железодефицитной анемии при заболеваниях пищеварительной системы. World J Gastroenterol 2009; 15: 4638-43; http: // dx.doi.org/10.3748/wjg.15.4638
11. Iolascon A, Camaschella C, Pospisilova D, et al. Естественная история рецессивного наследования мутаций DMT 1. J Pediatr 2008; 152: 136-9; http://dx.doi.org/10.1016/j.jpeds.2007.08.041
12. Кая З., Йылдыз Э., Гурсель Т. и др. Уровни прогепсидина в сыворотке крови у детей с солидными опухолями, воспалительными заболеваниями кишечника и железодефицитной анемией. J Trop Pediatr 2011; 57: 120-5; http://dx.doi.org/10.1093/tropej/fmq058
13. Ривера С., Немет Э., Габаян В. и др.Синтетический гепсидин вызывает быструю дозозависимую гипоферремию и концентрируется в ферропортин-содержащих органах. Кровь 2005; 106: 2196-9; http://dx.doi.org/10.1182/blood-2005-04-1766
14. Ганц Т., Немет Э. Импорт железа: IV. Гепсидин и регуляция метаболизма железа в организме. Am J Physiol Gastrointest Liver Physiol 2006; 290: 199-203; http://dx.doi.org/10.1152/ajpgi.00412.2005
15. Гриффин И.Дж., Абрамс С.А. Утюг и грудное вскармливание. Pediatr Clin North Am 2001; 48: 401-13; http: // dx.doi.org/10.1016/S0031-3955(08)70033-6
16. Чжу А., Канеширо М, Кауниц Дж. Д. Оценка и лечение железодефицитной анемии: гастроэнтерологические перспективы. Dig Dis Sci 2010; 55: 548-59; http://dx.doi.org/10.1007/s10620-009-1108-6
17. Шолль К. Статус материнского железа: связь с ростом плода, сроком беременности и обеспеченностью железом новорожденного. Nutr Rev 2011; 69: 23-9; http://dx.doi.org/10.1111/j.1753-4887.2011.00429.x
18. Маджид С., Салих М., Васая Р. и др.Предикторы поражения желудочно-кишечного тракта при эндоскопии при железодефицитной анемии без желудочно-кишечных симптомов. BMC Gastroenterol 2008; 8:52; http://dx.doi.org/10.1186/1471-230X-8-52
19. Serefhanolu S, Büyükaşik Y, Emmungil H, et al. Идентификация клинических и простых лабораторных переменных, позволяющих прогнозировать ответственные поражения желудочно-кишечного тракта у пациентов с железодефицитной анемией. Int J Med Sci 2010; 8: 30-8
20. Finch CA, Cook JD, Labbe RF, et al. Влияние донорства крови на запасы железа по ферритину сыворотки.Blood 1977; 50: 441-7
21. Финберг К.Е., Хини М.М., Кампанья Д.Р. и др. Мутации в TMPRSS6 вызывают железо-рефрактерную железодефицитную анемию (IRIDA). Nat Genet 2008; 40: 569-71; http://dx.doi.org/10.1038/ng.130
22. Biondich PG, Downs SM, Carroll AE, et al. Недостатки методов скрининга на дефицит железа у младенцев. Педиатрия 2006; 117: 290-4; http://dx.doi.org/10.1542/peds.2004-2103
23. Боген Д.Л., Дагган А.К., Довер Г.Дж. и др. Скрининг железодефицитной анемии по анамнезу питания в популяции высокого риска.Педиатрия 2000; 105: 1254-9; http://dx.doi.org/10.1542/peds.105.6.1254
24. Lozoff B, Çorapci F, Burden MJ, et al. Дети дошкольного возраста с железодефицитной анемией демонстрируют измененные аффекты и поведение. J Nutr 2007; 137: 683-9
25. Oner N, Kaya Z, Türkyilmaz Z, et al. Необычная причина железодефицитной анемии у ребенка с литобезоаром толстой кишки: отчет о болезни и обзор литературы. J Hematol 2012; 1: 28-31
26. Felt BT, Beard JL, Schallert T, et al.Стойкие нейрохимические и поведенческие аномалии в зрелом возрасте, несмотря на раннее введение препаратов железа при перинатальной железодефицитной анемии у крыс. Behav Brain Res 2006; 171: 261-70; http://dx.doi.org/10.1016/j.bbr.2006.04.001
27. Акман М., Цебечи С., Окур В. и др. Влияние дефицита железа на результаты тестов развития младенцев. Acta Paediatr 2004; 93: 1391-6; http://dx.doi.org/10.1111/j.1651-2227.2004.tb02941.x
28. Ортис Э., Паскини Дж. М., Томпсон К. и др.Влияние манипулирования хранением, транспортом или доступностью железа на состав миелина и содержание железа в головном мозге на трех различных моделях животных. J Neurosci Res 2004; 77: 681-9; http://dx.doi.org/10.1002/jnr.20207
29. Grantham-McGregor S, Ani C. Обзор исследований влияния дефицита железа на когнитивное развитие у детей. J Nutr 2001; 131: 649-66S
30. Urrechaga E, Borque L, Escanero JF. Параметры эритроцитов и ретикулоцитов при дефиците железа и талассемии.J Clin Lab Anal 2011: 25: 223-8; http://dx.doi.org/10.1002/jcla.20462
31. Даллман П.Р., Сиймес Массачусетс. Процентильные кривые для гемоглобина и объема эритроцитов в младенчестве и детстве. J Pediatr 1979; 94: 26-31; http://dx.doi.org/10.1016/S0022-3476(79)80344-3
32. Керпер М.А., Даллман ПР. Концентрация железа в сыворотке и насыщение трансферрина в диагностике дефицита железа у детей: нормальные изменения развития. J Pediatr 1977; 91: 870-4; http://dx.doi.org/10.1016/S0022-3476(77)80879-2
33.Оливарес М., Уолтер Т., Кук Дж. Д. и др. Польза сывороточного рецептора трансферрина и сывороточного ферритина в диагностике дефицита железа в младенчестве. Am J Clin Nutr 2000; 72: 1191-5
34. Пуннонен К., Ирьяла К., Раджамаки А. Рецептор трансферина сыворотки и его соотношение к ферритину сыворотки при диагностике дефицита железа. Blood 1997; 89: 1052-7
35. Brugnara C, Laufer MR, Friedman AJ, et al. Содержание гемоглобина в ретикулоцитах (CHr): ранний индикатор дефицита железа и ответ на терапию.Кровь 1994; 83: 3100-1
36. Даллман П.Р., Ип Р., Оски Ф.А. Дефицит железа и связанные с ним пищевые анемии. В: Натан Д.Г., Оски Фа (ред.) Гематология в младенчестве и детстве. Филадельфия: Сондерс, 1993
37.


