Симптомы иммунодефицита у взрослых: Первичный иммунодефицит: лечение заболевания | Клиника Рассвет
12 настораживающих признаков ПЕРВИЧНОГО ИММУНОДЕФИЦИТА
Первичный иммунодефицит (ПИД) может быть причиной тяжелых инфекций у детей и у взрослых, которые с трудом поддаются лечению. 1 из 500 человек является носителем хотя бы одного из известных первичных иммунодефицитов. Если Вы или кто-то из Ваших родственников или знакомых имеют два или более двух настораживающих признаков иммунодефицита, обратитесь к своему лечащему врачу.
-
Наличие семейного анамнеза, факты ранних смертей от тяжелых инфекций.
-
Частые отиты (8 и более в течение года).
-
Тяжелые синуситы (2 и более в течение года).
-
Пневмония не менее 2 раз в год.
-
Длительное, в течение 2-х месяцев и более применение антибиотиков с минимальным эффектом.
-
Осложнения при вакцинации.
-
Отставание в росте и развитии грудного ребенка.
-
Рецидивирующие глубокие абсцессы кожи или внутренних органов.

-
Не менее двух тяжелых инфекций в год (менингит, остеомиелит, эмпиема, сепсис).
-
Персистирующий кандидоз кожи и слизистых у ребенка в течение 1 года.
-
Нарушение пищеварения в раннем детском возрасте.
-
Рецидивирующие системные инфекции атипичными микобактериями (например, шейный лимфаденит).
АЛГОРИТМ ДИАГНОСТИКИ ПЕРВИЧНЫХ ИММУНОДЕФИЦИТОВ
Анамнез (какие клинические симптомы изменения в анализах были у ребенка ранее, семейный анамнез).
Осмотр.
Предварительный диагноз.
Иммунологическое обследование.
Верификация диагноза.
Молекулярно-генетическое обследование.
Заключительный диагноз.
АЛГОРИТМ ДЕЙСТВИЙ ВРАЧА ДЛЯ ДИАГНОСТИКИ ПЕРВИЧНЫХ ИММУНОДЕФИЦИТОВ
-
Сбор анамнеза. Семейный анамнез. Осмотр (состояние лимфоидной ткани, размеры печени, селезенки). Общий анализ крови. Биохимический анализ крови (с определением гаммаглобулинов).
-
Определение концентраций сывороточных иммуноглобулинов (IgA, IgG, IgM, IgE соответственно возрастным нормам).

- Определение субпопуляций лимфоцитов (CD3, CD4, CD8, CD19, CD16/56, CD 45). Определение хемилюминисценсции нейтрофилов. Определение анамнестических антител.
- Определение экспрессии CD40L, WASP, синтеза АДА. Определение компонентов комплемента (CH50, C3, C4). Определение экспрессии CD18, CD11b; хемотаксиса.
- Определение цитотоксичности NK-клеток. Определение антительного ответа на неоантигены.
- Определение рецепторов и синтеза гамма интерферона и IL-12.
- Генетическое исследование.
Адреса иммунологических центров:
г. Москва
ФГБУ ГНЦ РФ Институт иммунологии ФМБА России
Каширское шоссе, д. 24, корп. 2
Российская детская клиническая больница,
отделение клинической иммунологии
Ленинский проспект, д. 117
ФГУ “Федеральный научно-клинический центр детской гематологии, онкологии и иммунологии” МЗ РФ
ул. Саморы Машела, д. 1
Московский городской консультативно-диагностический центр детской аллергологии и иммунологии ДЗ г. Москвы
Москвы
ДГКБ №9 им. Д.Г. Сперанского
Шмитовский пр-д, д. 29
Пути передачи ВИЧ-инфекции — Как обезопасить себя? — ВИЧ/СПИД: материалы Детского фонда ООН
Как обезопасить себя?
Пути передачи ВИЧ-инфекции
ВИЧ передается при передаче биологических жидкостей, содержащих вирус иммунодефицита, от одного человека другому.
Вирус иммунодефицита присутствует в следующих биологических жидкостях: кровь, сперма и пре-эякуляционные выделения, вагинальные выделения и грудное молоко. Данный вирус также содержится в слюне, однако, по мнению экспертов, его концентрация слишком мала для того, чтобы вызвать заболевание.
Встреча в джаз-клубе в столице Замбии Лусаке,. Фото ЮНИСЕФ.Отсюда следует, что поцелуи, даже глубокие поцелуи с открытым ртом, не несут никакого риска. Также невозможно заразиться ВИЧ при обычных прикосновениях, например при рукопожатии. Более того, нельзя заразиться ВИЧ от прикосновения к той вещи, которой уже касался ВИЧ-инфицированный. ВИЧ также невозможно заразиться воздушным путем. Биологические жидкости, содержащие вирус иммунодефицита, попадают в организм человека только через повреждения в тканях/коже.
Более того, нельзя заразиться ВИЧ от прикосновения к той вещи, которой уже касался ВИЧ-инфицированный. ВИЧ также невозможно заразиться воздушным путем. Биологические жидкости, содержащие вирус иммунодефицита, попадают в организм человека только через повреждения в тканях/коже.
Секс
Незащищенный проникающий секс является наиболее распространенным способом попадания биологических жидкостей из одного организма в другой, что может повлечь распространение вируса. «Незащищенный» означает секс без презерватива, «проникающий» значит, что во время полового акта пенис проникает или входит во влагалище или анальное отверстие. В этом случае сперма, зараженная вирусом иммунодефицита, вагинальная жидкость или кровь одного человека могут попасть в организм другого человека через мельчайшие порезы или раны во влагалище, анальном отверстии или на пенисе. Данные порезы или раны могут быть настолько малы, что их невозможно увидеть.
Наличие другого венерического заболевания повышает вероятность заражения ВИЧ-инфекцией, т. к. венерические заболевания вызывают повреждения тканей половых органов, способствуя попаданию зараженной крови в кровеносную систему. Венерические заболевания могут также становиться причиной серьезных проблем со здоровьем. Поэтому при возникновении в половых органах таких симптомов, как боль, язвы или раны, зуд или опухание, проблемы с мочеиспусканием, следует обязательно обратиться к медицинскому работнику. Все больницы, медицинские центры, клиники и частные врачи могут вылечить венерические заболевания. Не следует стесняться: вне зависимости от того, где проходит лечение, вся информация об этом является конфиденциальной.
к. венерические заболевания вызывают повреждения тканей половых органов, способствуя попаданию зараженной крови в кровеносную систему. Венерические заболевания могут также становиться причиной серьезных проблем со здоровьем. Поэтому при возникновении в половых органах таких симптомов, как боль, язвы или раны, зуд или опухание, проблемы с мочеиспусканием, следует обязательно обратиться к медицинскому работнику. Все больницы, медицинские центры, клиники и частные врачи могут вылечить венерические заболевания. Не следует стесняться: вне зависимости от того, где проходит лечение, вся информация об этом является конфиденциальной.
Наркотики и иглы
Наркоманы, использующие нестерильные иглы, шприцы и воду для промывки, подвергают себя огромному риску заражения ВИЧ-инфекцией. Биологические жидкости (чаще всего кровь), содержащие вирус иммунодефицита, могут попасть прямо в систему кровообращения через иголки на шприце, что делает риск заражения очень высоким.
Татуировки и пирсинг, производимые с использованием нестерильного оборудования, также несут риск заражения ВИЧ-инфекцией.
Передача инфекции от матери ребенку
Матери, зараженные ВИЧ-инфекцией, могут передать ее своим детям во время беременности, родов или в период грудного вскармливания. Если ВИЧ-инфицированная женщина становится беременной, существует 35-процентная вероятность того, что она передаст вирус ребенку в случае отсутствия превентивного лечения.
Переливание крови и препараты крови
Каждому донору крови следует пройти тест на ВИЧ, чтобы зараженная кровь не попала в другой организм. К сожалению, не везде медицинские услуги включают проверку донорской крови на содержание вируса иммунодефицита.
Лечение первичного иммунодефицита в Иваново платный прием, цены на услуги в лечебно-диагностическом центре «Миленарис»
Симптомы
Обратиться к иммунологу нужно при наличии признаков, которые говорят о нарушении защитных сил организма. Все они сигнализируют о том, что тело находится в истощенном состоянии, не может самостоятельно бороться с бактериями и противостоять болезням.
Признаками проблем с иммунитетом могут быть:
- повышенная температура тела, которая возникает без причины и «сопровождения» в виде насморка, кашля и т.п.
- частые инфекционные заболевания.
- невозможность вылечит грибковые или вирусные заболевания.
- головные боли, которые становятся регулярными.
- боли в суставах и общий дискомфорт.
- мышечные боли.
- увеличенные лимфатические узлы.
- общая слабость и повышенная утомляемость – даже в выходной день, когда вы не идете на работу, физически не работаете.
- нарушение сна, частые нервные расстройства.
- скачки веса – в сторону набора или потери.
- гнойные высыпания на коже, возникающие регулярно или часто.
Если хотя бы один из симптомов вы наблюдаете у себя или своего близкого, обратитесь в ЛДЦ Миленарис, чтобы получить квалифицированную консультацию. Если проблему выявить и лечить на раннем этапе, можно избежать множества негативных последствий и быстро вернуть себе хорошее самочувствие.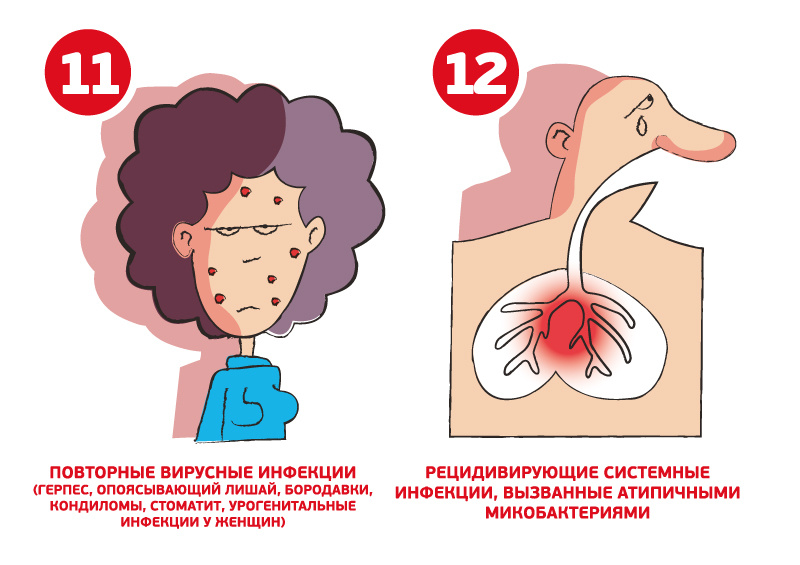
Подготовка к приему
К посещению иммунолога нужно заранее подготовиться, ведь в процессе приема возможен забор анализов. А чтобы результаты обследования были максимально объективными, подготовьтесь таким образом:
- Перед консультацией не ешьте в течение 12 часов. Поэтому, первичный прием лучше назначить на первую половину дня.
- Откажитесь от спиртного и не курите.
- Если возможно, не принимайте лекарства. В случае, если лекарства отменить на время нельзя, обязательно скажите об этом врачу.
- Утром перед обследованием не пейте жидкости, максимально ограничьте ее вечером.
В случае, если перед приемом вы испытали нервный стресс или произошло обострение хронического заболевания, то консультацию лучше перенести. Других мер подготовки не нужно.<
Как проходит прием
Прежде всего, происходит сбор анамнеза и первичное обследование. Иммунолог направит вас на проведение лабораторных исследований, среди которых:
- биохимический и общий анализ крови;
- комплексное иммунологическое исследование;
- ревмопробы;
- выявление и диагностика хронических инфекций.

На основе полученных данных, специалист назначает схему лечения. Она построена таким образом, чтобы восстановить нормальную работу иммунной системы. Кроме того, даются рекомендации по профилактике дальнейших проблем. Чаще всего, последние заключаются в правильном питании, регулярных физических нагрузках (умеренных), отдыхе. Однако, конкретные рекомендации зависят от особенностей проблемы пациента.
Методы диагностики и лечения
Клиника Миленарис обладает всем необходимым оборудованием для того, чтобы комплексно исследовать иммунный статус пациента. Так, проводится оценка системного и местного иммунитетов. В первом случае вам потребуется иммунограмма, исследование инфекционного статуса, клинический анализ крови. Во втором – развернутый анализ мокроты, цитологические исследования из носа и зева, бакпосевы кала, а также со слизистых зева и носа.
После получения результатов назначается лечение. На основании иммунограммы происходит коррекция при помощи иммуномодуляторами. Это лекарства, которые восстанавливают эффективность иммунных сил организма. При этом, нужно строго следовать схеме лечения, не менять самостоятельно дозировку или срок приема.
Это лекарства, которые восстанавливают эффективность иммунных сил организма. При этом, нужно строго следовать схеме лечения, не менять самостоятельно дозировку или срок приема.
Если вы обнаружили у себя проблемы с иммунитетом, обратитесь к специалисту клиники Миленарис. Здесь помогут восстановить ваш иммунитет и укрепить его.
Иммунологи обозначили 12 признаков первичного иммунодефицита
МОСКВА, 26 апреля. Врачи-иммунологи по просьбе благотворительного фонда «Подсолнух» сформулировали 12 признаков, по которым можно заподозрить первичный иммунодефицит у пациента. Этот список опубликован в открытом письме к медицинским работникам на сайте фонда.
«Врачи зачастую вообще не знают о таком заболевании, как первичный иммунодефицит», — объяснила «Росбалту» важность письма сотрудник фонда Виолетта Кожерева.
Она рассказала, что это заболевание на сегодняшний день считается редким. Многие узнают о своей болезни слишком поздно, потому что в регионах ее практически не диагностируют.
«К сожалению, патологоанатомы оказываются намного опытнее лечащих врачей, потому что во многих случаях диагноз иммунодефицит ставится посмертно», — рассказала Кожарева. Такая ситуация, по ее мнению, сложилась из-за недостатка у врачей знаний об этом заболевании.
«Открытое письмо рассчитано на то, чтобы привлечь к проблеме внимание медиков. Но если родители прочтут его, и вместо того, чтобы месяцами лежать в инфекционных больницах, пока у ребенка не откажут легкие, станут требовать направление к иммунологу, число посмертных диагнозов снизится», — считает собеседница агентства.
Еще одна проблема, по ее словам, состоит в том, что специальность иммунолог–аллерголог смежная. В связи с тем, что самое распространенное заболевание в этой области – бронхиальная астма, большинство врачей акцент делают именно на аллергических проявлениях. Поэтому, как отметила Кожерева, даже иммунологи не всегда могут заподозрить первичный иммунодефицит у пациента.
Она также добавила, что только в этом году в расписании медвузов появились дополнительные часы на клиническую иммунологию. Теперь пациентам с этим редким заболеванием придется ждать еще как минимум 5-6 лет, пока специалисты, обладающие достаточными знаниями по иммунодефициту, придут в больницы.
Теперь пациентам с этим редким заболеванием придется ждать еще как минимум 5-6 лет, пока специалисты, обладающие достаточными знаниями по иммунодефициту, придут в больницы.
Настораживающие признаки первичного иммунодефицита у детей:
1. Положительные данные о наследственном анамнезе по ПИД.
2. Восемь или более гнойных отитов в течение года.
3. Два или более тяжелых синусита в течение года.
4. Две или более пневмонии в течение года.
5. Антибактериальная терапия, проводимая более 2 месяцев, без эффекта.
6. Осложнения при проведении вакцинации ослабленными живыми вакцинами (БЦЖ, полиомиелит).
7. Нарушения переваривания в период грудного возраста, с или без хронических поносов.
8. Рецидивирующие глубокие абсцессы кожи и мягких тканей.
9. Две или более генерализованные инфекции (менингит, остеомиелит, септический артрит, эмпиема плевры, сепсис).
10. Персистирующая кандидозная инфекция кожи и слизистых у детей старше 1 года жизни.
11. Хроническая реакция трансплантат-против-хозяина (например: неясные эритемы у детей грудного возраста).
12. Рецидивирующая системная инфекция, вызванная атипичными микобактериями (не только однократные шейные лимфадениты).
Настораживающие признаки первичных иммунодефицитов у взрослых:
1. Частые гнойные отиты (не менее 3-4 раз в течение одного года).
2. Частые синуситы, протекающие в тяжелой форме.
3. Тяжелое течение бронхо-легочной патологии с частыми рецидивами.
4. Повторные глубокие абсцессы кожи или внутренних органов.
5. Необходимость в длительной иногда внутривенной терапии антибиотиками для купирования инфекции (до 2 месяцев и дольше).
6. Перенесенные не менее 2 раз глубокие инфекции, такие как менингит, остеомиелит, целлюлит, сепсис.
7. Атипичное течение гематологических заболеваний.
Атипичное течение гематологических заболеваний.
8. Атипичное течение аутоиммунных заболеваний.
9. Рецидивирующие системные инфекции, вызванные атипичными микобактериями.
10. Рецидивирующие оппортунистические инфекции (Pneumocystis carinii и др.)
11. Повторные диареи.
12. Наличие у родственников первичных иммунодефицитов, ранних смертей от тяжелых инфекций или одного из вышеперечисленных симптомов.
Симптомы, признаки и лечение ВИЧ-инфекции у женщин и мужчин — Медюнион
ВИЧ – инфекционное заболевание, при котором поражается иммунная система человека. Патология вызвана вирусом иммунодефицита человека, который разрушает иммунные клетки. В результате снижается способность организма противостоять инфекционным заболеваниям и онкопроцессам.
Вирус в окружающей среде
ВИЧ — вирус нестойкий, он погибает вне среды человеческого организма при высыхании содержащих его жидкостей и практически моментально погибает при температуре выше 56ºС.
Вирус погибает:
-
При воздействии солнечных лучей. -
В щелочной и кислой среде. Женщины, имеющие здоровую микрофлору половых органов с повышенной кислотностью, заражаются реже. -
От высоких температур. На поверхности предметов в условиях умеренной температуры ВИЧ может жить до 2 часов. Однако при нагревании свыше 60 градусов погибает за 1-2 минуты. При кипячении – моментально. При дезинфекции. -
От действия хлора. То же действие вызывает 6% перекись водорода, убивает патоген и 70% этиловый спирт.
Дольше всего ВИЧ сохраняется в крови человека. Высохшая капля крови содержит в себе активный вирус на протяжении 2-3 суток в нормальных условиях окружающей среды. Другие жидкости на предметах могут сохранять инфекцию 2-3 суток. Чем ниже температура окружающей среды, тем дольше живёт микроорганизм.
Пути инфицирования ВИЧ
ВИЧ или СПИД передается половым путем во время незащищенного полового акта. Для того, чтобы размножаться в организме человека, вирусу иммунодефицита человека, как и любому другому вирусу, необходимо «встроить» свою генетическую информацию в живую клетку. После того как это происходит, зараженный человек становится носителем вируса, но долгое время никаких признаков инфицирования может не обнаруживаться.
-
Незащищенный проникающий сексуальный контакт – анальный или вагинальный. -
Совместное использование нестерильного оборудования для инъекций. -
Совместное использование нестерильного оборудования для татуировок и пирсинга. -
От ВИЧ-инфицированной матери ребенку (возможно инфицирование во время беременности, родов и при кормлении грудью).
Заболевание не передается бытовым путем, так как вирус не способен передвигаться в окружающей среде и быстро погибает. Также невозможно заразиться через рукопожатие или объятие. Риск передачи вируса через слюну ничтожно мал, для этого два партнёра с ранками на слизистой оболочке рта должны довольно долго целоваться. При этом у носителя должно быть большое количество вируса в крови.
Классификация заболевания
ВИЧ – это не один тип возбудителя, а несколько разных. Все они относятся к лентивирусам, что от латинского означает «медленный». Такое название они получили из-за длительного развития инфекции.
Различают 2 основных типа возбудителя ВИЧ-1 и ВИЧ-2. Оба приводят к постепенному снижению иммунитета, но ВИЧ-2 менее патогенен. Для него характерно меньшее число вирусных частиц на микролитр крови, поэтому передаётся он реже и не так часто приводит к СПИДу.
Основные стадии заболевания
-
Инкубационная – происходит заражение и последующее размножение вируса в крови. Она длится до шести недель, иногда меньше. Даже будучи зараженным, на этом этапе человек не увидит явных признаков, а анализ крови не покажет, что в крови есть антитела.
Она длится до шести недель, иногда меньше. Даже будучи зараженным, на этом этапе человек не увидит явных признаков, а анализ крови не покажет, что в крови есть антитела.
-
Первичная – могут появиться первые признаки инфекции. Длится вторая стадия в течение 3 недель – в это время появляются антитела, вирус определяется лабораторно. -
Субклиническая. Появляется первый признак болезни – увеличенные лимфоузлы. Пациент чувствует себя полностью здоровым, на самочувствие не жалуется. Могут появляться вторичные заболевания: от частых простуд до кандидоза и пневмонии. -
Терминальная – предполагает быстрое и прогрессирующее истощение, а также последующую смерть больного.
Симптомы развития ВИЧ-инфекции в организме
ВИЧ-инфекция течет медленно и почти бессимптомно. В течение многих лет (от 5 до 15 лет) она может никак не тревожить человека. Бывает и так, что первые признаки могут появиться на ранней стадии, а затем исчезнуть и больше не беспокоить носителя инфекции на протяжении длительного времени.
Бывает и так, что первые признаки могут появиться на ранней стадии, а затем исчезнуть и больше не беспокоить носителя инфекции на протяжении длительного времени.
Также первые симптомы ВИЧ легко спутать с признаками других заболеваний, что может вводить в заблуждение.
На первом этапе:
-
боль в горле, повышение температуры -
болезненность кожи, суставов, костей -
озноб, лихорадка -
одновременно увеличиваются шейные лимфоузлы -
могут проявляться высыпания на коже разного рода
Новые признаки ВИЧ возвращаются через несколько лет спокойной и здоровой жизни. К ним относятся:
-
сильная усталость, быстрая утомляемость -
увеличение лимфоузлов – не только шейных, а уже нескольких групп -
снижение веса. Обычно оно выглядит беспричинным, человек не понимает, в чем дело
Обычно оно выглядит беспричинным, человек не понимает, в чем дело
-
лихорадка, озноб, потливость (преимущественно ночная) -
проблемы с ЖКТ – обычно проявляются жидким стулом без видимых на то причин
Чем опасна патология?
Болезнь опасна, в первую очередь, для заразившегося. Попадая в кровь, патоген постепенно уничтожает клетки иммунитета. Этот процесс можно замедлить с помощью антиретровирусной терапии, но полностью остановить нельзя. В результате этого организм не может противостоять инфекциям извне.
Чаще всего у пациентов развивается молочница, стоматит, длительная диарея, частые ОРВИ и т. д. Чем меньше иммунных клеток в организме человека, тем в последующем появляются более опасные заболевания, среди которых туберкулёз, онкология, поражения периферической нервной системы, саркома Капоши и другие.
Инфекция может проявлять себя абсолютно на всех органах и системах, часто заболевания совмещаются. При должном лечении эти болезни можно вылечить и поддерживать приемлемый уровень жизни пациента.
При должном лечении эти болезни можно вылечить и поддерживать приемлемый уровень жизни пациента.
Главная опасность – это СПИД – последняя стадия ВИЧ заболевания. Средняя продолжительность жизни на этой стадии – до 9 месяцев. Хотя при положительном психологическом состоянии и должной терапии пациент может прожить ещё до 3 лет.
Методы диагностики патологии
Сегодня применяются специальные высокоточные тесты, которые способны обнаружить оба вируса и антитела к ним, в том числе и в латентном течении.
Наличие ВИЧ в организме человека определяется по присутствию антител в крови. Для этого у пациента берут кровь на ВИЧ из вены. Этот анализ позволяет решить 3 задачи:
-
определить присутствие вируса в крови и начать лечение на ранних стадиях -
выявить стадию болезни и спрогнозировать ее течение -
контролировать результативность терапии
Обнаружить заболевание можно с помощью:
-
Полимеразной цепной реакции (ПЦР) – высокоточный метод молекулярно-генетической диагностики, который позволяет выявить у человека инфекционные и наследственные заболевания.
Диагностика этим методом позволяет найти возбудителя непосредственно в гене, который содержится в исследуемых материалах. Это самый точный анализ на половые инфекции, скрытые инфекции, различные венерические заболевания.
Метод прекрасен тем, что обладает высокой чувствительностью. Возможно выявить возбудителя болезни даже при наличии нескольких молекул его ДНК, то есть на очень ранних стадиях. Что позволяет вовремя вылечить заболевание.
-
ИФА (иммуноферментный анализ), который определяет антитела к обеим разновидностям вируса (ВИЧ 1 и 2). Достоверность метода составляет до 98%. При положительном результате анализ делают повторно или проводят дополнительный анализ методом иммуноблота.
Ложноположительные результаты возможны при беременности, аутоиммунных заболеваниях, гепатите или даже гриппе.
Как лечится ВИЧ?
Необходимо как можно скорее после обнаружения в организме следов вируса начать антиретровирусную терапию (сокращенно АРВТ или АРТ).
Антиретровирусная терапия — это комбинация из 3-4 препаратов, которые блокируют размножение ВИЧ на разных этапах. Вследствие ее применения вирус иммунодефицита человека перестает размножаться.
Пока АРТ не способна полностью вылечить ВИЧ-инфекцию, однако в состоянии не просто продлить жизнь ВИЧ-инфицированного человека, но и повысить ее качество.
Не менее важен образ жизни пациента, ему показан эмоциональный покой, правильное питание, профилактика инфекционных заболеваний. Также для качественного лечения важно вовремя проходить осмотр и сдавать анализы.
Какие меры профилактики нужно применять?
Так как основной способ передачи вируса – половым путем, следует заниматься только защищенным проникающим сексом. Иначе увеличивается риск заражения ВИЧ.
Кроме того, необходимо:
-
использовать только личные средства гигиены (зубная щётка, бритва, маникюрные принадлежности и т. д.)
д.)
-
проверять дезинфекцию инструментов в косметическом и медицинском кабинете, тату-салоне и во время других услуг, где можно повредить кожу -
парам – совместно сдавать анализы 2 раза в год -
зависимым от инъекционных наркотиков – использовать новый шприц или только свой
Сдать анализ на ВИЧ, пройти комплексную диагностику и лечение вирусной инфекции вы можете в медицинском центре «Медюнион». Чтобы записаться на прием или узнать расписание работы врачей, заполните форму обратной связи, и наши менеджеры свяжутся с вами в течение 15 минут.
СПИД.Пути заражения и профилактика — Кировский клинико-диагностический центр (бывшая Кировская клиническая больница № 8)
Четверг,
27
Ноября
2014
СПИД — это аббревиатура, которая расшифровывается следующим образом: Синдром Приобретенного Иммунодефицита.
- Синдром — это ряд признаков и симптомов, отличающих отдельные заболевания и состояния.
- Приобретенный — т.е. не врожденный, а полученный в течение жизни (хотя, можно сказать, что в некоторых случаях иммунодефицит может быть врожденным — в случае передачи ВИЧ-инфекции от ВИЧ-положительной матери ее ребенку во время беременности или родов).
- Иммуно-, иммунный — относящийся к иммунной системе человека, той, которая обеспечивает нашу защиту от различных болезнетворных бактерий и вирусов.
- Дефицит — недостаток чего-либо.
К развитию СПИДа приводит заражение человека ВИЧ-инфекцией.
ВИЧ — Вирус Иммунодефицита Человека (мельчайший микроорганизм, вызывающий у человека иммунодефицит).
Иммунодефицит — состояние организма, когда защитная (иммунная) система разрушена настолько, что не в состоянии бороться с любыми, даже самыми безобидными заболеваниями.
ВИЧ, как и другие вирусы, очень мал — слишком мал, чтобы его можно было разглядеть в обычный микроскоп.
Действие вируса иммунодефицита в общих словах можно описать следующим образом. При попадании в организм человека, ВИЧ поражает иммунную систему, уничтожает специальные клетки, функцией которых является защита организма от инфекций, уничтожение опасных микробов. Разрушая иммунную систему, ВИЧ делает нас неспособными противостоять не только внешним инфекциям, но и «инфекционным агентам» (бактериям, грибкам и т.д.), которые при здоровой иммунной системе существуют в нашем организме и не вызывают заболеваний.
Как и другие вирусы, ВИЧ может размножаться только внутри клеток хозяина — инфицированного человека. ВИЧ способен жить вне организма в течение довольно короткого периода времени, продолжительность которого зависит от таких факторов, как температура и наличие жидкости в среде, окружающей вирус. Вирус чувствителен к нагреванию и погибает при 56 градусах по Цельсию.
Вирус чувствителен к нагреванию и погибает при 56 градусах по Цельсию.
Как передается вирус иммунодефицита?
Существует только три пути передачи ВИЧ-инфекции.
Половой путь. ВИЧ передается от одного человека к другому во время незащищенного сексуального контакта (без презерватива), когда в организм попадает сперма или влагалищные выделения зараженного партнера.
Через кровь. ВИЧ передается через зараженную кровь или кровепродукы. Это может произойти при переливании не тестированной на ВИЧ крови, плазмы, препаратов крови. Однако, заражение ВИЧ при переливании донорской крови маловероятно, вследствие того, что все доноры в обязательном порядке обследуются на ВИЧ при каждой кроводаче. Люди, имевшие возможность заразиться, не должны быть донорами (пусть даже анализы на данный момент отрицательные, но этот человек может находиться в «периоде окна»), чтобы не подвергать даже минимальной опасности заражения реципиентов — людей, которым будет сделано переливание.
Многократное использование медицинских игл и шприцев без стерилизации, также может приводить к передаче малого количества крови от одного человека к другому и, следовательно, к заражению ВИЧ. Чаще всего это наблюдается среди наркоманов, вводящих наркотики внутривенно и пользующихся общим шприцем.
Также возможна передача ВИЧ при попадании инфицированной крови в ранку на теле незараженного человека.
ВИЧ может передаваться через зараженную кровь, оставшуюся на инструментах для прокалывания ушей, нанесения татуировок и т.д. Иглы, используемые для этих целей, также должны быть одноразового использования или стерилизоваться после каждого применения. Следует также избегать пользования общими зубными щетками и бритвами, хотя риск заражения таким путем минимален.
От матери к ребенку. ВИЧ-положительная мать может передать вирус ребенку во время беременности, родов или при грудном вскармливании.
По статистике, риск заражения составляет в среднем 20-45%. Вероятно, риск больше, если мать недавно инфицирована или уже больна СПИДом, чем при бессимптомной стадии ВИЧ-инфекции. Но сегодня существуют лекарства, которые позволяют снизить риск рождения ВИЧ-инфицированного ребенка до 4-6%, если женщина будет принимать их во время беременности. Все дети, рожденные от ВИЧ-положительных матерей, содержат в крови антитела к ВИЧ, независимо от того, заражен ребенок или нет, т.к. материнские антитела к ВИЧ проникают через плаценту. У незараженных детей антитела исчезают к полутора годам. Только после этого анализ на ВИЧ может определить, заражен ли ребенок. Также, передача вируса от матери к ребенку может произойти при грудном вскармливании, т.к. грудное молоко содержит достаточную концентрацию ВИЧ-инфекции, чтобы ребенок мог заразиться. Если ВИЧ-положительная женщина хочет иметь ребенка, то ей следует проконсультироваться с квалифицированным специалистом о риске рождения ребенка с ВИЧ.
Как можно защитить себя от заражения ВИЧ-инфекцией?
Зная, как передается ВИЧ, мы можем предотвратить его распространение. Лучший способ избежать заражения ВИЧ — это не допускать проникновения крови, семенной жидкости и влагалищных выделений других людей в свой организм.
Вы можете также принять решение иметь только одного полового партнера и сохранять взаимную верность. Если Вы не представляете свою жизнь без секса, то следующим эффективным способом предохранения являются латексные презервативы, т.е. безопасный секс. Латексные презервативы являются менее пористыми, чем какие-либо другие, и поэтому они надежнее защитят Вас от разного рода неприятностей.
Следующим важным правилом является ответственность и внимательность во время инъекций в лечебном учреждении. Необходимо всегда следить за тем, чтобы врачи или медсестры пользовались только одноразовыми шприцами и иглами. Также избегайте переливания Вам непроверенной донорской крови.
Также избегайте переливания Вам непроверенной донорской крови.
И, самое главное, — не употреблять наркотики, т.к. более 70% ВИЧ-положительных в России, это люди, употребляющие наркотики внутривенно. Следуя этим правилам, Вы можете быть в большей степени уверенными, что Вы не заразитесь ВИЧ.
симптомы, причины, диагностика, лечение| АО «Медицина» (клиника академика Ройтберга)
Первичные иммунодефициты — общее название группы патологических состояний, характеризующихся нарушениями в работе иммунитета человека. В большинстве случаев заболевания носят врождённый характер. Симптоматика зависит от типа расстройства, имеющегося у ребёнка или взрослого. Часто пациенты страдают от повышенной восприимчивости к бактериальным и вирусным инфекциям.
Общие сведения
Иммунодефицитные состояния стали предметом клинических исследований во второй половине XX века. Современная иммунология выделяет более двух десятков заболеваний рассматриваемого типа. Значительная часть патологий относится к генетическим дефектам. Наиболее часто диагноз «первичный иммунодефицит» ставится детям в возрасте до пяти лет. Взрослые могут страдать от слабовыраженных форм заболевания. Некоторые пациенты узнают о том, что являются носителями первичного иммунодефицита, только после прохождения диагностических тестов в клинических условиях. Отдельные типы патологии сопровождаются многочисленными пороками развития и отличаются высокой летальностью.
Современная иммунология выделяет более двух десятков заболеваний рассматриваемого типа. Значительная часть патологий относится к генетическим дефектам. Наиболее часто диагноз «первичный иммунодефицит» ставится детям в возрасте до пяти лет. Взрослые могут страдать от слабовыраженных форм заболевания. Некоторые пациенты узнают о том, что являются носителями первичного иммунодефицита, только после прохождения диагностических тестов в клинических условиях. Отдельные типы патологии сопровождаются многочисленными пороками развития и отличаются высокой летальностью.
Причины первичных иммунодефицитов
Первичные иммунодефициты формируются на этапе внутриутробного развития плода под действием внешних факторов. Заболевания этой группы часто осложняются пороками — дистрофиями, дефектами органов, ферментопатиями.
Иммунологи выделяют две основных причины развития иммунных патологий:
- генетические мутации;
- тератогенные воздействия (токсины, медикаменты, вирусные и бактериальные инфекции, перенесённые женщиной в период вынашивания плода).
Иммунодефицитные состояния могут характеризоваться как идиопатические при отсутствии в анамнезе пациента сведений о генетических патологиях или тератогенных воздействиях.
Виды патологии
Общее количество патологических состояний, относящихся к первичным иммунодефицитам, превышает два десятка наименований. Базовая классификация, используемая иммунологами, предусматривает выделение пяти основных групп заболеваний:
- первичных дефицитов клеточного иммунитета — проявляются на фоне низкой активности или недостаточного количества T-лимфоцитов;
- первичных дефицитов гуморального иммунитета — развиваются из-за сниженной функции B-лимфоцитов и нарушений в синтезе иммуноглобулинов;
- комбинированных первичных иммунодефицитов — становятся следствием снижения активности клеточных и гуморальных звеньев иммунитета;
- первичных недостаточностей фагоцитов — возникают при недостаточной активности моноцитов и гранулоцитов;
- дефицитов белков комплемента — обусловлены мутациями генов, кодирующих компоненты комплемента (каскадной системы защитных белков).

Диагностика перечисленных заболеваний выполняется в клинических условиях. Отдельные признаки врождённых патологий иммунной системы проявляются в первые дни жизни ребёнка.
Симптомы первичных иммунодефицитов
Клиническая картина первичных иммунодефицитов разнообразна, но у каждой из рассмотренных выше групп патологий существуют общие признаки. Их выявление позволяет врачам поставить пациентам точный диагноз.
При дефицитах клеточного иммунитета дети часто страдают от вирусных и грибковых инфекций. Они тяжелее своих сверстников переносят ветряную оспу, паротит, герпетические поражения. Часто у носителей патологии выявляется кандидоз полости рта, грибковые поражения лёгких.
Дефекты гуморальной защиты организма становятся причиной повышенной чувствительности пациентов к бактериальным инфекциям: пневмониям, пиодермиям, стрептодермиям. Бактерии поражают слизистые оболочки, бронхи, кишечник.
Бактерии поражают слизистые оболочки, бронхи, кишечник.
Комбинированные иммунодефициты и ослабления функций фагоцитов провоцируют развитие вирусных, бактериальных и грибковых заболеваний. Часто течение одной патологии осложняется присоединением вторичной инфекции. Пациенты страдают от образования абсцессов в различных органах, флегмон и очагов септического поражения.
Диагностика заболевания
Первичные иммунодефициты могут проявляться в первые дни и недели жизни ребёнка. Родителям следует обратиться к иммунологу или педиатру при частых вирусных и простудных заболеваниях.
Врач проводит осмотр пациента. Признаком иммунодефицитного состояния может стать дерматомикоз, эрозии или атрофии слизистых оболочек. Иногда первичный иммунодефицит приводит к отёкам подкожной жировой клетчатки.
Лабораторные анализы крови подтвердят снижение уровня лейкоцитов и фагоцитов. На фоне гуморального иммунодефицита в плазме присутствуют необычные метаболиты — результаты развития ферментопатий.
Специфические иммунологические тесты применяются для выявления конкретной формы патологии, от которой страдает пациент. Сотрудники клинических лабораторий изучают концентрацию активированных лейкоцитов в крови, фагоцитарную активность гранулоцитов, определяют общий уровень иммуноглобулинов и их отдельных фракций.
Молекулярно-генетический анализ позволяет выявить наследственные формы первичных иммунодефицитов. Во время исследования врачи определяют гены, подвергшиеся мутации и спровоцировавшие развитие иммунодефицитного состояния.
Лечение первичных иммунодефицитов
Отдельные формы заболевания купируются при трансплантации костного мозга или эмбриональной ткани тимуса. Угнетение функций клеточного иммунитета ослабляется при использовании стимулирующих препаратов. Ферментопатии лечатся с помощью средств на основе энзимов или специфичных метаболитов. При первичном гуморальном иммунодефиците пациенты получают заместительную терапию — инъекции иммуноглобулинов.
Угнетение функций клеточного иммунитета ослабляется при использовании стимулирующих препаратов. Ферментопатии лечатся с помощью средств на основе энзимов или специфичных метаболитов. При первичном гуморальном иммунодефиците пациенты получают заместительную терапию — инъекции иммуноглобулинов.
Значительная роль в лечении патологии отводится профилактике инфекционных заболеваний. Детям, страдающим от иммунодефицитов, назначаются максимальные дозы медикаментов при выявлении первых признаков бактериальных, вирусных или грибковых поражений.
Вопросы и ответы
- Какие врачи занимаются лечением первичных иммунодефицитов?
- Постановка диагноза и разработка тактики лечения осуществляется иммунологом или педиатром. Пациентам могут потребоваться консультации других врачей: инфекционистов, гастроэнтерологов, кардиологов, пульмонологов и т.
 д.
д. - В каком возрасте у детей проявляются признаки первичного иммунодефицита?
- Отдельные симптомы патологии можно заметить в первые дни жизни новорождённого. Манифестация заболевания проходит в течение полугода после рождения ребёнка.
- Чем опасны первичные иммунодефициты?
- Заболевания этой группы часто осложняются различными аномалиями. При отсутствии лечения замедляется развитие ребёнка, формируются угрожающие жизни новорождённого состояния.
Источники
При подготовке статьи использованы следующие материалы:
- Ивановская Т. Е., Цинзерлинг А. В. Патологическая анатомия (болезни детского возраста). — М., 1976.
- Пальцев М. А., Аничков Н. М. Патологическая анатомия: В 2 т.
 — Т. 1.— М., 2001.
— Т. 1.— М., 2001. - Стефани Д. В., Вельтищев Ю. Е. Иммунология и иммунопатология детского возраста. — М., 1996.
Иммунодефицит у взрослых Практическое руководство для аллерголога
Allergo J Int. 2014; 23 (7): 261–268.
и
Оливер Хаусманн
Аллерголого-иммунологическая поликлиника, Университетская клиника ревматологии, клинической иммунологии и аллергологии, Больница Бернского университета, 3010 Берн, Швейцария
Варнац
Центр хронического иммунодефицита (CCI), Университетская клиника Фрайбурга, Фрайбург, Германия
Аллергико-иммунологическая поликлиника, Университетская клиника ревматологии, клинической иммунологии и аллергологии, Больница Бернского университета
, Бернский университет, Швейцария
, Берн, 30104 Люцерн, Швейцария
Центр хронического иммунодефицита (CCI), Университетская клиника Фрайбурга, Фрайбург, Германия
Автор, отвечающий за переписку.
Поступило 28 апреля 2014 г .; Принято 21 июля 2014 г.
Эта статья цитировалась в других статьях в PMC.
Abstract
Знание клинических признаков иммунодефицита (ИД) в зрелом возрасте имеет решающее значение для раннего выявления более 200 форм первичного ИД, известных на сегодняшний день. Многие из этих врожденных заболеваний генетического происхождения проявляются уже в детстве. Заболевания, связанные с недостаточностью антител, представляют собой важное исключение, при этом наиболее распространенной формой ID является общий вариабельный иммунодефицит (ОВИН).Средний возраст возникновения ОВИН составляет 24 года. К сожалению, задержка постановки диагноза все еще превышает 4 года. Врачи общей практики, а также аллергологи играют особенно важную роль в раннем выявлении. Пациенты с ID, которые обращаются в основном с признаками нарушения иммунной регуляции, представляют собой еще большую диагностическую проблему. Таким образом, аутоиммунная цитопения, воспалительные заболевания кишечника или саркоидоподобное гранулематозное воспаление могут быть первым проявлением почти у 20% пациентов с ИН. Вторичные формы удостоверений личности [e.g., из-за длительного лечения кортикостероидами, ВИЧ-инфекцию, лейкоз, лимфому, нефротический синдром, синдром мальабсорбции] необходимо дифференцировать от первичной недостаточности антител.
Вторичные формы удостоверений личности [e.g., из-за длительного лечения кортикостероидами, ВИЧ-инфекцию, лейкоз, лимфому, нефротический синдром, синдром мальабсорбции] необходимо дифференцировать от первичной недостаточности антител.
Учитывая совпадение с аллергическими симптомами [ID, сопровождающийся предрасположенностью к экземе, повышенным общим IgE, эозинофилией в крови], в настоящей статье обсуждаются клинические предупреждающие признаки ID, первые необходимые диагностические шаги и возможность дальнейшей диагностической работы. в специализированных центрах для сложных случаев, а также варианты лечения для таких случаев.
Ключевые слова: иммунодефицит, иммунодефицит, предупреждающие признаки, раннее выявление, терапия, иммуноглобулин, аутоиммунитет
Введение
В эпоху, когда продвигаются пищевые добавки, витаминные препараты и широкий спектр форм дополнительной медицинской терапии аргументом в пользу того, что они укрепляют и стимулируют иммунную систему — и учитывая, что реакция на эту рекламу предполагает, что есть большое количество людей, которые явно считают свою иммунную систему слабой, или которые чувствуют себя неуверенно или в целом хрупкими, — это важно для опытный врач-специалист, интересующийся иммунологией, чтобы установить ясность в отдельных случаях и ответить на потребности пациентов в совете и заверении с помощью целевой и экономичной диагностики.
В данной обзорной статье освещаются клинически значимые предупреждающие признаки иммунодефицита (ИД) и обсуждаются шаги, которые помогут в его диагностике и когда эти шаги следует предпринять. Статья намеренно ограничивается формами удостоверения личности у взрослых. Обзор более 200 первичных иммунных дефектов, описанных в настоящее время у детей и взрослых в значительной степени генетического происхождения, можно найти в других источниках [1, 2]. Классификация первичных иммунных дефектов IUIS (Международный союз иммунологических обществ) [2] представила текущий обзор этой группы заболеваний (табл.1). Большинство врожденных первичных иммунных дефектов проявляется в детстве. Заметным исключением здесь являются болезни, связанные с недостаточностью антител (группа 3 по классификации IUIS), в частности общий вариабельный иммунодефицит (ОВИН), который проявляется в среднем в возрасте 24 лет [3, 4]. Как наиболее распространенная форма идентификатора, CVID будет обсуждаться более подробно ниже. Обсуждается также совпадение с аллергическими заболеваниями, а также возможность дальнейшей диагностики сложных случаев в специализированных центрах.
Обсуждается также совпадение с аллергическими заболеваниями, а также возможность дальнейшей диагностики сложных случаев в специализированных центрах.
Таблица 1
Классификация IUIS и разделение на группы болезней [2]
| 1. Комбинированный Т- и В-клеточный иммунодефицит |
| 2. Комбинированный иммунодефицит с ассоциированными или синдромальными признаками |
| 3. Преимущественно недостаточность антител |
| 4. Заболевания иммунной дисрегуляции |
| 5. Врожденные дефекты количества и / или функции фагоцитов |
| 6.Нарушения естественного иммунитета (врожденный иммунитет) |
| 7. Аутовоспалительные расстройства |
8. Дефицит комплемента Дефицит комплемента |
Клинические проявления иммунодефицитов
Иммунная защита организма начинается с анатомических барьеров, т.е. е., кожа и слизистые оболочки. Даже у иммунокомпетентных людей здесь возникает большинство инфекций. Обеспокоенность возникает, когда инфекции, вызываемые типичными патогенами, такими как пневмококки, стафилококки или сальмонеллы, развиваются сложным и длительным течением или когда эти анатомические барьеры неоднократно нарушаются.Инфекции в необычных местах, а также инфекции, вызванные практически безвредными патогенами, с которыми иммунная система обычно способна справиться, так называемыми условно-патогенными микроорганизмами, такими как микобактерии, Candida или Pneumocystis jirovecii, должны вызывать беспокойство. В таких случаях одно только обнаружение патогена, независимо от клинического течения, должно указывать на ИД. Во всех вышеупомянутых случаях следует начать дальнейшие исследования для установления иммунного статуса пациента.
Тщательный сбор анамнеза пациентов с прошлыми инфекциями имеет решающее значение для любой оценки иммунокомпетентности.
Направленные вопросы используются для записи типа, локализации, частоты и серьезности инфекций. В некоторых случаях этот шаг уже позволяет отличить ID от вторичной восприимчивости к инфекциям из-за локальных нарушений барьера кожи и слизистых оболочек. Таким образом, особенно в случае очаговых инфекций, таких как рецидивирующие инфекции мочевыводящих путей или хронический риносинусит или бронхит, необходимо учитывать местные неиммунологические нарушения защитных механизмов организма или анатомические аномалии.Примеры общей вторичной восприимчивости к инфекциям, не являющимся результатом ID, перечислены в Табл. 2. Особого внимания в этом контексте заслуживает атопический диатез, который из-за аллерген-опосредованных поражений слизистой оболочки иногда связан с повышенной восприимчивостью к инфекциям дыхательных путей и желудочно-кишечным симптомам. Эту причину необходимо исключить до проведения иммунологического обследования.
Таблица 2
Предрасположенность к инфекции без основного иммунодефицита
| Расположение | Причина |
|---|---|
| Кожа | Барьерное нарушение при атопической экземе, ожогах и т. Д. |
| Дыхательные пути | Курение, сухость слизистых оболочек, аллергия Бронхоэктатическая болезнь, муковисцидоз Нарушение вентиляции придаточных пазух носа и среднего уха, дисфагия, свищи |
| Кишечный тракт | Ингибиторы протонной помпы (снижение желудочной кислоты) Нарушение на фоне антибактериальной терапии |
| Мочевыводящие пути | Рефлюкс, стеноз, остаточная моча, половой акт, сухость слизистой между мочевыводящими путями и кишечником |
| Инородные тела | Катетер, протезы |
При наличии удостоверения личности, тип инфекции может определять тип иммунного дефекта. Рецидивирующие бактериальные инфекции дыхательных путей и желудочно-кишечного тракта особенно указывают на гуморальный иммунный дефект (дефицит антител, дефект комплемента). С другой стороны, необычная (условно-патогенная) инфекция указывает, в частности, на клеточный иммунный дефект, как, например, при ВИЧ-инфекциях. Стойкое образование абсцесса, особенно при поражении внутренних органов, системных грибковых инфекциях или остеомиелите, может быть результатом дисфункции нейтрофилов / макрофагов (нарушение фагоцитоза, нейтропения).С другой стороны, кожно-слизистый кандидоз, ограниченный кожей и слизистыми оболочками, свидетельствует об особом дефекте Т-клеток, продуцирующих интерлейкин (ИЛ) -17 (дефицит Th-17) [5].
Рецидивирующие бактериальные инфекции дыхательных путей и желудочно-кишечного тракта особенно указывают на гуморальный иммунный дефект (дефицит антител, дефект комплемента). С другой стороны, необычная (условно-патогенная) инфекция указывает, в частности, на клеточный иммунный дефект, как, например, при ВИЧ-инфекциях. Стойкое образование абсцесса, особенно при поражении внутренних органов, системных грибковых инфекциях или остеомиелите, может быть результатом дисфункции нейтрофилов / макрофагов (нарушение фагоцитоза, нейтропения).С другой стороны, кожно-слизистый кандидоз, ограниченный кожей и слизистыми оболочками, свидетельствует об особом дефекте Т-клеток, продуцирующих интерлейкин (ИЛ) -17 (дефицит Th-17) [5].
По этой причине классические предупреждающие знаки ID были сформулированы и обобщены для пациентов с повышенной восприимчивостью к инфекции в немецкой мнемонике ELVIS от имени Немецкой ассоциации научных медицинских обществ (AWMF, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften е. V., www.awmf.org) [4]. Хотя эти предупреждения не являются исчерпывающими и конкретными, они могут помочь практикующему врачу:
V., www.awmf.org) [4]. Хотя эти предупреждения не являются исчерпывающими и конкретными, они могут помочь практикующему врачу:
-
Патоген (Эррегер): Инфекции, вызванные условно-патогенными микроорганизмами, такими как Pneumocystis jirovecii (рис.), Должны вызывать подозрение на ИН.
Двусторонняя интерстициальная пневмония с Pneumocystis jirovecii , преимущественно при комбинированном иммунодефиците
© (4) Springer Medizin
-
Локализация (локализация): атипичная локализация инфекции, например.g., абсцесс мозга, вызванный Aspergillus (рис.), церебральный токсоплазмоз или пневмококковый артрит, наводят на мысль о ID.
Инвазивный аспергиллез с абсцессом головного мозга в правой теменно-затылочной доле. 2b: Гистология с прямым обнаружением патогенов, преимущественно при комбинированных иммунных дефектах и WAS
-
Курс (Verlauf): необычное течение с точки зрения хроничности / рецидива и неудовлетворительный ответ на терапию антибиотиками представляют признаки (хотя трудно дифференцировать) ID .

-
Интенсивность (Intensität): То же самое относится к инфекциям, которые имеют необычно тяжелое течение.
-
Количество инфекций (Summe der Infektionen): этот параметр явно зависит от возраста: ≥ 8 незначительных инфекций в год, ≥ 2 случая пневмонии или тяжелого синусита в год считаются ненормальными для маленьких детей, в то время как эмпирическое правило у взрослых ≥ 3 бактериальных инфекций в год, каждая продолжительностью более 4 недель, требует дальнейшего исследования (Табл.) [6–8].
Таблица 3
Нормальное распределение частоты инфицирования у детей (изменено из [7, 8])
Возраст (лет) Респираторные инфекции / год SD Максимум <1 6,1 ± 2,6 11,3 1-2 5,7 ± 3,0 11.  7
7 3–4 4,7 ± 2,9 10,5 5–9 5,5 ± 2,6 8,7 10–14 2,7 ± 2,2 7.2
Семейный анамнез (свидетельство генетического дефекта? Способ наследования?), А в идеале также анамнез, предоставленный третьими сторонами, например. g. родители в отношении детских инфекций и заживления пуповины или терапевт в отношении курса лечения инфекций могут помочь в диагностике ID.В случае дефицита антител (гипогаммаглобулинемия) необходимо целенаправленно искать вторичные причины до постановки диагноза первичной ID. К ним относятся лекарства (например, кортикостероиды, иммунодепрессанты, химиотерапия, некоторые противоэпилептические препараты), инфекционные заболевания [инфекция вируса иммунодефицита человека (ВИЧ), вирус Эпштейна-Барра (ВЭБ), врожденные инфекции краснухи / цитомегаловируса (ЦМВ) / токсоплазмы], опухоли. (в частности, хронический лимфолейкоз, неходжкинская лимфома, тимома) и синдромы, связанные с чрезмерной потерей белка (нефротический синдром, синдром мальабсорбции, лимфангиэктазия).Системная терапия кортикостероидами более 20 мг / день может привести к стойкому снижению уровня IgG в сыворотке [9].
(в частности, хронический лимфолейкоз, неходжкинская лимфома, тимома) и синдромы, связанные с чрезмерной потерей белка (нефротический синдром, синдром мальабсорбции, лимфангиэктазия).Системная терапия кортикостероидами более 20 мг / день может привести к стойкому снижению уровня IgG в сыворотке [9].
Другие проявления иммунодефицита
Помимо восприимчивости к инфекции, важно знать, что другие признаки нарушения иммунной системы могут быть связаны с ID. К ним относятся хроническое воспаление, аутоиммунитет и лимфопролиферативные расстройства, которые кратко изложены в рекомендациях AWMF немецкой мнемоники GARFIELD [4]:
-
Гранулемы (Granulome): в частности, в легких, лимфатических узлах, коже, а также в других органах
-
Аутоиммунитет (аутоиммунитет): в частности аутоиммунная цитопения, а также аутоиммунитет органов
- лихорадка (Rezidivierendes Fieber): периодическая лихорадка, гемофагоцитоз и др.
-
Экзема (Экземе): часто с ранним началом, атипичная, рефрактерная к терапии
-
Лимфопролиферативные расстройства (лимфопролиферация, лимфопролиферация, лимфопролиферация): хроническая доброкачественная лимфопролиферация.
 и)
и) Средостенная лимфаденопатия при общем вариабельном иммунодефиците (ОВИН). Компьютерная томография (КТ) грудной клетки
Выраженная спленомегалия при общем вариабельном иммунодефиците (ОВИН), достигающая почти нижнего полюса почек. Компьютерная томография (КТ) грудной клетки / живота, коронарный разрез
© (2) Springer Medizin
-
Воспалительное заболевание кишечника (Darmentzündung): часто с ранним началом, атипичное, невосприимчивое к терапии (рис.)
Хроническое воспалительное заболевание кишечника, подобное болезни Крона, при общем вариабельном иммунодефиците (ОВИН).Колоскопия
Этот тип иммунной дисрегуляции нередко проявляется до того, как становится очевидной восприимчивость к инфекции, поэтому дифференциальный диагноз ID необходимо учитывать у некоторых пациентов с аутоиммунной цитопенией, глютеновой болезнью, подобной глютеновой. независимая энтеропатия, кишечное заболевание, подобное болезни Крона, или саркоидоподобное гранулематозное воспаление. Хотя иммунный дефект подозревается раньше в случае повышенной восприимчивости к инфекциям, диагностическое обследование ID часто откладывается у пациентов с иммунной дисрегуляцией.Дефицит антител может быть вторичным, как при лимфомах, или быть вызванным основным заболеванием с последующим (вторичным) развитием лимфомы. В этом контексте может быть сложно, как клинически, так и даже гистологически, различить хроническую доброкачественную лимфаденопатию, связанную с ID, и злокачественную лимфому.
Хотя иммунный дефект подозревается раньше в случае повышенной восприимчивости к инфекциям, диагностическое обследование ID часто откладывается у пациентов с иммунной дисрегуляцией.Дефицит антител может быть вторичным, как при лимфомах, или быть вызванным основным заболеванием с последующим (вторичным) развитием лимфомы. В этом контексте может быть сложно, как клинически, так и даже гистологически, различить хроническую доброкачественную лимфаденопатию, связанную с ID, и злокачественную лимфому.
Первичный иммунодефицит с повышенным уровнем IgE или аллергическими проявлениями
Специфические, редкие ID, демонстрирующие раннее проявление хронической экземы, высокий общий IgE (синдром гипер-IgE, синдром Вискотта-Олдрича, синдром Оменна) или холодовая крапивница (мутация PLCG2). особый интерес для аллергологов.
Клиническое различие между истинной атопической экземой и синдромом гипер-IgE (HIES), возникающим в результате аутосомно-доминантных мутаций в гене STAT3, иногда может быть сложной задачей. Сами по себе уровни IgE в сыворотке не позволяют провести здесь различие [10]. Более того, в обоих случаях наблюдаются положительный семейный анамнез, обычно обширная экзема и эозинофилия крови. Напротив, пневмония, абсцессы и кандидозные инфекции (особенно в сочетании) типичны для HIES, тогда как при атопической экземе они возникают по большей части как отдельные явления.Эмпиемы, «внутренние» абсцессы (например, печени, лимфатических узлов, периренал) и тяжелые осложнения инфекций, такие как бактериальный менингит или остеомиелит у пациентов с экземой, наблюдаются почти исключительно при HIES. Характерные черты лица (широкий нос, высокое нёбо), гиперслабость суставов и проблемы со сменой зубов являются важными клиническими признаками дефицита STAT3, тогда как истинный атопический диатез крайне редко встречается при дефиците STAT3 [11]. Таким образом, повышенная или необычная восприимчивость к инфекциям у пациентов с экземой должна побуждать к рассмотрению HIES.Диагностическая шкала была разработана для дифференциации STAT3 от других заболеваний с высоким уровнем общего IgE [12].
Сами по себе уровни IgE в сыворотке не позволяют провести здесь различие [10]. Более того, в обоих случаях наблюдаются положительный семейный анамнез, обычно обширная экзема и эозинофилия крови. Напротив, пневмония, абсцессы и кандидозные инфекции (особенно в сочетании) типичны для HIES, тогда как при атопической экземе они возникают по большей части как отдельные явления.Эмпиемы, «внутренние» абсцессы (например, печени, лимфатических узлов, периренал) и тяжелые осложнения инфекций, такие как бактериальный менингит или остеомиелит у пациентов с экземой, наблюдаются почти исключительно при HIES. Характерные черты лица (широкий нос, высокое нёбо), гиперслабость суставов и проблемы со сменой зубов являются важными клиническими признаками дефицита STAT3, тогда как истинный атопический диатез крайне редко встречается при дефиците STAT3 [11]. Таким образом, повышенная или необычная восприимчивость к инфекциям у пациентов с экземой должна побуждать к рассмотрению HIES.Диагностическая шкала была разработана для дифференциации STAT3 от других заболеваний с высоким уровнем общего IgE [12].
В качестве второй группы ID, демонстрирующей повышенный общий IgE, здесь заслуживают упоминания комбинированные иммунные дефекты, которые вызывают нарушение регуляции Т-клеток. Особого внимания в этом контексте заслуживает аутосомно-рецессивный дефицит DOCK8, который обычно вызывает повышенную восприимчивость к инфекциям вируса папилломы человека (ВПЧ), вирусов герпеса, контагиозного моллюска, кандиды и бактериальных респираторных инфекций [13].В отличие от дефицита STAT3, клиническая картина здесь часто включает истинную атопию с тяжелой экземой, астмой и преимущественной сенсибилизацией к пищевым аллергенам [10].
Помимо сочетания рецидивирующих инфекций и хронической экземы с ранним началом, Синдром Вискотта-Олдрича (WAS) преимущественно характеризуется тяжелой тромбоцитопенией. Поскольку дефекты белка WAS (WASP) наследуются рецессивным образом, сцепленным с Х-хромосомой, поражаются почти только мальчики. Все эффекторные клетки иммунной системы вовлечены в WAS, что делает его комбинированным иммунным дефектом, как в случае с синдромом Omenn (OS) [14]. ОС представляет собой клинически отличный вариант тяжелой комбинированной ID (SCID), включающей гипоморфные мутации в генах RAG. ОВ проявляется уже в первые месяцы жизни из-за оппортунистических инфекций и генерализованной экземы с сопутствующей эозинофилией крови и повышенным общим IgE. Нарушение созревания Т-клеток с олигоклонально ограниченным репертуаром Т-клеток и значительное нарушение развития центральной толерантности в тимусе приводит к обширным аутоиммунным явлениям (алопеции, лимфаденопатии, гепатоспленомегалии и т. Д.). OS также имеет мрачный прогноз, учитывая, что основные проблемы с толерантностью препятствуют восстановлению иммунитета после трансплантации аллогенных стволовых клеток.
ОС представляет собой клинически отличный вариант тяжелой комбинированной ID (SCID), включающей гипоморфные мутации в генах RAG. ОВ проявляется уже в первые месяцы жизни из-за оппортунистических инфекций и генерализованной экземы с сопутствующей эозинофилией крови и повышенным общим IgE. Нарушение созревания Т-клеток с олигоклонально ограниченным репертуаром Т-клеток и значительное нарушение развития центральной толерантности в тимусе приводит к обширным аутоиммунным явлениям (алопеции, лимфаденопатии, гепатоспленомегалии и т. Д.). OS также имеет мрачный прогноз, учитывая, что основные проблемы с толерантностью препятствуют восстановлению иммунитета после трансплантации аллогенных стволовых клеток.
Пациенты со стойкой холодовой крапивницей, дефицитом антител (IgA / IgM) с частыми респираторными инфекциями и аутоиммунными явлениями (аутоиммунный тиреоидит, повышенные титры антинуклеарных антител [ANA]) могут страдать от чрезвычайно редкого дефекта фосфолипазы-Cγ2 (PLCCG2), впервые описанный в 2012 году [15], который, как молекула передачи сигнала в В-клетках, естественных клетках-киллерах и тучных клетках, играет важную роль в иммунорегуляции.
Общий вариабельный иммунодефицит
Синдром ОВИН — это синдром дефицита антител, который представляет собой наиболее частую форму симптоматического ID во взрослом возрасте, с точечной распространенностью от 1:25 000 до 1:75 000, в зависимости от исследуемой группы населения [3, 16] . Распространенность примерно одинакова у мужчин и женщин. Хотя изолированный дефицит IgA с показателем распространенности 1: 225–1: 3000 встречается чаще [17], это обычно случайный диагноз и обычно остается бессимптомным на протяжении всей жизни.В отличие от многих других первичных ID, CVID часто диагностируется в зрелом возрасте, преимущественно в возрасте от 20 до 40 лет, и обычно с латентным периодом около 4 лет между первоначальным проявлением и первым диагнозом.
Точная причина ОВИН в большинстве случаев остается неясной, хотя тем временем были описаны отдельные генные дефекты. Эти мутации влияют, например, на например, костимулирующие молекулы линии В-клеток (CD19, CD21, CD81, TACI и BAFF-R) [16]. Процесс созревания В-клеток до продуцирующих антитела плазматических клеток нарушен у большинства пациентов [18, 18].Табл. 4 резюмирует новые критерии, выпущенные Европейским обществом иммунодефицитов (ESID) для диагностики CVID [20].
Таблица 4
Диагностические критерии ESID для CVID [19]
| ОВИН диагностируется при соблюдении хотя бы одного из следующих критериев: | |
| _ Повышенная восприимчивость к инфекциям _ Аутоиммунные проявления _ Гранулематозная болезнь _ Необъяснимая поликлональная лимфопролиферация _ Другие члены семьи с дефицитом антител |
|
| и | Дефицит IgG и IgA как минимум на два стандартных отклонения ниже среднего соответствующего уровня (не нижней нормы!), Со сниженным IgM или без него, обнаруженный как минимум в двух измерениях |
| и | По крайней мере, один из следующих критериев: |
| _ Неспособность обнаружить значительный рост специфических IgG после вакцинации (и / или отсутствия изогемагглютининов), i.е., неспособность достичь защитного уровня IgG, где это определено _ Низкое количество B-клеток памяти с переключением классов (<70%, скорректированное по возрасту стандартное значение) |
|
| и | Исключение вторичных причин гипогаммаглобулинемии (см. Текст) |
| и | Диагностика заболевания после 4 лет (возможны предыдущие симптомы) |
| и |
№ № указание на выраженную недостаточность Т-клеток, определяемую двумя из следующих критериев: _ количество хелперных клеток CD4: 2–6 лет, <300 / мкл; 6–12 лет <250 / мкл; > 12 лет, <200 / мкл _% Наивные клетки-помощники CD4: 2–6 лет, <25%; 6–16 лет, <20%; > 16 лет <10% _ Отсутствие пролиферации Т-клеток in vitr |
Диагностический подход при подозрении на иммунодефицит
Поэтапный подход к диагностике иммунных дефектов:
-
Скрининг
В рамках этого процесса должен быть низкий порог для рентабельных методов скрининга, т.е.е., даже в случае низкой клинической подозрительности. Более подробный анализ иммунной системы (включая определение подкласса IgG), который часто технически сложен и дорог, следует проводить в специализированных клиниках или центрах.
На первом этапе клиническая картина определяет выбор скрининга: дифференциальный анализ крови (нейтропения? Моноцитопения?) При подозрении на врожденный иммунный дефект; в случае подозрения на клеточный дефект в дополнение к общему анализу крови требуется абсолютное количество хелперных клеток CD4, соотношение CD4: CD8 и скрининговый тест на ВИЧ.Любое указание в анамнезе пациента на гуморальный иммунный дефект следует исследовать путем количественного измерения сывороточных антител IgG, IgA и IgM. Эти исследования являются экономически эффективными (определение иммуноглобулинов, исключая подклассы: 4 евро в Германии, 18 sFr в Швейцарии) и могут значительно сократить часто длительные страдания пациентов до постановки диагноза и эффективного лечения. Повторение этих тестов в течение 1–6 месяцев необходимо, чтобы избежать классификации постинфекционной или преходящей гипогаммаглобулинемии (например,г., в младенчестве) как ID. При анализе результатов важно учитывать возрастную зависимость нормальных показателей, включая иммуноглобулины.
Совместное принятие решений лечащим врачом и специализированным центром о дальнейших диагностических шагах в каждом конкретном случае помогает избежать ненужных исследований и затрат, с одной стороны, обеспечивая при этом выполнение иногда технически сложных функциональных иммунологических тестов. на качественно высоком уровне. Многие из более специализированных лабораторных исследований могут проводиться на образцах крови, отправленных экспресс-почтой.
При подозрении на моногенетический дефект и соответствующей терапевтической значимости рекомендуется подтверждение с помощью генетического анализа. С другой стороны, в случае ОВИН с отрицательным семейным анамнезом генетическая диагностика в настоящее время не рекомендуется, поскольку на лечение (пока) не влияют результаты.
Лечение
В дополнение к общим мерам, включая оптимальную гигиену (рук) и уход за зубами, предотвращение передачи за счет улучшения барьерной защиты (увлажняющие / смягчающие средства кожи, местное лечение инфекций верхних дыхательных путей, включая сосудосуживающие капли для носа, полоскания солевым раствором, возможное предотвращение больших толпы людей), а также быстрое и целенаправленное применение антибиотиков в случае бактериальных инфекций, пациенты с иммунодефицитом (особенно в случае дефектов комплемента и асплении) должны последовательно проходить все рекомендованные вакцинации.Здесь следует отметить, что живые прививки при ИН противопоказаны. Заместительная терапия иммуноглобулином обеспечивает хорошую пассивную защиту от классических патогенов, указанных в национальных планах вакцинации (столбняк, дифтерия и т. Д.), Против которых не требуется дополнительная вакцинация. С другой стороны, ежегодные вакцины против гриппа в случаях, когда есть остаточная способность к иммунному ответу, безусловно, имеют смысл, поскольку можно предположить, что в препаратах иммуноглобулинов отсутствуют защитные антитела.Местные и национальные рекомендации по вакцинам, в том числе для групп риска, таких как ID, можно получить на следующих сайтах для конкретных стран:
Специфические меры лечения определяются видом иммунного дефекта; поэтому мы можем предоставить только обзор общих принципов лечения.
В случае гуморального ID замещение IgG является наиболее важной формой лечения. Его можно вводить внутривенно в начальной дозе 0,4 г / кг массы тела (МТ) (ок.20-25 г / 3-4 недели) в кабинете врача или подкожно с недельными интервалами самими пациентами (начальная доза 0,1 г / кг МТ в неделю). Перед первоначальным введением пациента необходимо проинформировать о том, что он получает продукт крови и о связанных с ним побочных эффектах. Доступные препараты иммуноглобулинов соответствуют фармацевтическим требованиям, и с 1994 г. в Европе и США не было зарегистрировано случаев передачи патогенов через препараты иммуноглобулинов [21].
В случае подкожного замещения пациенты проходят инструктаж по самостоятельному введению с помощью микронасоса и набора стерильных игл перед тем, как самостоятельно вводить препарат в домашних условиях. Домашняя терапия дополняется контрольными осмотрами каждые 3–6 месяцев лечащим врачом. Доза корректируется в соответствии с индивидуальными потребностями пациента в течение курса терапии с целью достижения статуса безинфекционного состояния. Важным клиническим исключением здесь является хронический риносинусит, который может сохраняться, несмотря на лечение.Целевой уровень сывороточного IgG 7 г / л, обычно используемый лабораторный суррогатный маркер для адекватного замещения, не может применяться универсально для всех пациентов. Увеличение дозы с получением минимальных уровней IgG в сыворотке крови в диапазоне 10–12 г / л необходимо в некоторых случаях для достижения статуса отсутствия инфекции.
При других формах ID или в случае гуморального ID, резистентного к терапии, требуется длительная антибиотикопрофилактика в качестве единственного лечения или в сочетании с заменой иммуноглобулинов.
-
Котримоксазол 960 мг (3 раза в неделю) при комбинированном ID (количество CD4-клеток <200 / мкл)
-
Пенициллин (2 x 1 млн IE / день) у пациентов с спленэктомией
-
Ципрофлоксацин в тяжелой форме нейтропения (дополнительно, гранулоцитарный колониестимулирующий фактор [G-CSF])
-
Ингаляции тобрамицина или колистина при муковисцидозе и осложненных бронхоэктазах
-
Итраконазол (2 х 100 мг) и котримуломатозол
в сутки, септик гранулометрический гранулометрический 960 мг / сут 960 мг / сут.
Инфекции могут возникать даже при замене иммуноглобулинов.Симптомы острой инфекции требуют быстрого выявления с низким порогом начала антибактериальной терапии. Важно, чтобы все лечащие коллеги знали, что серологический диагноз инфекций у пациентов с ОВИН недействителен из-за нарушения образования антител. В этих условиях прямое обнаружение патогенов с использованием гистологии, посева или полимеразной цепной реакции (ПЦР) является единственными надежными диагностическими вариантами. Перед хирургическим и стоматологическим вмешательством следует рассмотреть вопрос о профилактике антибиотиками.
В случае некоторых иммунных дефектов, в частности клеточного ID, только «замена» иммунной системы посредством трансплантации стволовых клеток является эффективным и причинным лечением. Генная терапия является вариантом в конкретных случаях четко определенных иммунных дефектов, особенно при отсутствии подходящего донора. Хотя трансплантация стволовых клеток является стандартной процедурой для детей с ТКИД, она считается экспериментальным подходом к лечению взрослых с врожденными иммунными дефектами и ограничивается отдельными случаями, которые оказываются сложными и не поддаются лечению.Важно, чтобы специализированные центры участвовали как в показаниях, так и в назначении этого лечения.
Систематическая регистрация пациентов с первичными иммунными дефектами лечащим врачом в регистрах, таких как Европейский регистр ESID (www.esid.org), помогает создать научную основу для улучшения нашего понимания этих сложных и редких заболеваний, в частности их клинических проявлений. течение и клиническое значение предупреждающих знаков, описанных выше.
Помимо медицинского обслуживания, некоторые пациенты получают выгоду от сетевых возможностей, предлагаемых организациями пациентов и заинтересованных сторон, которые способствуют общению, организуют публичные лекции и предлагают множество практических советов о том, как справиться с ID в повседневной жизни.Их можно найти в разделе:
Немецкие центры экспертизы в области ID создали сеть FIND-ID (www.find-id.net) для обеспечения непрерывного обмена информацией между существующими центрами, клиниками и врачами, тем самым способствуя раннему выявлению и лечение пациентов с врожденным ID — цель, полностью поддерживаемая настоящей статьей.
Сокращения
| ANA | Антиядерные антитела | |
| AWMF | Немецкая ассоциация научных медицинских обществ (Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V) | |
| CMV | Цитомегаловирус | |
| CVID | Общий вариабельный иммунодефицит, синдром вариабельного иммунодефицита | |
| EBV | Вирусы Эпштейна-Барра | |
| ESID | Европейское общество G-CSF | Гранулоцитарный колониестимулирующий фактор |
| HIES | Синдром гипер-IgE | |
| ВИЧ | Вирус иммунодефицита человека | |
| ВПЧ | Вирус папилломы человека | 70 Идентификатор иммунитета | 70 |
| Ig | Иммуноглобулин | |
| IL | Интерлейкин | |
| IUIS | Международный союз иммунологических обществ | |
| OS | Синдром Оменна | |
| ПЦР-цепочка реферазы | ction | |
| SCID | Тяжелый комбинированный иммунодефицит | |
| SD | Стандартное отклонение | |
| Th | Т-хелперные клетки | |
| WAS | Синдром Вискотта-Олдрича | |
| Синдром Wiskott-Aldrich | ||
| белок |
Сноски
Конфликт интересов
Автор корреспонденции заявляет, что конфликта интересов нет.Профессор доктор Варнац получал гонорары от компаний Baxter, CSL Behring, Octapharma и Biotest.
Укажите это как
Хаусманн О., Варнац К. Иммунодефицит у взрослых: практическое руководство для аллерголога. Allergo J Int 2014; 23: 261–8 DOI: 10.1007 / s40629-014-0030-4
Ссылки
1. Peter HH, Pichler WJ, Müller-Ladner U, eds. Klinische Immunologie. 3. Aufl. Мюнхен — Эльзевир; 2012
2. Аль-Херц В., Бусфиха А., Казанова Дж. Л., Шатила Т., Конли М.Э., Каннингем-Рандлс С. и др.Болезни первичного иммунодефицита: обновленная информация о классификации комитета экспертов международного союза иммунологических обществ по первичному иммунодефициту. Фронт Иммунол. 2014; 5: 162. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Гатманн Б., Махлауи Н., Жерар Л., Оксенхендлер Э., Варнац К., Шульце И. и др. Клиника и лечение 2212 больных общим вариабельным иммунодефицитом. J Allergy Clin Immunol. 2014; S0091-6749 (14): 00029–3. [PubMed] [Google Scholar] 4. Farmand S, Baumann U, Bernuth H, Borte M, Foerster-Waldl E, Franke K и др.Ассоциация научных медицинских обществ Германии (AWMF). [Междисциплинарное руководство AWMF по диагностике первичного иммунодефицита] Клин Падиатр. 2011; 223: 378–85. DOI: 10,1055 / с-0031-1287835. [PubMed] [CrossRef] [Google Scholar] 5. Силлевис Смитт JH, Kuijpers TW. Кожные проявления первичного иммунодефицита. Curr Opin Pediatr. 2013; 25: 492–7. DOI: 10.1097 / MOP.0b013e3283623b9f. [PubMed] [CrossRef] [Google Scholar] 6. Monto AS, Napier JA, Metzner HL. Исследование респираторных заболеваний Текумсе.I. План исследования и наблюдения за синдромами ОРЗ. Am J Epidemiol. 1971; 94: 269–79. [PubMed] [Google Scholar] 7. Fleming DW, Cochi SL, Hightower AW, Broome CV. Инфекции верхних дыхательных путей в детском возрасте: в какой степени посещаемость детских садов влияет на заболеваемость? Педиатрия. 1987. 79: 55–60. [PubMed] [Google Scholar] 8. Monto AS, Салливан KM. Epidemiol Infect. 1993. Острое респираторное заболевание в обществе. Частота заболевания и вовлеченные агенты; С. 110145–60. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Кавано Т., Мацусе Х, Обасе Й, Кондо Й, Мачида I, Томари С. и др. Гипогаммаглобулинемия у стероид-зависимых астматиков коррелирует с суточной дозой перорального преднизолона. Int Arch Allergy Immunol. 2002; 128: 240–3. DOI: 10,1159 / 000064258. [PubMed] [CrossRef] [Google Scholar] 10. Боос А.С., Хагл Б., Шлезингер А., Хальм Б.Е., Балленбергер Н., Пинарчи М. и др. Атопический дерматит, синдромы STAT3- и DOCK8-гипер-IgE различаются по типу сенсибилизации на основе IgE. Аллергия. 2014; 69: 943–53. DOI: 10.1111 / все.12416. [PubMed] [CrossRef] [Google Scholar] 11. Schimke LF, Sawalle-Belohradsky J, Roesler J, Wollenberg A, Rack A, Borte M и др. Диагностический подход к синдромам гипер-IgE: ключевые иммунологические и клинические данные для дифференциации синдромов гипер-IgE от атопического дерматита. J Allergy Clin Immunol. 2010; 126: 611–7. DOI: 10.1016 / j.jaci.2010.06.029. [PubMed] [CrossRef] [Google Scholar] 12. Woellner C, Gertz EM, Schaffer AA, Lagos M, Perro M, Glocker EO и др. Мутации в STAT3 и рекомендации по диагностике синдрома гипер-IgE.J Allergy Clin Immunol. 2010; 125: 424–32. DOI: 10.1016 / j.jaci.2009.10.059. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Альберт MH, Notarangelo LD, Ochs HD. Клинический спектр, патофизиология и лечение синдрома Вискотта-Олдрича. Curr Opin Hematol. 2011; 18: 42–8. DOI: 10.1097 / MOH.0b013e32834114bc. [PubMed] [CrossRef] [Google Scholar] 15. Омбрелло М.Дж., Реммерс Э.Ф., Сан Дж., Фриман А.Ф., Датта С., Тораби-Паризи П. и др. Холодовая крапивница, иммунодефицит и аутоиммунитет, связанные с делециями PLCG2.N Engl J Med. 2012; 366: 330–8. DOI: 10.1056 / NEJMoa1102140. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 18. Вер Ц., Кивиоя Т., Шмитт Ц., Ферри Б, Витте Т., Эрен Э. и др. Исследование EUROclass: определение подгрупп общего вариабельного иммунодефицита. Кровь. 2008; 111: 77–85. DOI: 10.1182 / кровь-2007-06-0
. [PubMed] [CrossRef] [Google Scholar] 19. ван де Вен AA, Compeer EB, van Montfrans JM, Boes M. Дефекты B-клеток при общем вариабельном иммунодефиците: передача сигналов BCR, кластеризация белков и зашитые генные мутации.Crit Rev Immunol. 2011; 31: 85–98. DOI: 10.1615 / CritRevImmunol.v31.i2.10. [PubMed] [CrossRef] [Google Scholar] 21. Krudewig J, Baumann U, von Bernuth H, Borte M, Burkhard-Meier U, Dueckers G, et al. [Междисциплинарное руководство AWMF по лечению первичной недостаточности антител] Klin Padiatr. 2012; 224: 404–15. DOI: 10,1055 / с-0032-1323837. [PubMed] [CrossRef] [Google Scholar]
Иммунодефицит у взрослых практическое руководство для аллерголога
Allergo J Int. 2014; 23 (7): 261–268.
и
Оливер Хаусманн
Аллерголого-иммунологическая поликлиника, Университетская клиника ревматологии, клинической иммунологии и аллергологии, Больница Бернского университета, 3010 Берн, Швейцария
Варнац
Центр хронического иммунодефицита (CCI), Университетская клиника Фрайбурга, Фрайбург, Германия
Аллергико-иммунологическая поликлиника, Университетская клиника ревматологии, клинической иммунологии и аллергологии, Больница Бернского университета
, Бернский университет, Швейцария
, Берн, 30104 Люцерн, Швейцария
Центр хронического иммунодефицита (CCI), Университетская клиника Фрайбурга, Фрайбург, Германия
Автор, отвечающий за переписку.
Поступило 28 апреля 2014 г .; Принято 21 июля 2014 г.
Эта статья цитировалась в других статьях в PMC.
Abstract
Знание клинических признаков иммунодефицита (ИД) в зрелом возрасте имеет решающее значение для раннего выявления более 200 форм первичного ИД, известных на сегодняшний день. Многие из этих врожденных заболеваний генетического происхождения проявляются уже в детстве. Заболевания, связанные с недостаточностью антител, представляют собой важное исключение, при этом наиболее распространенной формой ID является общий вариабельный иммунодефицит (ОВИН).Средний возраст возникновения ОВИН составляет 24 года. К сожалению, задержка постановки диагноза все еще превышает 4 года. Врачи общей практики, а также аллергологи играют особенно важную роль в раннем выявлении. Пациенты с ID, которые обращаются в основном с признаками нарушения иммунной регуляции, представляют собой еще большую диагностическую проблему. Таким образом, аутоиммунная цитопения, воспалительные заболевания кишечника или саркоидоподобное гранулематозное воспаление могут быть первым проявлением почти у 20% пациентов с ИН. Вторичные формы удостоверений личности [e.g., из-за длительного лечения кортикостероидами, ВИЧ-инфекцию, лейкоз, лимфому, нефротический синдром, синдром мальабсорбции] необходимо дифференцировать от первичной недостаточности антител.
Учитывая совпадение с аллергическими симптомами [ID, сопровождающийся предрасположенностью к экземе, повышенным общим IgE, эозинофилией в крови], в настоящей статье обсуждаются клинические предупреждающие признаки ID, первые необходимые диагностические шаги и возможность дальнейшей диагностической работы. в специализированных центрах для сложных случаев, а также варианты лечения для таких случаев.
Ключевые слова: иммунодефицит, иммунодефицит, предупреждающие признаки, раннее выявление, терапия, иммуноглобулин, аутоиммунитет
Введение
В эпоху, когда продвигаются пищевые добавки, витаминные препараты и широкий спектр форм дополнительной медицинской терапии аргументом в пользу того, что они укрепляют и стимулируют иммунную систему — и учитывая, что реакция на эту рекламу предполагает, что есть большое количество людей, которые явно считают свою иммунную систему слабой, или которые чувствуют себя неуверенно или в целом хрупкими, — это важно для опытный врач-специалист, интересующийся иммунологией, чтобы установить ясность в отдельных случаях и ответить на потребности пациентов в совете и заверении с помощью целевой и экономичной диагностики.
В данной обзорной статье освещаются клинически значимые предупреждающие признаки иммунодефицита (ИД) и обсуждаются шаги, которые помогут в его диагностике и когда эти шаги следует предпринять. Статья намеренно ограничивается формами удостоверения личности у взрослых. Обзор более 200 первичных иммунных дефектов, описанных в настоящее время у детей и взрослых в значительной степени генетического происхождения, можно найти в других источниках [1, 2]. Классификация первичных иммунных дефектов IUIS (Международный союз иммунологических обществ) [2] представила текущий обзор этой группы заболеваний (табл.1). Большинство врожденных первичных иммунных дефектов проявляется в детстве. Заметным исключением здесь являются болезни, связанные с недостаточностью антител (группа 3 по классификации IUIS), в частности общий вариабельный иммунодефицит (ОВИН), который проявляется в среднем в возрасте 24 лет [3, 4]. Как наиболее распространенная форма идентификатора, CVID будет обсуждаться более подробно ниже. Обсуждается также совпадение с аллергическими заболеваниями, а также возможность дальнейшей диагностики сложных случаев в специализированных центрах.
Таблица 1
Классификация IUIS и разделение на группы болезней [2]
| 1. Комбинированный Т- и В-клеточный иммунодефицит |
| 2. Комбинированный иммунодефицит с ассоциированными или синдромальными признаками |
| 3. Преимущественно недостаточность антител |
| 4. Заболевания иммунной дисрегуляции |
| 5. Врожденные дефекты количества и / или функции фагоцитов |
| 6.Нарушения естественного иммунитета (врожденный иммунитет) |
| 7. Аутовоспалительные расстройства |
| 8. Дефицит комплемента |
Клинические проявления иммунодефицитов
Иммунная защита организма начинается с анатомических барьеров, т.е. е., кожа и слизистые оболочки. Даже у иммунокомпетентных людей здесь возникает большинство инфекций. Обеспокоенность возникает, когда инфекции, вызываемые типичными патогенами, такими как пневмококки, стафилококки или сальмонеллы, развиваются сложным и длительным течением или когда эти анатомические барьеры неоднократно нарушаются.Инфекции в необычных местах, а также инфекции, вызванные практически безвредными патогенами, с которыми иммунная система обычно способна справиться, так называемыми условно-патогенными микроорганизмами, такими как микобактерии, Candida или Pneumocystis jirovecii, должны вызывать беспокойство. В таких случаях одно только обнаружение патогена, независимо от клинического течения, должно указывать на ИД. Во всех вышеупомянутых случаях следует начать дальнейшие исследования для установления иммунного статуса пациента.
Тщательный сбор анамнеза пациентов с прошлыми инфекциями имеет решающее значение для любой оценки иммунокомпетентности.
Направленные вопросы используются для записи типа, локализации, частоты и серьезности инфекций. В некоторых случаях этот шаг уже позволяет отличить ID от вторичной восприимчивости к инфекциям из-за локальных нарушений барьера кожи и слизистых оболочек. Таким образом, особенно в случае очаговых инфекций, таких как рецидивирующие инфекции мочевыводящих путей или хронический риносинусит или бронхит, необходимо учитывать местные неиммунологические нарушения защитных механизмов организма или анатомические аномалии.Примеры общей вторичной восприимчивости к инфекциям, не являющимся результатом ID, перечислены в Табл. 2. Особого внимания в этом контексте заслуживает атопический диатез, который из-за аллерген-опосредованных поражений слизистой оболочки иногда связан с повышенной восприимчивостью к инфекциям дыхательных путей и желудочно-кишечным симптомам. Эту причину необходимо исключить до проведения иммунологического обследования.
Таблица 2
Предрасположенность к инфекции без основного иммунодефицита
| Расположение | Причина |
|---|---|
| Кожа | Барьерное нарушение при атопической экземе, ожогах и т. Д. |
| Дыхательные пути | Курение, сухость слизистых оболочек, аллергия Бронхоэктатическая болезнь, муковисцидоз Нарушение вентиляции придаточных пазух носа и среднего уха, дисфагия, свищи |
| Кишечный тракт | Ингибиторы протонной помпы (снижение желудочной кислоты) Нарушение на фоне антибактериальной терапии |
| Мочевыводящие пути | Рефлюкс, стеноз, остаточная моча, половой акт, сухость слизистой между мочевыводящими путями и кишечником |
| Инородные тела | Катетер, протезы |
При наличии удостоверения личности, тип инфекции может определять тип иммунного дефекта.Рецидивирующие бактериальные инфекции дыхательных путей и желудочно-кишечного тракта особенно указывают на гуморальный иммунный дефект (дефицит антител, дефект комплемента). С другой стороны, необычная (условно-патогенная) инфекция указывает, в частности, на клеточный иммунный дефект, как, например, при ВИЧ-инфекциях. Стойкое образование абсцесса, особенно при поражении внутренних органов, системных грибковых инфекциях или остеомиелите, может быть результатом дисфункции нейтрофилов / макрофагов (нарушение фагоцитоза, нейтропения).С другой стороны, кожно-слизистый кандидоз, ограниченный кожей и слизистыми оболочками, свидетельствует об особом дефекте Т-клеток, продуцирующих интерлейкин (ИЛ) -17 (дефицит Th-17) [5].
По этой причине классические предупреждающие знаки ID были сформулированы и обобщены для пациентов с повышенной восприимчивостью к инфекции в немецкой мнемонике ELVIS от имени Немецкой ассоциации научных медицинских обществ (AWMF, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften е.V., www.awmf.org) [4]. Хотя эти предупреждения не являются исчерпывающими и конкретными, они могут помочь практикующему врачу:
-
Патоген (Эррегер): Инфекции, вызванные условно-патогенными микроорганизмами, такими как Pneumocystis jirovecii (рис.), Должны вызывать подозрение на ИН.
Двусторонняя интерстициальная пневмония с Pneumocystis jirovecii , преимущественно при комбинированном иммунодефиците
© (4) Springer Medizin
-
Локализация (локализация): атипичная локализация инфекции, например.g., абсцесс мозга, вызванный Aspergillus (рис.), церебральный токсоплазмоз или пневмококковый артрит, наводят на мысль о ID.
Инвазивный аспергиллез с абсцессом головного мозга в правой теменно-затылочной доле. 2b: Гистология с прямым обнаружением патогенов, преимущественно при комбинированных иммунных дефектах и WAS
-
Курс (Verlauf): необычное течение с точки зрения хроничности / рецидива и неудовлетворительный ответ на терапию антибиотиками представляют признаки (хотя трудно дифференцировать) ID .
-
Интенсивность (Intensität): То же самое относится к инфекциям, которые имеют необычно тяжелое течение.
-
Количество инфекций (Summe der Infektionen): этот параметр явно зависит от возраста: ≥ 8 незначительных инфекций в год, ≥ 2 случая пневмонии или тяжелого синусита в год считаются ненормальными для маленьких детей, в то время как эмпирическое правило у взрослых ≥ 3 бактериальных инфекций в год, каждая продолжительностью более 4 недель, требует дальнейшего исследования (Табл.) [6–8].
Таблица 3
Нормальное распределение частоты инфицирования у детей (изменено из [7, 8])
Возраст (лет) Респираторные инфекции / год SD Максимум <1 6,1 ± 2,6 11,3 1-2 5,7 ± 3,0 11.7 3–4 4,7 ± 2,9 10,5 5–9 5,5 ± 2,6 8,7 10–14 2,7 ± 2,2 7.2
Семейный анамнез (свидетельство генетического дефекта? Способ наследования?), А в идеале также анамнез, предоставленный третьими сторонами, например. g. родители в отношении детских инфекций и заживления пуповины или терапевт в отношении курса лечения инфекций могут помочь в диагностике ID.В случае дефицита антител (гипогаммаглобулинемия) необходимо целенаправленно искать вторичные причины до постановки диагноза первичной ID. К ним относятся лекарства (например, кортикостероиды, иммунодепрессанты, химиотерапия, некоторые противоэпилептические препараты), инфекционные заболевания [инфекция вируса иммунодефицита человека (ВИЧ), вирус Эпштейна-Барра (ВЭБ), врожденные инфекции краснухи / цитомегаловируса (ЦМВ) / токсоплазмы], опухоли. (в частности, хронический лимфолейкоз, неходжкинская лимфома, тимома) и синдромы, связанные с чрезмерной потерей белка (нефротический синдром, синдром мальабсорбции, лимфангиэктазия).Системная терапия кортикостероидами более 20 мг / день может привести к стойкому снижению уровня IgG в сыворотке [9].
Другие проявления иммунодефицита
Помимо восприимчивости к инфекции, важно знать, что другие признаки нарушения иммунной системы могут быть связаны с ID. К ним относятся хроническое воспаление, аутоиммунитет и лимфопролиферативные расстройства, которые кратко изложены в рекомендациях AWMF немецкой мнемоники GARFIELD [4]:
-
Гранулемы (Granulome): в частности, в легких, лимфатических узлах, коже, а также в других органах
-
Аутоиммунитет (аутоиммунитет): в частности аутоиммунная цитопения, а также аутоиммунитет органов
- лихорадка (Rezidivierendes Fieber): периодическая лихорадка, гемофагоцитоз и др.
-
Экзема (Экземе): часто с ранним началом, атипичная, рефрактерная к терапии
-
Лимфопролиферативные расстройства (лимфопролиферация, лимфопролиферация, лимфопролиферация): хроническая доброкачественная лимфопролиферация.и)
Средостенная лимфаденопатия при общем вариабельном иммунодефиците (ОВИН). Компьютерная томография (КТ) грудной клетки
Выраженная спленомегалия при общем вариабельном иммунодефиците (ОВИН), достигающая почти нижнего полюса почек. Компьютерная томография (КТ) грудной клетки / живота, коронарный разрез
© (2) Springer Medizin
-
Воспалительное заболевание кишечника (Darmentzündung): часто с ранним началом, атипичное, невосприимчивое к терапии (рис.)
Хроническое воспалительное заболевание кишечника, подобное болезни Крона, при общем вариабельном иммунодефиците (ОВИН).Колоскопия
Этот тип иммунной дисрегуляции нередко проявляется до того, как становится очевидной восприимчивость к инфекции, поэтому дифференциальный диагноз ID необходимо учитывать у некоторых пациентов с аутоиммунной цитопенией, глютеновой болезнью, подобной глютеновой. независимая энтеропатия, кишечное заболевание, подобное болезни Крона, или саркоидоподобное гранулематозное воспаление. Хотя иммунный дефект подозревается раньше в случае повышенной восприимчивости к инфекциям, диагностическое обследование ID часто откладывается у пациентов с иммунной дисрегуляцией.Дефицит антител может быть вторичным, как при лимфомах, или быть вызванным основным заболеванием с последующим (вторичным) развитием лимфомы. В этом контексте может быть сложно, как клинически, так и даже гистологически, различить хроническую доброкачественную лимфаденопатию, связанную с ID, и злокачественную лимфому.
Первичный иммунодефицит с повышенным уровнем IgE или аллергическими проявлениями
Специфические, редкие ID, демонстрирующие раннее проявление хронической экземы, высокий общий IgE (синдром гипер-IgE, синдром Вискотта-Олдрича, синдром Оменна) или холодовая крапивница (мутация PLCG2). особый интерес для аллергологов.
Клиническое различие между истинной атопической экземой и синдромом гипер-IgE (HIES), возникающим в результате аутосомно-доминантных мутаций в гене STAT3, иногда может быть сложной задачей. Сами по себе уровни IgE в сыворотке не позволяют провести здесь различие [10]. Более того, в обоих случаях наблюдаются положительный семейный анамнез, обычно обширная экзема и эозинофилия крови. Напротив, пневмония, абсцессы и кандидозные инфекции (особенно в сочетании) типичны для HIES, тогда как при атопической экземе они возникают по большей части как отдельные явления.Эмпиемы, «внутренние» абсцессы (например, печени, лимфатических узлов, периренал) и тяжелые осложнения инфекций, такие как бактериальный менингит или остеомиелит у пациентов с экземой, наблюдаются почти исключительно при HIES. Характерные черты лица (широкий нос, высокое нёбо), гиперслабость суставов и проблемы со сменой зубов являются важными клиническими признаками дефицита STAT3, тогда как истинный атопический диатез крайне редко встречается при дефиците STAT3 [11]. Таким образом, повышенная или необычная восприимчивость к инфекциям у пациентов с экземой должна побуждать к рассмотрению HIES.Диагностическая шкала была разработана для дифференциации STAT3 от других заболеваний с высоким уровнем общего IgE [12].
В качестве второй группы ID, демонстрирующей повышенный общий IgE, здесь заслуживают упоминания комбинированные иммунные дефекты, которые вызывают нарушение регуляции Т-клеток. Особого внимания в этом контексте заслуживает аутосомно-рецессивный дефицит DOCK8, который обычно вызывает повышенную восприимчивость к инфекциям вируса папилломы человека (ВПЧ), вирусов герпеса, контагиозного моллюска, кандиды и бактериальных респираторных инфекций [13].В отличие от дефицита STAT3, клиническая картина здесь часто включает истинную атопию с тяжелой экземой, астмой и преимущественной сенсибилизацией к пищевым аллергенам [10].
Помимо сочетания рецидивирующих инфекций и хронической экземы с ранним началом, Синдром Вискотта-Олдрича (WAS) преимущественно характеризуется тяжелой тромбоцитопенией. Поскольку дефекты белка WAS (WASP) наследуются рецессивным образом, сцепленным с Х-хромосомой, поражаются почти только мальчики. Все эффекторные клетки иммунной системы вовлечены в WAS, что делает его комбинированным иммунным дефектом, как в случае с синдромом Omenn (OS) [14].ОС представляет собой клинически отличный вариант тяжелой комбинированной ID (SCID), включающей гипоморфные мутации в генах RAG. ОВ проявляется уже в первые месяцы жизни из-за оппортунистических инфекций и генерализованной экземы с сопутствующей эозинофилией крови и повышенным общим IgE. Нарушение созревания Т-клеток с олигоклонально ограниченным репертуаром Т-клеток и значительное нарушение развития центральной толерантности в тимусе приводит к обширным аутоиммунным явлениям (алопеции, лимфаденопатии, гепатоспленомегалии и т. Д.). OS также имеет мрачный прогноз, учитывая, что основные проблемы с толерантностью препятствуют восстановлению иммунитета после трансплантации аллогенных стволовых клеток.
Пациенты со стойкой холодовой крапивницей, дефицитом антител (IgA / IgM) с частыми респираторными инфекциями и аутоиммунными явлениями (аутоиммунный тиреоидит, повышенные титры антинуклеарных антител [ANA]) могут страдать от чрезвычайно редкого дефекта фосфолипазы-Cγ2 (PLCCG2), впервые описанный в 2012 году [15], который, как молекула передачи сигнала в В-клетках, естественных клетках-киллерах и тучных клетках, играет важную роль в иммунорегуляции.
Общий вариабельный иммунодефицит
Синдром ОВИН — это синдром дефицита антител, который представляет собой наиболее частую форму симптоматического ID во взрослом возрасте, с точечной распространенностью от 1:25 000 до 1:75 000, в зависимости от исследуемой группы населения [3, 16] . Распространенность примерно одинакова у мужчин и женщин. Хотя изолированный дефицит IgA с показателем распространенности 1: 225–1: 3000 встречается чаще [17], это обычно случайный диагноз и обычно остается бессимптомным на протяжении всей жизни.В отличие от многих других первичных ID, CVID часто диагностируется в зрелом возрасте, преимущественно в возрасте от 20 до 40 лет, и обычно с латентным периодом около 4 лет между первоначальным проявлением и первым диагнозом.
Точная причина ОВИН в большинстве случаев остается неясной, хотя тем временем были описаны отдельные генные дефекты. Эти мутации влияют, например, на например, костимулирующие молекулы линии В-клеток (CD19, CD21, CD81, TACI и BAFF-R) [16]. Процесс созревания В-клеток до продуцирующих антитела плазматических клеток нарушен у большинства пациентов [18, 18].Табл. 4 резюмирует новые критерии, выпущенные Европейским обществом иммунодефицитов (ESID) для диагностики CVID [20].
Таблица 4
Диагностические критерии ESID для CVID [19]
| ОВИН диагностируется при соблюдении хотя бы одного из следующих критериев: | |
| _ Повышенная восприимчивость к инфекциям _ Аутоиммунные проявления _ Гранулематозная болезнь _ Необъяснимая поликлональная лимфопролиферация _ Другие члены семьи с дефицитом антител |
|
| и | Дефицит IgG и IgA как минимум на два стандартных отклонения ниже среднего соответствующего уровня (не нижней нормы!), Со сниженным IgM или без него, обнаруженный как минимум в двух измерениях |
| и | По крайней мере, один из следующих критериев: |
| _ Неспособность обнаружить значительный рост специфических IgG после вакцинации (и / или отсутствия изогемагглютининов), i.е., неспособность достичь защитного уровня IgG, где это определено _ Низкое количество B-клеток памяти с переключением классов (<70%, скорректированное по возрасту стандартное значение) |
|
| и | Исключение вторичных причин гипогаммаглобулинемии (см. Текст) |
| и | Диагностика заболевания после 4 лет (возможны предыдущие симптомы) |
| и |
№ № указание на выраженную недостаточность Т-клеток, определяемую двумя из следующих критериев: _ количество хелперных клеток CD4: 2–6 лет, <300 / мкл; 6–12 лет <250 / мкл; > 12 лет, <200 / мкл _% Наивные клетки-помощники CD4: 2–6 лет, <25%; 6–16 лет, <20%; > 16 лет <10% _ Отсутствие пролиферации Т-клеток in vitr |
Диагностический подход при подозрении на иммунодефицит
Поэтапный подход к диагностике иммунных дефектов:
-
Скрининг
В рамках этого процесса должен быть низкий порог для рентабельных методов скрининга, т.е.е., даже в случае низкой клинической подозрительности. Более подробный анализ иммунной системы (включая определение подкласса IgG), который часто технически сложен и дорог, следует проводить в специализированных клиниках или центрах.
На первом этапе клиническая картина определяет выбор скрининга: дифференциальный анализ крови (нейтропения? Моноцитопения?) При подозрении на врожденный иммунный дефект; в случае подозрения на клеточный дефект в дополнение к общему анализу крови требуется абсолютное количество хелперных клеток CD4, соотношение CD4: CD8 и скрининговый тест на ВИЧ.Любое указание в анамнезе пациента на гуморальный иммунный дефект следует исследовать путем количественного измерения сывороточных антител IgG, IgA и IgM. Эти исследования являются экономически эффективными (определение иммуноглобулинов, исключая подклассы: 4 евро в Германии, 18 sFr в Швейцарии) и могут значительно сократить часто длительные страдания пациентов до постановки диагноза и эффективного лечения. Повторение этих тестов в течение 1–6 месяцев необходимо, чтобы избежать классификации постинфекционной или преходящей гипогаммаглобулинемии (например,г., в младенчестве) как ID. При анализе результатов важно учитывать возрастную зависимость нормальных показателей, включая иммуноглобулины.
Совместное принятие решений лечащим врачом и специализированным центром о дальнейших диагностических шагах в каждом конкретном случае помогает избежать ненужных исследований и затрат, с одной стороны, обеспечивая при этом выполнение иногда технически сложных функциональных иммунологических тестов. на качественно высоком уровне. Многие из более специализированных лабораторных исследований могут проводиться на образцах крови, отправленных экспресс-почтой.
При подозрении на моногенетический дефект и соответствующей терапевтической значимости рекомендуется подтверждение с помощью генетического анализа. С другой стороны, в случае ОВИН с отрицательным семейным анамнезом генетическая диагностика в настоящее время не рекомендуется, поскольку на лечение (пока) не влияют результаты.
Лечение
В дополнение к общим мерам, включая оптимальную гигиену (рук) и уход за зубами, предотвращение передачи за счет улучшения барьерной защиты (увлажняющие / смягчающие средства кожи, местное лечение инфекций верхних дыхательных путей, включая сосудосуживающие капли для носа, полоскания солевым раствором, возможное предотвращение больших толпы людей), а также быстрое и целенаправленное применение антибиотиков в случае бактериальных инфекций, пациенты с иммунодефицитом (особенно в случае дефектов комплемента и асплении) должны последовательно проходить все рекомендованные вакцинации.Здесь следует отметить, что живые прививки при ИН противопоказаны. Заместительная терапия иммуноглобулином обеспечивает хорошую пассивную защиту от классических патогенов, указанных в национальных планах вакцинации (столбняк, дифтерия и т. Д.), Против которых не требуется дополнительная вакцинация. С другой стороны, ежегодные вакцины против гриппа в случаях, когда есть остаточная способность к иммунному ответу, безусловно, имеют смысл, поскольку можно предположить, что в препаратах иммуноглобулинов отсутствуют защитные антитела.Местные и национальные рекомендации по вакцинам, в том числе для групп риска, таких как ID, можно получить на следующих сайтах для конкретных стран:
Специфические меры лечения определяются видом иммунного дефекта; поэтому мы можем предоставить только обзор общих принципов лечения.
В случае гуморального ID замещение IgG является наиболее важной формой лечения. Его можно вводить внутривенно в начальной дозе 0,4 г / кг массы тела (МТ) (ок.20-25 г / 3-4 недели) в кабинете врача или подкожно с недельными интервалами самими пациентами (начальная доза 0,1 г / кг МТ в неделю). Перед первоначальным введением пациента необходимо проинформировать о том, что он получает продукт крови и о связанных с ним побочных эффектах. Доступные препараты иммуноглобулинов соответствуют фармацевтическим требованиям, и с 1994 г. в Европе и США не было зарегистрировано случаев передачи патогенов через препараты иммуноглобулинов [21].
В случае подкожного замещения пациенты проходят инструктаж по самостоятельному введению с помощью микронасоса и набора стерильных игл перед тем, как самостоятельно вводить препарат в домашних условиях. Домашняя терапия дополняется контрольными осмотрами каждые 3–6 месяцев лечащим врачом. Доза корректируется в соответствии с индивидуальными потребностями пациента в течение курса терапии с целью достижения статуса безинфекционного состояния. Важным клиническим исключением здесь является хронический риносинусит, который может сохраняться, несмотря на лечение.Целевой уровень сывороточного IgG 7 г / л, обычно используемый лабораторный суррогатный маркер для адекватного замещения, не может применяться универсально для всех пациентов. Увеличение дозы с получением минимальных уровней IgG в сыворотке крови в диапазоне 10–12 г / л необходимо в некоторых случаях для достижения статуса отсутствия инфекции.
При других формах ID или в случае гуморального ID, резистентного к терапии, требуется длительная антибиотикопрофилактика в качестве единственного лечения или в сочетании с заменой иммуноглобулинов.
-
Котримоксазол 960 мг (3 раза в неделю) при комбинированном ID (количество CD4-клеток <200 / мкл)
-
Пенициллин (2 x 1 млн IE / день) у пациентов с спленэктомией
-
Ципрофлоксацин в тяжелой форме нейтропения (дополнительно, гранулоцитарный колониестимулирующий фактор [G-CSF])
-
Ингаляции тобрамицина или колистина при муковисцидозе и осложненных бронхоэктазах
-
Итраконазол (2 х 100 мг) и котримуломатозол
в сутки, септик гранулометрический гранулометрический 960 мг / сут 960 мг / сут.
Инфекции могут возникать даже при замене иммуноглобулинов.Симптомы острой инфекции требуют быстрого выявления с низким порогом начала антибактериальной терапии. Важно, чтобы все лечащие коллеги знали, что серологический диагноз инфекций у пациентов с ОВИН недействителен из-за нарушения образования антител. В этих условиях прямое обнаружение патогенов с использованием гистологии, посева или полимеразной цепной реакции (ПЦР) является единственными надежными диагностическими вариантами. Перед хирургическим и стоматологическим вмешательством следует рассмотреть вопрос о профилактике антибиотиками.
В случае некоторых иммунных дефектов, в частности клеточного ID, только «замена» иммунной системы посредством трансплантации стволовых клеток является эффективным и причинным лечением. Генная терапия является вариантом в конкретных случаях четко определенных иммунных дефектов, особенно при отсутствии подходящего донора. Хотя трансплантация стволовых клеток является стандартной процедурой для детей с ТКИД, она считается экспериментальным подходом к лечению взрослых с врожденными иммунными дефектами и ограничивается отдельными случаями, которые оказываются сложными и не поддаются лечению.Важно, чтобы специализированные центры участвовали как в показаниях, так и в назначении этого лечения.
Систематическая регистрация пациентов с первичными иммунными дефектами лечащим врачом в регистрах, таких как Европейский регистр ESID (www.esid.org), помогает создать научную основу для улучшения нашего понимания этих сложных и редких заболеваний, в частности их клинических проявлений. течение и клиническое значение предупреждающих знаков, описанных выше.
Помимо медицинского обслуживания, некоторые пациенты получают выгоду от сетевых возможностей, предлагаемых организациями пациентов и заинтересованных сторон, которые способствуют общению, организуют публичные лекции и предлагают множество практических советов о том, как справиться с ID в повседневной жизни.Их можно найти в разделе:
Немецкие центры экспертизы в области ID создали сеть FIND-ID (www.find-id.net) для обеспечения непрерывного обмена информацией между существующими центрами, клиниками и врачами, тем самым способствуя раннему выявлению и лечение пациентов с врожденным ID — цель, полностью поддерживаемая настоящей статьей.
Сокращения
| ANA | Антиядерные антитела | |
| AWMF | Немецкая ассоциация научных медицинских обществ (Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V) | |
| CMV | Цитомегаловирус | |
| CVID | Общий вариабельный иммунодефицит, синдром вариабельного иммунодефицита | |
| EBV | Вирусы Эпштейна-Барра | |
| ESID | Европейское общество G-CSF | Гранулоцитарный колониестимулирующий фактор |
| HIES | Синдром гипер-IgE | |
| ВИЧ | Вирус иммунодефицита человека | |
| ВПЧ | Вирус папилломы человека | 70 Идентификатор иммунитета | 70 |
| Ig | Иммуноглобулин | |
| IL | Интерлейкин | |
| IUIS | Международный союз иммунологических обществ | |
| OS | Синдром Оменна | |
| ПЦР-цепочка реферазы | ction | |
| SCID | Тяжелый комбинированный иммунодефицит | |
| SD | Стандартное отклонение | |
| Th | Т-хелперные клетки | |
| WAS | Синдром Вискотта-Олдрича | |
| Синдром Wiskott-Aldrich | ||
| белок |
Сноски
Конфликт интересов
Автор корреспонденции заявляет, что конфликта интересов нет.Профессор доктор Варнац получал гонорары от компаний Baxter, CSL Behring, Octapharma и Biotest.
Укажите это как
Хаусманн О., Варнац К. Иммунодефицит у взрослых: практическое руководство для аллерголога. Allergo J Int 2014; 23: 261–8 DOI: 10.1007 / s40629-014-0030-4
Ссылки
1. Peter HH, Pichler WJ, Müller-Ladner U, eds. Klinische Immunologie. 3. Aufl. Мюнхен — Эльзевир; 2012
2. Аль-Херц В., Бусфиха А., Казанова Дж. Л., Шатила Т., Конли М.Э., Каннингем-Рандлс С. и др.Болезни первичного иммунодефицита: обновленная информация о классификации комитета экспертов международного союза иммунологических обществ по первичному иммунодефициту. Фронт Иммунол. 2014; 5: 162. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Гатманн Б., Махлауи Н., Жерар Л., Оксенхендлер Э., Варнац К., Шульце И. и др. Клиника и лечение 2212 больных общим вариабельным иммунодефицитом. J Allergy Clin Immunol. 2014; S0091-6749 (14): 00029–3. [PubMed] [Google Scholar] 4. Farmand S, Baumann U, Bernuth H, Borte M, Foerster-Waldl E, Franke K и др.Ассоциация научных медицинских обществ Германии (AWMF). [Междисциплинарное руководство AWMF по диагностике первичного иммунодефицита] Клин Падиатр. 2011; 223: 378–85. DOI: 10,1055 / с-0031-1287835. [PubMed] [CrossRef] [Google Scholar] 5. Силлевис Смитт JH, Kuijpers TW. Кожные проявления первичного иммунодефицита. Curr Opin Pediatr. 2013; 25: 492–7. DOI: 10.1097 / MOP.0b013e3283623b9f. [PubMed] [CrossRef] [Google Scholar] 6. Monto AS, Napier JA, Metzner HL. Исследование респираторных заболеваний Текумсе.I. План исследования и наблюдения за синдромами ОРЗ. Am J Epidemiol. 1971; 94: 269–79. [PubMed] [Google Scholar] 7. Fleming DW, Cochi SL, Hightower AW, Broome CV. Инфекции верхних дыхательных путей в детском возрасте: в какой степени посещаемость детских садов влияет на заболеваемость? Педиатрия. 1987. 79: 55–60. [PubMed] [Google Scholar] 8. Monto AS, Салливан KM. Epidemiol Infect. 1993. Острое респираторное заболевание в обществе. Частота заболевания и вовлеченные агенты; С. 110145–60. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Кавано Т., Мацусе Х, Обасе Й, Кондо Й, Мачида I, Томари С. и др. Гипогаммаглобулинемия у стероид-зависимых астматиков коррелирует с суточной дозой перорального преднизолона. Int Arch Allergy Immunol. 2002; 128: 240–3. DOI: 10,1159 / 000064258. [PubMed] [CrossRef] [Google Scholar] 10. Боос А.С., Хагл Б., Шлезингер А., Хальм Б.Е., Балленбергер Н., Пинарчи М. и др. Атопический дерматит, синдромы STAT3- и DOCK8-гипер-IgE различаются по типу сенсибилизации на основе IgE. Аллергия. 2014; 69: 943–53. DOI: 10.1111 / все.12416. [PubMed] [CrossRef] [Google Scholar] 11. Schimke LF, Sawalle-Belohradsky J, Roesler J, Wollenberg A, Rack A, Borte M и др. Диагностический подход к синдромам гипер-IgE: ключевые иммунологические и клинические данные для дифференциации синдромов гипер-IgE от атопического дерматита. J Allergy Clin Immunol. 2010; 126: 611–7. DOI: 10.1016 / j.jaci.2010.06.029. [PubMed] [CrossRef] [Google Scholar] 12. Woellner C, Gertz EM, Schaffer AA, Lagos M, Perro M, Glocker EO и др. Мутации в STAT3 и рекомендации по диагностике синдрома гипер-IgE.J Allergy Clin Immunol. 2010; 125: 424–32. DOI: 10.1016 / j.jaci.2009.10.059. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Альберт MH, Notarangelo LD, Ochs HD. Клинический спектр, патофизиология и лечение синдрома Вискотта-Олдрича. Curr Opin Hematol. 2011; 18: 42–8. DOI: 10.1097 / MOH.0b013e32834114bc. [PubMed] [CrossRef] [Google Scholar] 15. Омбрелло М.Дж., Реммерс Э.Ф., Сан Дж., Фриман А.Ф., Датта С., Тораби-Паризи П. и др. Холодовая крапивница, иммунодефицит и аутоиммунитет, связанные с делециями PLCG2.N Engl J Med. 2012; 366: 330–8. DOI: 10.1056 / NEJMoa1102140. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 18. Вер Ц., Кивиоя Т., Шмитт Ц., Ферри Б, Витте Т., Эрен Э. и др. Исследование EUROclass: определение подгрупп общего вариабельного иммунодефицита. Кровь. 2008; 111: 77–85. DOI: 10.1182 / кровь-2007-06-0
. [PubMed] [CrossRef] [Google Scholar] 19. ван де Вен AA, Compeer EB, van Montfrans JM, Boes M. Дефекты B-клеток при общем вариабельном иммунодефиците: передача сигналов BCR, кластеризация белков и зашитые генные мутации.Crit Rev Immunol. 2011; 31: 85–98. DOI: 10.1615 / CritRevImmunol.v31.i2.10. [PubMed] [CrossRef] [Google Scholar] 21. Krudewig J, Baumann U, von Bernuth H, Borte M, Burkhard-Meier U, Dueckers G, et al. [Междисциплинарное руководство AWMF по лечению первичной недостаточности антител] Klin Padiatr. 2012; 224: 404–15. DOI: 10,1055 / с-0032-1323837. [PubMed] [CrossRef] [Google Scholar]
Иммунодефицит у взрослых практическое руководство для аллерголога
Allergo J Int. 2014; 23 (7): 261–268.
и
Оливер Хаусманн
Аллерголого-иммунологическая поликлиника, Университетская клиника ревматологии, клинической иммунологии и аллергологии, Больница Бернского университета, 3010 Берн, Швейцария
Варнац
Центр хронического иммунодефицита (CCI), Университетская клиника Фрайбурга, Фрайбург, Германия
Аллергико-иммунологическая поликлиника, Университетская клиника ревматологии, клинической иммунологии и аллергологии, Больница Бернского университета
, Бернский университет, Швейцария
, Берн, 30104 Люцерн, Швейцария
Центр хронического иммунодефицита (CCI), Университетская клиника Фрайбурга, Фрайбург, Германия
Автор, отвечающий за переписку.
Поступило 28 апреля 2014 г .; Принято 21 июля 2014 г.
Эта статья цитировалась в других статьях в PMC.
Abstract
Знание клинических признаков иммунодефицита (ИД) в зрелом возрасте имеет решающее значение для раннего выявления более 200 форм первичного ИД, известных на сегодняшний день. Многие из этих врожденных заболеваний генетического происхождения проявляются уже в детстве. Заболевания, связанные с недостаточностью антител, представляют собой важное исключение, при этом наиболее распространенной формой ID является общий вариабельный иммунодефицит (ОВИН).Средний возраст возникновения ОВИН составляет 24 года. К сожалению, задержка постановки диагноза все еще превышает 4 года. Врачи общей практики, а также аллергологи играют особенно важную роль в раннем выявлении. Пациенты с ID, которые обращаются в основном с признаками нарушения иммунной регуляции, представляют собой еще большую диагностическую проблему. Таким образом, аутоиммунная цитопения, воспалительные заболевания кишечника или саркоидоподобное гранулематозное воспаление могут быть первым проявлением почти у 20% пациентов с ИН. Вторичные формы удостоверений личности [e.g., из-за длительного лечения кортикостероидами, ВИЧ-инфекцию, лейкоз, лимфому, нефротический синдром, синдром мальабсорбции] необходимо дифференцировать от первичной недостаточности антител.
Учитывая совпадение с аллергическими симптомами [ID, сопровождающийся предрасположенностью к экземе, повышенным общим IgE, эозинофилией в крови], в настоящей статье обсуждаются клинические предупреждающие признаки ID, первые необходимые диагностические шаги и возможность дальнейшей диагностической работы. в специализированных центрах для сложных случаев, а также варианты лечения для таких случаев.
Ключевые слова: иммунодефицит, иммунодефицит, предупреждающие признаки, раннее выявление, терапия, иммуноглобулин, аутоиммунитет
Введение
В эпоху, когда продвигаются пищевые добавки, витаминные препараты и широкий спектр форм дополнительной медицинской терапии аргументом в пользу того, что они укрепляют и стимулируют иммунную систему — и учитывая, что реакция на эту рекламу предполагает, что есть большое количество людей, которые явно считают свою иммунную систему слабой, или которые чувствуют себя неуверенно или в целом хрупкими, — это важно для опытный врач-специалист, интересующийся иммунологией, чтобы установить ясность в отдельных случаях и ответить на потребности пациентов в совете и заверении с помощью целевой и экономичной диагностики.
В данной обзорной статье освещаются клинически значимые предупреждающие признаки иммунодефицита (ИД) и обсуждаются шаги, которые помогут в его диагностике и когда эти шаги следует предпринять. Статья намеренно ограничивается формами удостоверения личности у взрослых. Обзор более 200 первичных иммунных дефектов, описанных в настоящее время у детей и взрослых в значительной степени генетического происхождения, можно найти в других источниках [1, 2]. Классификация первичных иммунных дефектов IUIS (Международный союз иммунологических обществ) [2] представила текущий обзор этой группы заболеваний (табл.1). Большинство врожденных первичных иммунных дефектов проявляется в детстве. Заметным исключением здесь являются болезни, связанные с недостаточностью антител (группа 3 по классификации IUIS), в частности общий вариабельный иммунодефицит (ОВИН), который проявляется в среднем в возрасте 24 лет [3, 4]. Как наиболее распространенная форма идентификатора, CVID будет обсуждаться более подробно ниже. Обсуждается также совпадение с аллергическими заболеваниями, а также возможность дальнейшей диагностики сложных случаев в специализированных центрах.
Таблица 1
Классификация IUIS и разделение на группы болезней [2]
| 1. Комбинированный Т- и В-клеточный иммунодефицит |
| 2. Комбинированный иммунодефицит с ассоциированными или синдромальными признаками |
| 3. Преимущественно недостаточность антител |
| 4. Заболевания иммунной дисрегуляции |
| 5. Врожденные дефекты количества и / или функции фагоцитов |
| 6.Нарушения естественного иммунитета (врожденный иммунитет) |
| 7. Аутовоспалительные расстройства |
| 8. Дефицит комплемента |
Клинические проявления иммунодефицитов
Иммунная защита организма начинается с анатомических барьеров, т.е. е., кожа и слизистые оболочки. Даже у иммунокомпетентных людей здесь возникает большинство инфекций. Обеспокоенность возникает, когда инфекции, вызываемые типичными патогенами, такими как пневмококки, стафилококки или сальмонеллы, развиваются сложным и длительным течением или когда эти анатомические барьеры неоднократно нарушаются.Инфекции в необычных местах, а также инфекции, вызванные практически безвредными патогенами, с которыми иммунная система обычно способна справиться, так называемыми условно-патогенными микроорганизмами, такими как микобактерии, Candida или Pneumocystis jirovecii, должны вызывать беспокойство. В таких случаях одно только обнаружение патогена, независимо от клинического течения, должно указывать на ИД. Во всех вышеупомянутых случаях следует начать дальнейшие исследования для установления иммунного статуса пациента.
Тщательный сбор анамнеза пациентов с прошлыми инфекциями имеет решающее значение для любой оценки иммунокомпетентности.
Направленные вопросы используются для записи типа, локализации, частоты и серьезности инфекций. В некоторых случаях этот шаг уже позволяет отличить ID от вторичной восприимчивости к инфекциям из-за локальных нарушений барьера кожи и слизистых оболочек. Таким образом, особенно в случае очаговых инфекций, таких как рецидивирующие инфекции мочевыводящих путей или хронический риносинусит или бронхит, необходимо учитывать местные неиммунологические нарушения защитных механизмов организма или анатомические аномалии.Примеры общей вторичной восприимчивости к инфекциям, не являющимся результатом ID, перечислены в Табл. 2. Особого внимания в этом контексте заслуживает атопический диатез, который из-за аллерген-опосредованных поражений слизистой оболочки иногда связан с повышенной восприимчивостью к инфекциям дыхательных путей и желудочно-кишечным симптомам. Эту причину необходимо исключить до проведения иммунологического обследования.
Таблица 2
Предрасположенность к инфекции без основного иммунодефицита
| Расположение | Причина |
|---|---|
| Кожа | Барьерное нарушение при атопической экземе, ожогах и т. Д. |
| Дыхательные пути | Курение, сухость слизистых оболочек, аллергия Бронхоэктатическая болезнь, муковисцидоз Нарушение вентиляции придаточных пазух носа и среднего уха, дисфагия, свищи |
| Кишечный тракт | Ингибиторы протонной помпы (снижение желудочной кислоты) Нарушение на фоне антибактериальной терапии |
| Мочевыводящие пути | Рефлюкс, стеноз, остаточная моча, половой акт, сухость слизистой между мочевыводящими путями и кишечником |
| Инородные тела | Катетер, протезы |
При наличии удостоверения личности, тип инфекции может определять тип иммунного дефекта.Рецидивирующие бактериальные инфекции дыхательных путей и желудочно-кишечного тракта особенно указывают на гуморальный иммунный дефект (дефицит антител, дефект комплемента). С другой стороны, необычная (условно-патогенная) инфекция указывает, в частности, на клеточный иммунный дефект, как, например, при ВИЧ-инфекциях. Стойкое образование абсцесса, особенно при поражении внутренних органов, системных грибковых инфекциях или остеомиелите, может быть результатом дисфункции нейтрофилов / макрофагов (нарушение фагоцитоза, нейтропения).С другой стороны, кожно-слизистый кандидоз, ограниченный кожей и слизистыми оболочками, свидетельствует об особом дефекте Т-клеток, продуцирующих интерлейкин (ИЛ) -17 (дефицит Th-17) [5].
По этой причине классические предупреждающие знаки ID были сформулированы и обобщены для пациентов с повышенной восприимчивостью к инфекции в немецкой мнемонике ELVIS от имени Немецкой ассоциации научных медицинских обществ (AWMF, Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften е.V., www.awmf.org) [4]. Хотя эти предупреждения не являются исчерпывающими и конкретными, они могут помочь практикующему врачу:
-
Патоген (Эррегер): Инфекции, вызванные условно-патогенными микроорганизмами, такими как Pneumocystis jirovecii (рис.), Должны вызывать подозрение на ИН.
Двусторонняя интерстициальная пневмония с Pneumocystis jirovecii , преимущественно при комбинированном иммунодефиците
© (4) Springer Medizin
-
Локализация (локализация): атипичная локализация инфекции, например.g., абсцесс мозга, вызванный Aspergillus (рис.), церебральный токсоплазмоз или пневмококковый артрит, наводят на мысль о ID.
Инвазивный аспергиллез с абсцессом головного мозга в правой теменно-затылочной доле. 2b: Гистология с прямым обнаружением патогенов, преимущественно при комбинированных иммунных дефектах и WAS
-
Курс (Verlauf): необычное течение с точки зрения хроничности / рецидива и неудовлетворительный ответ на терапию антибиотиками представляют признаки (хотя трудно дифференцировать) ID .
-
Интенсивность (Intensität): То же самое относится к инфекциям, которые имеют необычно тяжелое течение.
-
Количество инфекций (Summe der Infektionen): этот параметр явно зависит от возраста: ≥ 8 незначительных инфекций в год, ≥ 2 случая пневмонии или тяжелого синусита в год считаются ненормальными для маленьких детей, в то время как эмпирическое правило у взрослых ≥ 3 бактериальных инфекций в год, каждая продолжительностью более 4 недель, требует дальнейшего исследования (Табл.) [6–8].
Таблица 3
Нормальное распределение частоты инфицирования у детей (изменено из [7, 8])
Возраст (лет) Респираторные инфекции / год SD Максимум <1 6,1 ± 2,6 11,3 1-2 5,7 ± 3,0 11.7 3–4 4,7 ± 2,9 10,5 5–9 5,5 ± 2,6 8,7 10–14 2,7 ± 2,2 7.2
Семейный анамнез (свидетельство генетического дефекта? Способ наследования?), А в идеале также анамнез, предоставленный третьими сторонами, например. g. родители в отношении детских инфекций и заживления пуповины или терапевт в отношении курса лечения инфекций могут помочь в диагностике ID.В случае дефицита антител (гипогаммаглобулинемия) необходимо целенаправленно искать вторичные причины до постановки диагноза первичной ID. К ним относятся лекарства (например, кортикостероиды, иммунодепрессанты, химиотерапия, некоторые противоэпилептические препараты), инфекционные заболевания [инфекция вируса иммунодефицита человека (ВИЧ), вирус Эпштейна-Барра (ВЭБ), врожденные инфекции краснухи / цитомегаловируса (ЦМВ) / токсоплазмы], опухоли. (в частности, хронический лимфолейкоз, неходжкинская лимфома, тимома) и синдромы, связанные с чрезмерной потерей белка (нефротический синдром, синдром мальабсорбции, лимфангиэктазия).Системная терапия кортикостероидами более 20 мг / день может привести к стойкому снижению уровня IgG в сыворотке [9].
Другие проявления иммунодефицита
Помимо восприимчивости к инфекции, важно знать, что другие признаки нарушения иммунной системы могут быть связаны с ID. К ним относятся хроническое воспаление, аутоиммунитет и лимфопролиферативные расстройства, которые кратко изложены в рекомендациях AWMF немецкой мнемоники GARFIELD [4]:
-
Гранулемы (Granulome): в частности, в легких, лимфатических узлах, коже, а также в других органах
-
Аутоиммунитет (аутоиммунитет): в частности аутоиммунная цитопения, а также аутоиммунитет органов
- лихорадка (Rezidivierendes Fieber): периодическая лихорадка, гемофагоцитоз и др.
-
Экзема (Экземе): часто с ранним началом, атипичная, рефрактерная к терапии
-
Лимфопролиферативные расстройства (лимфопролиферация, лимфопролиферация, лимфопролиферация): хроническая доброкачественная лимфопролиферация.и)
Средостенная лимфаденопатия при общем вариабельном иммунодефиците (ОВИН). Компьютерная томография (КТ) грудной клетки
Выраженная спленомегалия при общем вариабельном иммунодефиците (ОВИН), достигающая почти нижнего полюса почек. Компьютерная томография (КТ) грудной клетки / живота, коронарный разрез
© (2) Springer Medizin
-
Воспалительное заболевание кишечника (Darmentzündung): часто с ранним началом, атипичное, невосприимчивое к терапии (рис.)
Хроническое воспалительное заболевание кишечника, подобное болезни Крона, при общем вариабельном иммунодефиците (ОВИН).Колоскопия
Этот тип иммунной дисрегуляции нередко проявляется до того, как становится очевидной восприимчивость к инфекции, поэтому дифференциальный диагноз ID необходимо учитывать у некоторых пациентов с аутоиммунной цитопенией, глютеновой болезнью, подобной глютеновой. независимая энтеропатия, кишечное заболевание, подобное болезни Крона, или саркоидоподобное гранулематозное воспаление. Хотя иммунный дефект подозревается раньше в случае повышенной восприимчивости к инфекциям, диагностическое обследование ID часто откладывается у пациентов с иммунной дисрегуляцией.Дефицит антител может быть вторичным, как при лимфомах, или быть вызванным основным заболеванием с последующим (вторичным) развитием лимфомы. В этом контексте может быть сложно, как клинически, так и даже гистологически, различить хроническую доброкачественную лимфаденопатию, связанную с ID, и злокачественную лимфому.
Первичный иммунодефицит с повышенным уровнем IgE или аллергическими проявлениями
Специфические, редкие ID, демонстрирующие раннее проявление хронической экземы, высокий общий IgE (синдром гипер-IgE, синдром Вискотта-Олдрича, синдром Оменна) или холодовая крапивница (мутация PLCG2). особый интерес для аллергологов.
Клиническое различие между истинной атопической экземой и синдромом гипер-IgE (HIES), возникающим в результате аутосомно-доминантных мутаций в гене STAT3, иногда может быть сложной задачей. Сами по себе уровни IgE в сыворотке не позволяют провести здесь различие [10]. Более того, в обоих случаях наблюдаются положительный семейный анамнез, обычно обширная экзема и эозинофилия крови. Напротив, пневмония, абсцессы и кандидозные инфекции (особенно в сочетании) типичны для HIES, тогда как при атопической экземе они возникают по большей части как отдельные явления.Эмпиемы, «внутренние» абсцессы (например, печени, лимфатических узлов, периренал) и тяжелые осложнения инфекций, такие как бактериальный менингит или остеомиелит у пациентов с экземой, наблюдаются почти исключительно при HIES. Характерные черты лица (широкий нос, высокое нёбо), гиперслабость суставов и проблемы со сменой зубов являются важными клиническими признаками дефицита STAT3, тогда как истинный атопический диатез крайне редко встречается при дефиците STAT3 [11]. Таким образом, повышенная или необычная восприимчивость к инфекциям у пациентов с экземой должна побуждать к рассмотрению HIES.Диагностическая шкала была разработана для дифференциации STAT3 от других заболеваний с высоким уровнем общего IgE [12].
В качестве второй группы ID, демонстрирующей повышенный общий IgE, здесь заслуживают упоминания комбинированные иммунные дефекты, которые вызывают нарушение регуляции Т-клеток. Особого внимания в этом контексте заслуживает аутосомно-рецессивный дефицит DOCK8, который обычно вызывает повышенную восприимчивость к инфекциям вируса папилломы человека (ВПЧ), вирусов герпеса, контагиозного моллюска, кандиды и бактериальных респираторных инфекций [13].В отличие от дефицита STAT3, клиническая картина здесь часто включает истинную атопию с тяжелой экземой, астмой и преимущественной сенсибилизацией к пищевым аллергенам [10].
Помимо сочетания рецидивирующих инфекций и хронической экземы с ранним началом, Синдром Вискотта-Олдрича (WAS) преимущественно характеризуется тяжелой тромбоцитопенией. Поскольку дефекты белка WAS (WASP) наследуются рецессивным образом, сцепленным с Х-хромосомой, поражаются почти только мальчики. Все эффекторные клетки иммунной системы вовлечены в WAS, что делает его комбинированным иммунным дефектом, как в случае с синдромом Omenn (OS) [14].ОС представляет собой клинически отличный вариант тяжелой комбинированной ID (SCID), включающей гипоморфные мутации в генах RAG. ОВ проявляется уже в первые месяцы жизни из-за оппортунистических инфекций и генерализованной экземы с сопутствующей эозинофилией крови и повышенным общим IgE. Нарушение созревания Т-клеток с олигоклонально ограниченным репертуаром Т-клеток и значительное нарушение развития центральной толерантности в тимусе приводит к обширным аутоиммунным явлениям (алопеции, лимфаденопатии, гепатоспленомегалии и т. Д.). OS также имеет мрачный прогноз, учитывая, что основные проблемы с толерантностью препятствуют восстановлению иммунитета после трансплантации аллогенных стволовых клеток.
Пациенты со стойкой холодовой крапивницей, дефицитом антител (IgA / IgM) с частыми респираторными инфекциями и аутоиммунными явлениями (аутоиммунный тиреоидит, повышенные титры антинуклеарных антител [ANA]) могут страдать от чрезвычайно редкого дефекта фосфолипазы-Cγ2 (PLCCG2), впервые описанный в 2012 году [15], который, как молекула передачи сигнала в В-клетках, естественных клетках-киллерах и тучных клетках, играет важную роль в иммунорегуляции.
Общий вариабельный иммунодефицит
Синдром ОВИН — это синдром дефицита антител, который представляет собой наиболее частую форму симптоматического ID во взрослом возрасте, с точечной распространенностью от 1:25 000 до 1:75 000, в зависимости от исследуемой группы населения [3, 16] . Распространенность примерно одинакова у мужчин и женщин. Хотя изолированный дефицит IgA с показателем распространенности 1: 225–1: 3000 встречается чаще [17], это обычно случайный диагноз и обычно остается бессимптомным на протяжении всей жизни.В отличие от многих других первичных ID, CVID часто диагностируется в зрелом возрасте, преимущественно в возрасте от 20 до 40 лет, и обычно с латентным периодом около 4 лет между первоначальным проявлением и первым диагнозом.
Точная причина ОВИН в большинстве случаев остается неясной, хотя тем временем были описаны отдельные генные дефекты. Эти мутации влияют, например, на например, костимулирующие молекулы линии В-клеток (CD19, CD21, CD81, TACI и BAFF-R) [16]. Процесс созревания В-клеток до продуцирующих антитела плазматических клеток нарушен у большинства пациентов [18, 18].Табл. 4 резюмирует новые критерии, выпущенные Европейским обществом иммунодефицитов (ESID) для диагностики CVID [20].
Таблица 4
Диагностические критерии ESID для CVID [19]
| ОВИН диагностируется при соблюдении хотя бы одного из следующих критериев: | |
| _ Повышенная восприимчивость к инфекциям _ Аутоиммунные проявления _ Гранулематозная болезнь _ Необъяснимая поликлональная лимфопролиферация _ Другие члены семьи с дефицитом антител |
|
| и | Дефицит IgG и IgA как минимум на два стандартных отклонения ниже среднего соответствующего уровня (не нижней нормы!), Со сниженным IgM или без него, обнаруженный как минимум в двух измерениях |
| и | По крайней мере, один из следующих критериев: |
| _ Неспособность обнаружить значительный рост специфических IgG после вакцинации (и / или отсутствия изогемагглютининов), i.е., неспособность достичь защитного уровня IgG, где это определено _ Низкое количество B-клеток памяти с переключением классов (<70%, скорректированное по возрасту стандартное значение) |
|
| и | Исключение вторичных причин гипогаммаглобулинемии (см. Текст) |
| и | Диагностика заболевания после 4 лет (возможны предыдущие симптомы) |
| и |
№ № указание на выраженную недостаточность Т-клеток, определяемую двумя из следующих критериев: _ количество хелперных клеток CD4: 2–6 лет, <300 / мкл; 6–12 лет <250 / мкл; > 12 лет, <200 / мкл _% Наивные клетки-помощники CD4: 2–6 лет, <25%; 6–16 лет, <20%; > 16 лет <10% _ Отсутствие пролиферации Т-клеток in vitr |
Диагностический подход при подозрении на иммунодефицит
Поэтапный подход к диагностике иммунных дефектов:
-
Скрининг
В рамках этого процесса должен быть низкий порог для рентабельных методов скрининга, т.е.е., даже в случае низкой клинической подозрительности. Более подробный анализ иммунной системы (включая определение подкласса IgG), который часто технически сложен и дорог, следует проводить в специализированных клиниках или центрах.
На первом этапе клиническая картина определяет выбор скрининга: дифференциальный анализ крови (нейтропения? Моноцитопения?) При подозрении на врожденный иммунный дефект; в случае подозрения на клеточный дефект в дополнение к общему анализу крови требуется абсолютное количество хелперных клеток CD4, соотношение CD4: CD8 и скрининговый тест на ВИЧ.Любое указание в анамнезе пациента на гуморальный иммунный дефект следует исследовать путем количественного измерения сывороточных антител IgG, IgA и IgM. Эти исследования являются экономически эффективными (определение иммуноглобулинов, исключая подклассы: 4 евро в Германии, 18 sFr в Швейцарии) и могут значительно сократить часто длительные страдания пациентов до постановки диагноза и эффективного лечения. Повторение этих тестов в течение 1–6 месяцев необходимо, чтобы избежать классификации постинфекционной или преходящей гипогаммаглобулинемии (например,г., в младенчестве) как ID. При анализе результатов важно учитывать возрастную зависимость нормальных показателей, включая иммуноглобулины.
Совместное принятие решений лечащим врачом и специализированным центром о дальнейших диагностических шагах в каждом конкретном случае помогает избежать ненужных исследований и затрат, с одной стороны, обеспечивая при этом выполнение иногда технически сложных функциональных иммунологических тестов. на качественно высоком уровне. Многие из более специализированных лабораторных исследований могут проводиться на образцах крови, отправленных экспресс-почтой.
При подозрении на моногенетический дефект и соответствующей терапевтической значимости рекомендуется подтверждение с помощью генетического анализа. С другой стороны, в случае ОВИН с отрицательным семейным анамнезом генетическая диагностика в настоящее время не рекомендуется, поскольку на лечение (пока) не влияют результаты.
Лечение
В дополнение к общим мерам, включая оптимальную гигиену (рук) и уход за зубами, предотвращение передачи за счет улучшения барьерной защиты (увлажняющие / смягчающие средства кожи, местное лечение инфекций верхних дыхательных путей, включая сосудосуживающие капли для носа, полоскания солевым раствором, возможное предотвращение больших толпы людей), а также быстрое и целенаправленное применение антибиотиков в случае бактериальных инфекций, пациенты с иммунодефицитом (особенно в случае дефектов комплемента и асплении) должны последовательно проходить все рекомендованные вакцинации.Здесь следует отметить, что живые прививки при ИН противопоказаны. Заместительная терапия иммуноглобулином обеспечивает хорошую пассивную защиту от классических патогенов, указанных в национальных планах вакцинации (столбняк, дифтерия и т. Д.), Против которых не требуется дополнительная вакцинация. С другой стороны, ежегодные вакцины против гриппа в случаях, когда есть остаточная способность к иммунному ответу, безусловно, имеют смысл, поскольку можно предположить, что в препаратах иммуноглобулинов отсутствуют защитные антитела.Местные и национальные рекомендации по вакцинам, в том числе для групп риска, таких как ID, можно получить на следующих сайтах для конкретных стран:
Специфические меры лечения определяются видом иммунного дефекта; поэтому мы можем предоставить только обзор общих принципов лечения.
В случае гуморального ID замещение IgG является наиболее важной формой лечения. Его можно вводить внутривенно в начальной дозе 0,4 г / кг массы тела (МТ) (ок.20-25 г / 3-4 недели) в кабинете врача или подкожно с недельными интервалами самими пациентами (начальная доза 0,1 г / кг МТ в неделю). Перед первоначальным введением пациента необходимо проинформировать о том, что он получает продукт крови и о связанных с ним побочных эффектах. Доступные препараты иммуноглобулинов соответствуют фармацевтическим требованиям, и с 1994 г. в Европе и США не было зарегистрировано случаев передачи патогенов через препараты иммуноглобулинов [21].
В случае подкожного замещения пациенты проходят инструктаж по самостоятельному введению с помощью микронасоса и набора стерильных игл перед тем, как самостоятельно вводить препарат в домашних условиях. Домашняя терапия дополняется контрольными осмотрами каждые 3–6 месяцев лечащим врачом. Доза корректируется в соответствии с индивидуальными потребностями пациента в течение курса терапии с целью достижения статуса безинфекционного состояния. Важным клиническим исключением здесь является хронический риносинусит, который может сохраняться, несмотря на лечение.Целевой уровень сывороточного IgG 7 г / л, обычно используемый лабораторный суррогатный маркер для адекватного замещения, не может применяться универсально для всех пациентов. Увеличение дозы с получением минимальных уровней IgG в сыворотке крови в диапазоне 10–12 г / л необходимо в некоторых случаях для достижения статуса отсутствия инфекции.
При других формах ID или в случае гуморального ID, резистентного к терапии, требуется длительная антибиотикопрофилактика в качестве единственного лечения или в сочетании с заменой иммуноглобулинов.
-
Котримоксазол 960 мг (3 раза в неделю) при комбинированном ID (количество CD4-клеток <200 / мкл)
-
Пенициллин (2 x 1 млн IE / день) у пациентов с спленэктомией
-
Ципрофлоксацин в тяжелой форме нейтропения (дополнительно, гранулоцитарный колониестимулирующий фактор [G-CSF])
-
Ингаляции тобрамицина или колистина при муковисцидозе и осложненных бронхоэктазах
-
Итраконазол (2 х 100 мг) и котримуломатозол
в сутки, септик гранулометрический гранулометрический 960 мг / сут 960 мг / сут.
Инфекции могут возникать даже при замене иммуноглобулинов.Симптомы острой инфекции требуют быстрого выявления с низким порогом начала антибактериальной терапии. Важно, чтобы все лечащие коллеги знали, что серологический диагноз инфекций у пациентов с ОВИН недействителен из-за нарушения образования антител. В этих условиях прямое обнаружение патогенов с использованием гистологии, посева или полимеразной цепной реакции (ПЦР) является единственными надежными диагностическими вариантами. Перед хирургическим и стоматологическим вмешательством следует рассмотреть вопрос о профилактике антибиотиками.
В случае некоторых иммунных дефектов, в частности клеточного ID, только «замена» иммунной системы посредством трансплантации стволовых клеток является эффективным и причинным лечением. Генная терапия является вариантом в конкретных случаях четко определенных иммунных дефектов, особенно при отсутствии подходящего донора. Хотя трансплантация стволовых клеток является стандартной процедурой для детей с ТКИД, она считается экспериментальным подходом к лечению взрослых с врожденными иммунными дефектами и ограничивается отдельными случаями, которые оказываются сложными и не поддаются лечению.Важно, чтобы специализированные центры участвовали как в показаниях, так и в назначении этого лечения.
Систематическая регистрация пациентов с первичными иммунными дефектами лечащим врачом в регистрах, таких как Европейский регистр ESID (www.esid.org), помогает создать научную основу для улучшения нашего понимания этих сложных и редких заболеваний, в частности их клинических проявлений. течение и клиническое значение предупреждающих знаков, описанных выше.
Помимо медицинского обслуживания, некоторые пациенты получают выгоду от сетевых возможностей, предлагаемых организациями пациентов и заинтересованных сторон, которые способствуют общению, организуют публичные лекции и предлагают множество практических советов о том, как справиться с ID в повседневной жизни.Их можно найти в разделе:
Немецкие центры экспертизы в области ID создали сеть FIND-ID (www.find-id.net) для обеспечения непрерывного обмена информацией между существующими центрами, клиниками и врачами, тем самым способствуя раннему выявлению и лечение пациентов с врожденным ID — цель, полностью поддерживаемая настоящей статьей.
Сокращения
| ANA | Антиядерные антитела | |
| AWMF | Немецкая ассоциация научных медицинских обществ (Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V) | |
| CMV | Цитомегаловирус | |
| CVID | Общий вариабельный иммунодефицит, синдром вариабельного иммунодефицита | |
| EBV | Вирусы Эпштейна-Барра | |
| ESID | Европейское общество G-CSF | Гранулоцитарный колониестимулирующий фактор |
| HIES | Синдром гипер-IgE | |
| ВИЧ | Вирус иммунодефицита человека | |
| ВПЧ | Вирус папилломы человека | 70 Идентификатор иммунитета | 70 |
| Ig | Иммуноглобулин | |
| IL | Интерлейкин | |
| IUIS | Международный союз иммунологических обществ | |
| OS | Синдром Оменна | |
| ПЦР-цепочка реферазы | ction | |
| SCID | Тяжелый комбинированный иммунодефицит | |
| SD | Стандартное отклонение | |
| Th | Т-хелперные клетки | |
| WAS | Синдром Вискотта-Олдрича | |
| Синдром Wiskott-Aldrich | ||
| белок |
Сноски
Конфликт интересов
Автор корреспонденции заявляет, что конфликта интересов нет.Профессор доктор Варнац получал гонорары от компаний Baxter, CSL Behring, Octapharma и Biotest.
Укажите это как
Хаусманн О., Варнац К. Иммунодефицит у взрослых: практическое руководство для аллерголога. Allergo J Int 2014; 23: 261–8 DOI: 10.1007 / s40629-014-0030-4
Ссылки
1. Peter HH, Pichler WJ, Müller-Ladner U, eds. Klinische Immunologie. 3. Aufl. Мюнхен — Эльзевир; 2012
2. Аль-Херц В., Бусфиха А., Казанова Дж. Л., Шатила Т., Конли М.Э., Каннингем-Рандлс С. и др.Болезни первичного иммунодефицита: обновленная информация о классификации комитета экспертов международного союза иммунологических обществ по первичному иммунодефициту. Фронт Иммунол. 2014; 5: 162. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Гатманн Б., Махлауи Н., Жерар Л., Оксенхендлер Э., Варнац К., Шульце И. и др. Клиника и лечение 2212 больных общим вариабельным иммунодефицитом. J Allergy Clin Immunol. 2014; S0091-6749 (14): 00029–3. [PubMed] [Google Scholar] 4. Farmand S, Baumann U, Bernuth H, Borte M, Foerster-Waldl E, Franke K и др.Ассоциация научных медицинских обществ Германии (AWMF). [Междисциплинарное руководство AWMF по диагностике первичного иммунодефицита] Клин Падиатр. 2011; 223: 378–85. DOI: 10,1055 / с-0031-1287835. [PubMed] [CrossRef] [Google Scholar] 5. Силлевис Смитт JH, Kuijpers TW. Кожные проявления первичного иммунодефицита. Curr Opin Pediatr. 2013; 25: 492–7. DOI: 10.1097 / MOP.0b013e3283623b9f. [PubMed] [CrossRef] [Google Scholar] 6. Monto AS, Napier JA, Metzner HL. Исследование респираторных заболеваний Текумсе.I. План исследования и наблюдения за синдромами ОРЗ. Am J Epidemiol. 1971; 94: 269–79. [PubMed] [Google Scholar] 7. Fleming DW, Cochi SL, Hightower AW, Broome CV. Инфекции верхних дыхательных путей в детском возрасте: в какой степени посещаемость детских садов влияет на заболеваемость? Педиатрия. 1987. 79: 55–60. [PubMed] [Google Scholar] 8. Monto AS, Салливан KM. Epidemiol Infect. 1993. Острое респираторное заболевание в обществе. Частота заболевания и вовлеченные агенты; С. 110145–60. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9.Кавано Т., Мацусе Х, Обасе Й, Кондо Й, Мачида I, Томари С. и др. Гипогаммаглобулинемия у стероид-зависимых астматиков коррелирует с суточной дозой перорального преднизолона. Int Arch Allergy Immunol. 2002; 128: 240–3. DOI: 10,1159 / 000064258. [PubMed] [CrossRef] [Google Scholar] 10. Боос А.С., Хагл Б., Шлезингер А., Хальм Б.Е., Балленбергер Н., Пинарчи М. и др. Атопический дерматит, синдромы STAT3- и DOCK8-гипер-IgE различаются по типу сенсибилизации на основе IgE. Аллергия. 2014; 69: 943–53. DOI: 10.1111 / все.12416. [PubMed] [CrossRef] [Google Scholar] 11. Schimke LF, Sawalle-Belohradsky J, Roesler J, Wollenberg A, Rack A, Borte M и др. Диагностический подход к синдромам гипер-IgE: ключевые иммунологические и клинические данные для дифференциации синдромов гипер-IgE от атопического дерматита. J Allergy Clin Immunol. 2010; 126: 611–7. DOI: 10.1016 / j.jaci.2010.06.029. [PubMed] [CrossRef] [Google Scholar] 12. Woellner C, Gertz EM, Schaffer AA, Lagos M, Perro M, Glocker EO и др. Мутации в STAT3 и рекомендации по диагностике синдрома гипер-IgE.J Allergy Clin Immunol. 2010; 125: 424–32. DOI: 10.1016 / j.jaci.2009.10.059. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 14. Альберт MH, Notarangelo LD, Ochs HD. Клинический спектр, патофизиология и лечение синдрома Вискотта-Олдрича. Curr Opin Hematol. 2011; 18: 42–8. DOI: 10.1097 / MOH.0b013e32834114bc. [PubMed] [CrossRef] [Google Scholar] 15. Омбрелло М.Дж., Реммерс Э.Ф., Сан Дж., Фриман А.Ф., Датта С., Тораби-Паризи П. и др. Холодовая крапивница, иммунодефицит и аутоиммунитет, связанные с делециями PLCG2.N Engl J Med. 2012; 366: 330–8. DOI: 10.1056 / NEJMoa1102140. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 18. Вер Ц., Кивиоя Т., Шмитт Ц., Ферри Б, Витте Т., Эрен Э. и др. Исследование EUROclass: определение подгрупп общего вариабельного иммунодефицита. Кровь. 2008; 111: 77–85. DOI: 10.1182 / кровь-2007-06-0
. [PubMed] [CrossRef] [Google Scholar] 19. ван де Вен AA, Compeer EB, van Montfrans JM, Boes M. Дефекты B-клеток при общем вариабельном иммунодефиците: передача сигналов BCR, кластеризация белков и зашитые генные мутации.Crit Rev Immunol. 2011; 31: 85–98. DOI: 10.1615 / CritRevImmunol.v31.i2.10. [PubMed] [CrossRef] [Google Scholar] 21. Krudewig J, Baumann U, von Bernuth H, Borte M, Burkhard-Meier U, Dueckers G, et al. [Междисциплинарное руководство AWMF по лечению первичной недостаточности антител] Klin Padiatr. 2012; 224: 404–15. DOI: 10,1055 / с-0032-1323837. [PubMed] [CrossRef] [Google Scholar]
Общий вариабельный иммунодефицит (CVID): симптомы и лечение
Обзор
Что такое общий вариабельный иммунодефицит (ОВИН)?
ОВИН — это генетическое заболевание, поражающее иммунную систему.У людей с этим заболеванием низкий уровень антител (белков, борющихся с инфекциями) в крови. Когда в организме недостаточно этих антител, люди могут часто заражаться.
У людей с ОВИН инфекции часто развиваются в дыхательной системе, ушах и носовых пазухах. CVID может увеличить риск развития проблем с пищеварением и рака.
CVID — это заболевание первичного иммунодефицита (PIDD). Эти заболевания представляют собой генетические нарушения, при которых иммунная система человека не работает должным образом.
Кто страдает общим вариабельным иммунодефицитом (ОВИН)?
ОВИН встречается примерно у 1 из 25 000 человек. Он поражает мужчин и женщин в равных количествах. Заболевание может появиться у детей или подростков, но обычно не распознается до взрослого возраста. В большинстве случаев врач диагностирует заболевание, когда человеку от 20 до 50 лет.
Симптомы и причины
Что вызывает общий вариабельный иммунодефицит (ОВИН)?
Генетическая мутация (изменение) вызывает ОВИН.В большинстве случаев эта генетическая мутация — и симптомы ОВИН — развиваются без какой-либо очевидной причины. Примерно в 10% случаев ОВИН передается по наследству (передается от членов семьи).
ОВИН возникает в результате дефектов генов, связанных с иммунной системой. Эти дефекты заставляют организм вырабатывать аномально низкие количества белков, называемых иммуноглобулинами, включая иммуноглобулин G (IgG). Низкий уровень IgG в крови может затруднить борьбу с инфекциями.
Каковы симптомы общего вариабельного иммунодефицита (ОВИН)?
Симптомы ОВИН сильно различаются от человека к человеку.Они могут варьироваться от легких до тяжелых. Признаки и симптомы CVID включают:
- Проблемы с дыханием
- Хронический кашель
- Диарея, вызывающая похудание
- Инфекции уха
- Частые инфекции носовых пазух
- Рецидивирующие инфекции легких, включая пневмонию
Диагностика и тесты
Как диагностируется общий вариабельный иммунодефицит (ОВИН)?
Врач может рассмотреть ОВИН как возможную причину, если у вас есть признаки иммунного расстройства или необычная реакция на вакцины.
Ваш врач спросит о вашей семейной истории болезни и назначит анализы крови. Образец крови может выявить признаки ОВИН, включая низкий уровень IgG.
Анализы крови также могут помочь вашему врачу оценить, насколько хорошо функционирует ваша иммунная система. Ваш врач может сделать вам вакцину от другого заболевания, чтобы увидеть, как ваш организм реагирует на вакцину.
Ведение и лечение
Каковы методы лечения общего вариабельного иммунодефицита (ОВИН)?
Если установлен диагноз ОВИН, врач назначит заместительную терапию иммуноглобулином (IgG), чтобы попытаться предотвратить инфекции.Люди, которые нуждаются в терапии IgG, получают ее на протяжении всей жизни — это не разовое лечение.
IgG-терапия заменяет недостающий иммуноглобулин антителами из крови здоровых доноров. Вы получите это лечение внутривенно (через иглу, введенную в вену) или путем инъекции под кожу (подкожно).
Ваш врач может также назначить лекарства, называемые антибиотиками, для лечения инфекций, связанных с ОВИН, и другие лекарства для лечения осложнений ОВИН.
Какие осложнения связаны с общим вариабельным иммунодефицитом (ОВИН)?
Люди с ОВИН имеют повышенный риск развития осложнений, в том числе:
- Аутоиммунные расстройства: Состояния, при которых иммунная система организма наносит вред собственным клеткам. У некоторых людей с ОВИН развивается иммунная тромбоцитопения (низкий уровень тромбоцитов в крови) или аутоиммунная гемолитическая анемия (когда иммунная система организма разрушает эритроциты).
- Бронхоэктазия : Постоянное повреждение легких в результате рецидивирующих инфекций.
- Рак: Заболевания, включая лимфому и рак желудка.
- Гранулемы: Воспаленные клетки кожи, легких и других органов.
Профилактика
Как можно предотвратить общий вариабельный иммунодефицит (ОВИН)?
Вы не можете предотвратить CVID. Это заболевание передается в семье (генетическое заболевание) и присутствует на протяжении всей жизни человека.
Кто подвержен риску развития общего вариабельного иммунодефицита (ОВИН)?
В небольшом количестве случаев люди, у которых есть член семьи с ОВИН, подвергаются более высокому риску развития заболевания.В большинстве случаев врачи не знают, что вызывает мутацию гена, вызывающую ОВИН.
Перспективы / Прогноз
Каков прогноз (перспективы) для людей с общим вариабельным иммунодефицитом (ОВИН)?
CVID неизлечим. При продолжающемся лечении многие люди с этим расстройством живут активной и полноценной жизнью.
В некоторых случаях осложнения ОВИН, такие как поражение легких или рак, могут повлиять на продолжительность жизни. Эти осложнения появляются со временем. Они могут стать опасными для жизни, но этот процесс часто занимает годы.
Жить с
Когда мне следует обратиться к врачу по поводу общего вариабельного иммунодефицита (CVID)?
Обратитесь к своему врачу, если у вас частые или повторяющиеся инфекции или другие симптомы ОВИН.
Какие вопросы я должен задать своему врачу?
Если у вас общий вариабельный иммунодефицит, вы можете спросить своего врача:
- Насколько серьезна CVID?
- Что вызвало это состояние?
- Как это повлияет на мой дом и работу?
- На какие признаки осложнений следует обращать внимание?
Симптомы иммунодефицитных заболеваний
Наиболее очевидным признаком иммунодефицитных заболеваний являются частые, необычные и повторяющиеся инфекции, которые кажутся чрезмерными.
Число инфекций у здоровых людей варьируется в зависимости от нескольких факторов, таких как уровень стресса, воздействие на детей и вирулентность распространенных вирусов. Это затрудняет оценку наличия у человека чрезмерного количества инфекций.
Приведенный ниже список был взят из 10 предупреждающих признаков первичного иммунодефицита (ВЗОМТ), подготовленных Фондом Джеффри Моделла. Лица, которые испытали два или более из следующих симптомов, могут иметь первичный иммунодефицит:
Взрослые
-
Две или более новых инфекции уха в течение 1 года
-
Две или более новых инфекции носовых пазух в течение 1 года при отсутствии аллергии
-
Одна пневмония в год (подтверждена рентгенологически) более 1 года
-
Хроническая диарея с похуданием
-
Рецидивирующие вирусные инфекции (простуда, герпес, бородавки, кондиломы)
-
Периодическая потребность в внутривенных антибиотиках для лечения инфекций
-
Рецидивирующие глубокие абсцессы кожи, лимфатических узлов или внутренних органов
-
Стойкая молочница или грибковые инфекции на коже или в других местах
-
Инфекции, вызываемые обычно безвредными туберкулезоподобными бактериями
-
Семейный анамнез первичного иммунодефицита
Дети
-
Четыре или более ушных инфекций в течение 1 года
-
Две или более тяжелых инфекций носовых пазух в течение одного года
-
Два или более месяца лечения антибиотиками без небольшого эффекта
-
Две и более пневмонии в год
-
Недостаточная прибавка в весе или задержка роста
-
Рецидивирующие глубокие абсцессы кожи или органа
-
Стойкий молочница во рту или грибковая инфекция на коже
-
Необходимость внутривенных антибиотиков для лечения инфекций
-
Две или более глубоких инфекции
-
Семейный анамнез первичного иммунодефицита
Общие симптомы вариабельного иммунодефицита, диагностика и лечение
Общий вариабельный иммунодефицит (ОВИН) — это дефицит антител, из-за которого иммунная система не может защищаться от бактерий и вирусов, что приводит к повторяющимся и часто тяжелым инфекциям, в первую очередь поражающим уши, носовые пазухи и дыхательные пути (синусно-легочные инфекции).В большинстве случаев диагноз ставится только на третьем-четвертом десятилетии жизни. Необратимое повреждение дыхательных путей (бронхоэктатическая болезнь) может произойти из-за тяжелых и повторяющихся инфекций.
Хотя генетические мутации, приводящие к ОВИН, были идентифицированы, точная причина и характер генетического наследования ОВИН в большинстве случаев неизвестны. Поражаются как самцы, так и самки. Это одна из наиболее распространенных форм болезни первичного иммунодефицита (PIDD), и тяжесть симптомов варьируется от одного человека к другому.
ОВИН может быть связано с аутоиммунными заболеваниями, которые поражают другие клетки крови, вызывая низкое количество лейкоцитов или тромбоцитов, анемию, артрит и другие состояния, такие как эндокринные нарушения. Также могут присутствовать желудочно-кишечные проблемы, включая хроническую диарею, потерю веса, тошноту, рвоту и боль в животе. При некоторых формах ОВИН у пациентов развиваются гранулемы в легких, лимфатических узлах, печени, коже или других органах.
Люди с ОВИН также подвержены повышенному риску некоторых видов рака (в первую очередь лимфоидного и желудочно-кишечного рака).
Лечение ОВИН включает замену иммуноглобулинов, профилактические антибиотики и, если показано, лечение аутоиммунных и гранулематозных заболеваний.
Будьте в курсе последней информации и общайтесь с другими. Присоединиться к нам на Facebook.
Симптомы
ОВИН можно диагностировать в любое время, начиная с детства и заканчивая взрослой жизнью.
Как и в случае с дефицитом других антител, наиболее распространенными типами рецидивирующих инфекций являются уши, носовые пазухи, бронхи и легкие.К ним относятся:
- Пневмония
- Гайморит
- Инфекции уха
- Инфекции желудочно-кишечного тракта
Рецидивирующая пневмония и хронические инфекции легких могут привести к повреждению легких, называемому бронхоэктазами, что может осложнить лечение.
Диагностика
ОВИН можно заподозрить у детей или взрослых с историей рецидивирующих инфекций легких, бронхов, ушей или носовых пазух.
Точный диагноз можно поставить с помощью скрининговых тестов, измеряющих уровень иммуноглобулинов или количество В-клеток в крови.
ОВИН лечат заместительной иммуноглобулиновой терапией (ЗРТ), которая чаще всего облегчает симптомы. Лечение IRT должно проводиться регулярно и длиться всю жизнь.
Антибиотики используются для лечения большинства инфекций, вызванных ОВИН, хотя пациентам может потребоваться более длительное лечение, чем здоровому человеку.
Чтобы узнать больше о PIDD, посетите веб-сайт Фонда иммунодефицита.
Общественный центр CVID | Фонд иммунодефицита
Добро пожаловать в Общественный центр IDF CVID
Общественный центр по общему вариабельному иммунодефициту (CVID) IDF — это ваш онлайн-источник достоверной информации об CVID, клинических справок, публикаций и поддержки. Фонд иммунодефицита (IDF) создал этот центр для предоставления информации, обучения и поддержки по оценке, диагностике, лечению и вопросам здоровья и благополучия людей, живущих с ОВИН, и их семей.
IDF понимает проблемы и эмоции, с которыми вы сталкиваетесь. Если вам недавно поставили диагноз, вы ухаживаете за любимым человеком или длительное время лечите CVID, мы здесь, чтобы помочь вам разобраться в вашем опыте. От поиска врачей до оказания эмоциональной поддержки — мы предлагаем программы, услуги и ресурсы, которые помогут вам лучше справиться с диагнозом ОВИН.
Просмотр рекомендуемых ресурсов IDF по CVID
Обзор общей переменной иммунодефицита
Общий вариабельный иммунодефицит (ОВИН) — один из наиболее часто диагностируемых первичных иммунодефицитов, особенно у взрослых, характеризующийся низким уровнем сывороточных иммуноглобулинов и антител, что вызывает повышенную восприимчивость к инфекции.Считается, что причиной CVID являются генетические дефекты, но в большинстве случаев точная причина заболевания неизвестна.
По сравнению с другими дефектами иммунной системы человека, ОВИН является относительно частой формой первичного иммунодефицита, обнаруживаемой примерно у 1 из 25 000 человек; по этой причине он называется «обычным». Степень и тип дефицита сывороточных иммуноглобулинов, а также клиническое течение варьируются от пациента к пациенту, отсюда и слово «переменный». У некоторых пациентов наблюдается снижение как IgG, так и IgA; в других случаях снижены все три основных типа иммуноглобулинов (IgG, IgA и IgM).У других есть дефекты Т-клеток, и это также может способствовать повышенной восприимчивости к инфекциям, а также к аутоиммунитету, гранулемам и опухолям. Чтобы быть уверенным, что ОВИН является правильным диагнозом, должны быть доказательства нехватки функциональных антител и должны быть исключены другие возможные причины этих иммунологических нарушений. Частые и / или необычные инфекции могут впервые возникнуть в раннем детстве, подростковом или взрослом возрасте. Пациенты с ОВИН также имеют повышенную частоту аутоиммунных или воспалительных проявлений, гранулем и повышенную предрасположенность к раку по сравнению с населением в целом.Иногда именно наличие одного из этих состояний побуждает к оценке CVID. Медицинские термины для отсутствия или низкого уровня иммуноглобулинов крови — агаммаглобулинемия и гипогаммаглобулинемия соответственно. Из-за позднего появления симптомов и диагноза другие названия, которые использовались в прошлом, включают «приобретенную» агаммаглобулинемию, агаммаглобулинемию «взрослого начала» или гипогаммаглобулинемию «позднего начала». Термин «приобретенный иммунодефицит» относится к синдрому, вызванному вирусом СПИДа (ВИЧ), и не должен использоваться для людей с ОВИН, поскольку эти расстройства очень разные.
Присоединяйтесь к официальной группе IDF в Facebook для людей с диагнозом CVID и их ближайших родственников. Это место, где люди, затронутые CVID, могут общаться, задавать вопросы и делиться своими мыслями и опытом.
Присоединяйтесь к группе IDF CVID в Facebook
Клинические признаки общего вариабельного иммунодефицита
И мужчины, и женщины могут иметь ОВИН. В большинстве случаев диагноз ставится только на третьем или четвертом десятилетии жизни.Однако примерно у 20% пациентов наблюдаются симптомы заболевания или обнаруживается иммунодефицит в детстве. Поскольку иммунная система созревает медленно, диагноз ОВИН обычно ставится только в возрасте 4 лет. Обычными признаками ОВИН являются рецидивирующие инфекции ушей, носовых пазух, бронхов (дыхательные трубки) и легких (дыхательные пути). ). Когда легочные инфекции являются серьезными и повторяются неоднократно, может развиться необратимое повреждение с расширением и рубцеванием бронхиального дерева, состояние, называемое бронхоэктазией.Микроорганизмы, обычно обнаруживаемые при этих синопульмональных инфекциях, представляют собой широко распространенные среди населения бактерии, которые часто вызывают пневмонию (Hemophilus influenzae, пневмококки и стафилококки) даже у людей, не страдающих ОВИН. Целью лечения легочных инфекций является предотвращение их рецидива и сопутствующего хронического и прогрессирующего повреждения легочной ткани. Регулярный кашель по утрам и выделение желтой или зеленой мокроты могут указывать на наличие хронического бронхита или бронхоэктазов.У пациентов с ОВИН также могут развиваться увеличенные лимфатические узлы на шее, груди или животе. Конкретная причина неизвестна, но увеличение лимфатических узлов может быть вызвано инфекцией, аномальным иммунным ответом или и тем, и другим. Точно так же относительно часто встречается увеличение селезенки, как и увеличение пейеровских бляшек, которые представляют собой скопления лимфоцитов в стенках кишечника. В некоторых случаях другие скопления воспалительных клеток, называемые гранулемами, можно найти в легких, лимфатических узлах, печени, коже или других органах.Они в основном состоят из клеток, называемых моноцитами и макрофагами. Они могут быть реакцией на инфекцию, но причина неизвестна. Хотя пациенты с ОВИН имеют подавленный ответ антител и низкий уровень иммуноглобулинов в крови, некоторые из антител, вырабатываемых этими пациентами, могут атаковать их собственные ткани (аутоантитела). Эти аутоантитела могут атаковать и разрушать клетки крови, такие как эритроциты, лейкоциты или тромбоциты. Хотя у большинства людей с ОВИН сначала возникают рецидивирующие бактериальные инфекции, примерно в 20% случаев первым проявлением иммунного дефекта является обнаружение очень низкого уровня тромбоцитов в крови или тяжелой анемии из-за разрушения эритроцитов.Аутоантитела могут также вызывать другие заболевания, такие как артрит или эндокринные нарушения, такие как заболевание щитовидной железы. Жалобы со стороны желудочно-кишечного тракта, такие как боль в животе, вздутие живота, тошнота, рвота, диарея и потеря веса, не редкость при ОВИН. Тщательное обследование органов пищеварения может выявить нарушение всасывания жиров и некоторых сахаров или воспалительное заболевание кишечника. Если взят небольшой образец (биопсия) слизистой оболочки кишечника, можно увидеть характерные изменения. Эти изменения помогают диагностировать проблему и лечить ее.У некоторых пациентов с проблемами пищеварения в биоптатах и образцах стула был обнаружен небольшой паразит под названием Giardia lamblia. Устранение этих паразитов с помощью лекарств может устранить желудочно-кишечные симптомы. У некоторых пациентов с ОВИН, которые могут не получать оптимальную заместительную иммуноглобулиновую терапию, также может развиться болезненное воспаление одного или нескольких суставов. Это состояние называется полиартритом. В большинстве этих случаев суставная жидкость не содержит бактерий.Чтобы быть уверенным, что артрит не вызван излечимой инфекцией; суставная жидкость может быть удалена с помощью пункционной аспирации и исследована на наличие бактерий. В некоторых случаях причиной может быть бактерия Mycoplasma, которую трудно диагностировать. Типичный артрит, связанный с ОВИН, может поражать более крупные суставы, такие как колени, лодыжки, локти и запястья. Более мелкие суставы, такие как суставы пальцев, поражаются редко. Симптомы воспаления суставов обычно исчезают при адекватной терапии иммуноглобулинами и соответствующими антибиотиками.Однако у некоторых пациентов артрит может развиться даже тогда, когда пациент получает адекватную заместительную терапию иммуноглобулином. Наконец, пациенты с ОВИН могут иметь повышенный риск рака, особенно рака лимфоидной системы или желудочно-кишечного тракта.
Диагностика общего вариабельного иммунодефицита
ОВИН следует подозревать у детей или взрослых, у которых в анамнезе есть рецидивирующие бактериальные инфекции ушей, носовых пазух, бронхов и легких. Характерные лабораторные особенности включают низкие уровни сывороточных иммуноглобулинов, включая IgG, часто IgA и иногда IgM.Другая часть диагностики ОВИН — это определение отсутствия функциональных антител. Это делается путем измерения сывороточных уровней антител против вакцинных антигенов, таких как столбняк или дифтерия, корь, эпидемический паротит или краснуха, гемофильный или пневмококковый полисахарид. У пациентов с ОВИН очень низкие уровни антител к большинству этих вакцин или их отсутствие. Иммунизация убитыми вакцинами используется для измерения функции антител, и это функциональное тестирование имеет решающее значение до начала лечения.Эти тесты также помогают врачу решить, получит ли пациент пользу от заместительной терапии иммуноглобулином, и могут иметь ключевое значение для получения разрешения на страховку для этой терапии. Количество B- и T-лимфоцитов также может быть определено, а их функция проверена на тканевых культурах.
Генетика и наследование общего вариабельного иммунодефицита
Пациенты с ОВИН обычно имеют нормальное количество клеток, вырабатывающих антитела (В-лимфоцитов), но эти клетки не могут пройти нормальное созревание в плазматические клетки, клетки, способные вырабатывать различные типы иммуноглобулинов и антител для кровотока и секретов. .Генетические причины CVID в значительной степени неизвестны, хотя недавние исследования показали участие небольшой группы генов у нескольких пациентов. К ним относятся индуцибельные костимуляторы (ICOS) и некоторые другие белки В-клеток. По всей видимости, это причины аутосомно-рецессивного CVID. Мутации в клеточном рецепторе (TACI), необходимые для нормального роста и регуляции В-клеток, также были обнаружены примерно у 8% пациентов с ОВИН. Однако причинная роль мутаций TACI в этом иммунном дефекте еще не ясна, поскольку некоторые из этих мутаций могут быть обнаружены у людей с нормальными иммуноглобулинами.Поскольку по большей части это очень редкие генные дефекты, генетическое тестирование еще не требуется и не показано для диагностики ОВИН.
Лечение общего вариабельного иммунодефицита
Лечение ОВИН аналогично лечению других заболеваний с низким уровнем сывороточных иммуноглобулинов. При отсутствии значительного дефекта Т-лимфоцитов или повреждения органа заместительная иммуноглобулиновая терапия почти всегда приносит улучшение симптомов. Иммуноглобулин извлекается из большого пула плазмы человека; он состоит в основном из IgG и содержит все важные антитела, присутствующие в нормальной популяции. (См. Главу «Иммуноглобулинотерапия и другие медицинские методы лечения дефицита антител».) Пациентам с хроническим синуситом или хроническим заболеванием легких также может потребоваться длительное лечение антибиотиками широкого спектра действия. При подозрении на микоплазму или другие хронические инфекции могут быть показаны антибиотики, специфичные для этих микроорганизмов. Если развилась бронхоэктазия, может потребоваться ежедневный режим легочного туалета (физиотерапия грудной клетки и постуральный дренаж), чтобы мобилизовать секреты из легких и бронхов и облегчить их откашливание.Пациентов с желудочно-кишечными симптомами и мальабсорбцией следует обследовать на предмет наличия лямблий Giardia, ротавируса и ряда других желудочно-кишечных инфекций. В некоторых случаях обнаруживается воспалительное заболевание кишечника, которое лечат с помощью лекарств, обычно назначаемых пациентам с неиммунодефицитом. Поддержание баланса между иммуносупрессией, используемой для контроля аутоиммунного процесса, при одновременном избежании усугубления дефектов основного первичного иммунодефицита требует тесного сотрудничества между пациентом и различными специалистами, оказывающими им помощь. (См. Главу «Аутоиммунитет при первичном иммунодефиците».) Если развиваются аутоиммунные или воспалительные заболевания, гранулемы или опухоли, лечение обычно такое же, как и для людей с нормальной иммунной системой. Однако, когда пациенты с ОВИН имеют эти осложнения, они, как правило, хуже реагируют на терапию. Рекомендуются регулярные осмотры, в том числе функции легких.
Ожидания для пациентов с общим вариабельным иммунодефицитом
Заместительная иммуноглобулиновая терапия в сочетании с терапией антибиотиками значительно улучшила прогноз пациентов с ОВИН.Цель лечения — уберечь пациента от инфекций и предотвратить развитие хронических воспалительных изменений в тканях. Перспективы пациентов с ОВИН зависят от того, сколько повреждений было нанесено их легким или другим органам до постановки диагноза и начала лечения заместительной иммуноглобулиновой терапией, а также от того, насколько успешно можно предотвратить инфекции в будущем с помощью этих методов лечения. Развитие аутоиммунных заболеваний, воспалительных заболеваний, гранулем или злокачественных новообразований может существенно повлиять на качество жизни и реакцию на лечение.


