— переваривание — Биохимия
Эмульгирование и гидролиз липидов
Первые два этапа переваривания липидов, эмульгирование и гидролиз, происходят практически одновременно. Вместе с этим, продукты гидролиза не удаляются, а оставаясь в составе липидных капелек, облегчают дальнейшее эмульгирование и работу ферментов.
Переваривание в ротовой полости
У взрослых в ротовой полости переваривание липидов не идет, хотя длительное пережевывание пищи способствует частичному эмульгированию жиров.
Переваривание в желудке
Собственная липаза желудка у взрослого не играет существенной роли в переваривании липидов из-за ее небольшого количества и того, что ее оптимум рН 4,5-5,5. Также влияет отсутствие эмульгированных жиров в обычной пище (кроме молока).
Тем не менее, у взрослых теплая среда и перистальтика желудка вызывает некоторое эмульгирование жиров. При этом даже низко активная липаза расщепляет незначительные количества жира, что важно для дальнейшего переваривания жиров в кишечнике, т. к. наличие хотя бы минимального количества свободных жирных кислот облегчает эмульгирование жиров в двенадцатиперстной кишке и стимулирует секрецию панкреатической липазы.
к. наличие хотя бы минимального количества свободных жирных кислот облегчает эмульгирование жиров в двенадцатиперстной кишке и стимулирует секрецию панкреатической липазы.
Переваривание в кишечнике
Под влиянием перистальтики ЖКТ и составных компонентов желчи пищевой жир эмульгируется. Образующиеся при переваривании лизофосфолипиды также являются хорошим поверхностно-активным веществом, поэтому они способствуют дальнейшему эмульгированию пищевых жиров и образованию мицелл. Размер капель такой жировой эмульсии не превышает 0,5 мкм.
Гидролиз эфиров ХС осуществляет холестерол-эстераза панкреатического сока.
|
|
Роль колипазы в действии липазы
|
Переваривание ТАГ в кишечнике осуществляется под воздействием панкреатической липазы с оптимумом рН 8,0-9,0. В кишечник она поступает в виде пролипазы, для проявления ее активности требуется колипаза, которая помогает липазе расположиться на поверхности липидной капли.
Колипаза, в свою очередь, активируется трипсином и затем образует с липазой комплекс в соотношении 1:1. Панкреатическая липаза отщепляет жирные кислоты, связанные с С1 и С3 атомами углерода глицерола. В результате ее работы остаются 2-моноацилглицеролы (2-МАГ), которые всасываются в составе мицелл или превращаются моноглицерол-изомеразой в 1-МАГ. Последний гидролизуется до глицерола и жирной кислоты. Примерно 3/4 ТАГ после гидролиза остаются в форме 2-МАГ и только 1/4 часть ТАГ гидролизуется полностью.
Полный ферментативный гидролиз триацилглицерола
В панкреатическом соке также имеется активируемая трипсином фосфолипаза А2, отщепляющая в фосфолипидах жирную кислоту от С2, также обнаружена активность фосфолипазы С и лизофосфолипазы.
Действие фосфолипазы А
2 и лизофосфолипазы на примере фосфатидилхолина
В кишечном соке также имеется активность фосфолипазы А2 и фосфолипазы С.
Для работы всех указанных гидролитических ферментов в кишечнике необходимы ионы Са2+, способствующие удалению жирных кислот из зоны катализа.
Точки действия фосфолипаз
Образование мицелл
В результате воздействия на эмульгированные жиры ферментов панкреатического и кишечного соков образуются 2-моноацилглицеролы, свободные жирные кислоты и свободный холестерол, формирующие структуры мицеллярного типа (размер уже около 5 нм). Свободный глицерол всасывается напрямую в кровь.
Схематичное изображение переваривания липидов
Полученные смешанные мицеллы достигают эпителия кишечника и их компоненты диффундируют в клетки и попадают в гладкую эндоплазматическую сеть. Желчные кислоты почти не всасываются и остаются в просвете кишечника. Далее желчные кислоты достигают подвздошной кишки и всасываются там (Кишечно-печеночная циркуляция).
7.6. Переваривание липидов
Для взрослого
человека суточная потребность в липидах
составляет от 70-80 г до 100 г, для детей5 – 7 г/кг.
У взрослых людей
процесс переваривания липидов происходит
в тонком кишечнике. Необходимыми
условиями для этого являются:
— наличие ферментов;
— оптимальное рН;
— эмульгирование
жиров.
Необходимость
эмульгирования липидов связана с
водонерастворимостью жиров. Водорастворимые
ферменты могут действовать на липиды
только на поверхности капли. Эмульгирование
повышает поверхность раздела липид /
вода и обеспечивает большую поверхность
контакта фермента и липида. В эмульгировании
липидов основную роль играют жёлчные
кислоты, выделяемые в просвет кишечника
в составе жёлчи.
Различают простые
и парные, первичные и вторичные жёлчные
кислоты:
Простые жёлчные
кислоты являются производными холановой
кислоты.
К простым жёлчным
кислотам относятся холевая, дезоксихолевая
кислота, хенодезоксихолевая и литохолевая
кислоты.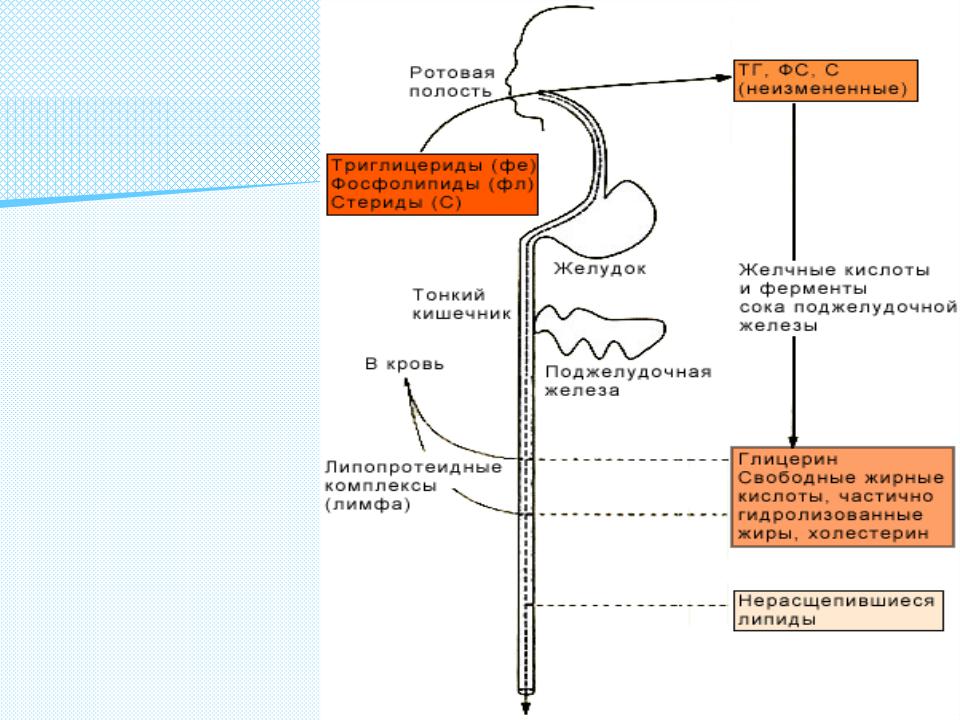
Синтез жёлчных
кислот из холестерина происходит в
печени. Ключевым ферментом является 7
– α -гидроксилаза. Она переводит
холестерин при участии цитохрома Р450в 7-α — холестерин — 3,7 (ОН)2. Он, в
свою очередь, переходит в хенодезоксихолевую
кислоту — 3,7 (ОН)2путём укорочения
бокового радикала и в холевую кислоту
— 3,7,12 (ОН)3. Эти две кислоты являютсяпервичнымижёлчными кислотами.
Полярность простых
жёлчных кислот увеличивается при
образовании парных жёлчных кислот
путём присоединения глицина (гликокола)
и таурина.
У взрослого
человека до 80% всех жёлчных кислот
представлено гликохолевой и таурохолевой
кислотами. В кишечнике под действием
микрофлоры происходит отцепление
таурина, гликокола и ОН группы в 7
положении с образованием вторичных
желчных кислот: дезоксихолевой и
литохолевой.
Все жёлчные кислоты
относятся к поверхностно активным
веществам, имеющим в своем составе
гидрофобные и гидрофильные участки.
Гидрофильными являются ОН — группы,
остатки таурина и гликокола, а гидрофобными
– радикал жёлчной кислоты. Благодаря
дифильности жёлчные кислоты располагаются
в поверхностном слое жировой капли и
уменьшают поверхностное натяжение.
В результате
снижения поверхностного натяжения под
действием перистальтики кишечника,
выделения СО2в результате
нейтрализации бикарбонатами соляной
кислоты желудочного содержимого
происходит дробление крупных капель
липида на множество мелких – эмульгирование,
резко возрастает поверхность
соприкосновения липидных капель и
ферментов.
Липолитические
ферменты, участвующие в переваривании
липидов, активны при pН 8
– 8,5. Такая среда обеспечивается секрецией
бикарбонатов поджелудочной железой.
Основные ферменты
переваривания липидов вырабатываются
поджелудочной железой и стенкой тонкого
кишечника.
Впереваривании
ТАГучаствует поджелудочная липаза.
Она вырабатывается в неактивной форме,
и в тонком кишечнике взаимодействует
с дополнительным белком колипазой,
который повышает активность липазы и
обеспечивает контакт фермента с
соответствующими жирами. Поджелудочная
липаза отщепляет последовательно
остатки жирных кислот из α — положений
с образованием β – моноацилглицерина
(β -МАГ)
Образующиеся
бета-МАГ в случае изомеризации в α –МАГ
могут в дальнейшем подвергаться
расщеплению под действием липазы до
глицерина и жирных кислот. Около 50% МАГ
подвергается всасыванию.
Переваривание
глицерофосфолипидов происходит
под действием ферментов фосфолипаз
поджелудочной железы. Под действием
фосфолипазы А2 отщепляется остаток
жирной кислоты из β – положения с
образованием продукта неполного распада
глицерофосфолипида – лизофосфолипида,
содержащего в β – положении гидрофильную
гидроксильную группу. Лизофосфолипиды
являются поверхностно активными
веществами и усиливают процессы
эмульгирования жиров. Лизофосфолипиды
Лизофосфолипиды
расщепляются лизофосфолипазой на жирную
кислоту и глицерофосфохолин, который
хорошо всасывается без гидролиза. Таким
образом, при распаде глицерофосфолипидов
образуются жирные кислоты и
глицерофосфохолин.
Эфиры холестеринарасщепляются ферментом холестеролэстеразой.
Переваривание
сфинголипидовосуществляется
ферментами эстеразами, фосфатазами,
амидазами, гликозидазами.
Биохимия питания и пищеварения. Переваривание и всасывание белков, жиров, углеводов.
10.3.1. Основным местом переваривания липидов является верхний отдел тонкого кишечника. Для переваривания липидов необходимы следующие условия:
- наличие липолитических ферментов;
- условия для эмульгирования липидов;
- оптимальные значения рН среды (в пределах 5,5 – 7,5).
10. 3.2. В расщеплении липидов участвуют различные ферменты. Пищевые жиры у взрослого человека расщепляются в основном панкреатической липазой; обнаруживается также липаза в кишечном соке, в слюне, у грудных детей активна липаза в желудке. Липазы относятся к классу гидролаз, они гидролизуют сложноэфирные связи -О-СО- с образованием свободных жирных кислот, диацилглицеролов, моноацилглицеролов, глицерола (рисунок 10.3).
3.2. В расщеплении липидов участвуют различные ферменты. Пищевые жиры у взрослого человека расщепляются в основном панкреатической липазой; обнаруживается также липаза в кишечном соке, в слюне, у грудных детей активна липаза в желудке. Липазы относятся к классу гидролаз, они гидролизуют сложноэфирные связи -О-СО- с образованием свободных жирных кислот, диацилглицеролов, моноацилглицеролов, глицерола (рисунок 10.3).
Рисунок 10.3. Схема гидролиза жиров.
Поступающие с пищей глицерофосфолипиды подвергаются воздействию специфических гидролаз – фосфолипаз, расщепляющих сложноэфирные связи между компонентами фосфолипидов. Специфичность действия фосфолипаз показана на рисунке 10.4.
Рисунок 10.4. Специфичность действия ферментов, расщепляющих фосфолипиды.
Продуктами гидролиза фосфолипидов являются жирные кислоты, глицерол, неорганический фосфат, азотистые основания (холин, этаноламин, серин).
Пищевые эфиры холестерола гидролизуются панкреатической холестеролэстеразой с образованием холестерола и жирных кислот.
10.3.3. Уясните особенности структуры желчных кислот и их роль в переваривании жиров. Желчные кислоты – конечный продукт обмена холестерола, образуются в печени. К ним относятся: холевая (3,7,12-триоксихолановая), хенодезоксихолевая (3,7-диоксихолановая)и дезоксихолевая (3, 12-диоксихолановая) кислоты (рисунок 10.5, а). Две первые являются первичными желчными кислотами (образуются непосредственно в гепатоцитах), дезоксихолевая – вторичной (так как образуется из первичных желчных кислот под влиянием микрофлоры кишечника).
В желчи эти кислоты присутствуют в конъюгированной форме, т.е. в виде соединений с глицином Н2N-СН2-СООН или таурином Н2N-СН2-СН2-SO3H (рисунок 10.5, б).
Рисунок 10. 5. Строение неконъюгированных (а) и конъюгированных (б) желчных кислот.
5. Строение неконъюгированных (а) и конъюгированных (б) желчных кислот.
15.1.4. Желчные кислоты обладают амфифильными свойствами: гидроксильные группы и боковая цепь гидрофильны, циклическая структура гидрофобна. Эти свойства обусловливают участие желчных кислот в переваривании липидов:
1) желчные кислоты способны эмульгировать жиры, их молекулы своей неполярной частью адсорбируются на поверхности жировых капель, в то же время гидрофильные группы вступают во взаимодействие с окружающей водной средой. В результате снижается поверхностное натяжение на границе раздела липидной и водной фаз, вследствие чего крупные жировые капли разбиваются на более мелкие;
2) желчные кислоты наряду с колипазой желчи участвуют в активировании панкреатической липазы, сдвигая её оптимум рН в кислую сторону;
3) желчные кислоты образуют с гидрофобными продуктами переваривания жиров водорастворимые комплексы, что способствует их всасыванию в стенку тонкого кишечника.
Желчные кислоты, проникающие в процессе всасывания вместе с продуктами гидролиза в энтероциты, через портальную систему поступают в печень. Эти кислоты могут повторно секретироваться с желчью в кишечник и участвовать в процессах переваривания и всасывания. Такая энтеро-гепатическая циркуляция желчных кислот может осуществляться до 10 и более раз в сутки.
15.1.5. Особенности всасывания продуктов гидролиза жиров в кишечнике представлены на рисунке 10.6. В процессе переваривания пищевых триацилглицеролов около 1/3 их расщепляется полностью до глицерола и свободных жирных кислот, приблизительно 2/3 гидролизуется частично с образованием моно- и диацилглицеролов, небольшая часть совсем не расщепляется. Глицерол и свободные жирные кислоты с длиной цепи до 12 углеродных атомов растворимы в воде и проникают в энтероциты, а оттуда через воротную вену в печень. Более длинные жирные кислоты и моноацилглицеролы всасываются при участии конъюгированных желчных кислот, формирующих мицеллы. Нерасщеплённые жиры, по-видимому, могут поглощаться клетками слизистой кишечника путём пиноцитоза. Нерастворимый в воде холестерол, подобно жирным кислотам, всасывается в кишечнике в присутствии желчных кислот.
Рисунок 10.6. Переваривание и всасывание ацилглицеролов и жирных кислот.
Страница не найдена |
Страница не найдена |
404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
27282930
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Метки
Настройки
для слабовидящих
ПЕРЕВАРИВАНИЕ И ВСАСЫВА¬НИЕ ПИЩЕВЫХ ЛИПИДОВ
ПЕРЕВАРИВАНИЕ И ВСАСЫВА¬НИЕ ПИЩЕВЫХ ЛИПИДОВ
. С пищей в организм ежедневно поступает от 80 до 150 г липидов. Основную массу составляют жиры, наряду с глюкозой служащие главными источниками энергии. Хотя калорийность жиров значи-тельно выше, чем углеводов (9 по сравнению с 4,7 ккал/моль), при рациональном питании жиры обеспечивают не более 30% от общего количества калорий, поступающих с пищей. Жидкие жиры (масла) содержат в своём составе полиеновые жирные кислоты, которые не синтезируются в организме; поэтому жидкие жиры должны составлять не менее одной трети жиров пищи. С ли-пидами в организм поступают и жирорастворимые витамины A, D, Е, К. Переваривание липидов пищи происходит в кишечнике. Основные продукты гидролиза (жирные кислоты и 2-моно-ацилглицеролы) после всасывания подвергаются ресинтезу и последующей упаковке в хиломикроны (ХМ) в клетках слизистой оболочки кишечника. Ресинтез жиров в слизистой оболочке тонкого кишечника. После всасывания продуктов гидролиза жиров жирные кислоты и 2-моноацилглицеролы в клетках слизи-стой оболочки тонкого кишечника включаются в процесс ре-синтеза с образованием триацилглицеролов). Жирные кислоты вступают в реакцию этерификации только в активной форме в виде производных коэнзима А, поэтому первая стадия ресинтеза жиров — реакция активации жирной кислоты: HS КоА + RCOOH + АТФ → R-CO ~ КоА + АМФ + Н4Р2О7. Реакция катализируется ферментом ацил-КоА-синтетазой (тиокиназой). Затем ацил~КоА участвует в реакции этерификации 2-моноацилглицерола с обра-зованием сначала диацилгли-церола, а затем триацилглицерола. Реакции ресинтеза жиров катализируют ацилтранеферазы. В реакциях ресинтеза жиров участвуют, как правило, только жирные кислоты с длинной углеводородной цепью. В ресинтезе жиров участвуют не только жирные кислоты, всосавшиеся из кишечника, но и жирные кислоты, синтезированные в организме, поэтому по составу ре-синтезированные жиры отличаются от жиров, полученных с пищей. Однако возможности «адаптировать» в процессе ресинтеза состав пищевых жиров к составу жиров организма человека ограничены, поэтому при поступлении с пищей жиров с необычными жирными кислотами,
Рис. Ресинтез жиров в клетках слизистой оболочки тонкой кишки. например бараньего жира, в адипоцитах появляются жиры, содержащие кислоты, характерные для бараньего жира (насы-щенные разветвлённые жирные кислоты). В клетках слизистой оболочки кишечника происходит активный синтез глицерофосфолипидов, необходимых для формирования структуры липопротеинов — транспортных форм липидов в крови. Желчные кислоты играют важную роль в переваривании и всасывании липидов. В тонкой кишке конъюгированные желчные кислоты, являясь поверхностно-активными веществами, адсорбируются в присутствии свободных жирных кислот и моноглицеридов на поверхности капелек жира, образуя при этом тончайшую пленку, препятствующую слиянию мельчайших капелек жира в более крупные. При этом происходит резкое снижение поверхностного натяжения на границе двух фаз — воды и жира, что приводит к образованию эмульсии с размерами частиц 300-1000 ммк и мице-лярного раствора с размерами частиц 3-30 ммк. Образование мицеллярных растворов облегчает действие панкреатической липазы, которая при воздействии на жиры расщепляет их на глицерин, легко всасывающийся кишечной стенкой, и жирные кислоты, нерастворимые в воде. Желчные кислоты, соединяясь с последними, образуют холеиновые кислоты, хорошо растворимые в воде и поэтому легко всасывающиеся кишечными ворсинками в верхних отделах тонкой кишки. Вторая существенная роль желчных кислот — регуляция синтеза холестерина и его деградации. Скорость синтеза холестерина в тонкой кишке зависит от концентрации желчных кислот в просвете кишки. Основная часть холестерина в организме человека образуется путем синтеза, а незначи-тельная часть поступает с пищей. Таким образом, влияние желчных кислот на обмен холестерина заключается в под-держании его баланса в организме. Желчные кислоты сводят к минимуму нарастание или недостаток холестерина в организме.
Учебная программа лечебного факультета
Содержание предмета биохимия. Биохимия белка. Строение, физико–химические и химические свойства протеиногенных аминокислот и белков. Классификации белков. Функции белков и пептидов. Биосинтез белка. Конформация белковой молекулы. Механизмы взаимодействия белок–лиганд. Денатурация белка. Методы исследования белков. Энзимология. Строение и механизмы функционирования ферментов. Классификация, индексация и номенклатура ферментов. Особенности ферментов в качестве биологических катализаторов. Кинетика ферментативного катализа. Уровни регуляции ферментов. Понятие о метаболических путях. Катаболизм и анаболизм. Энзимодиагностика и энзимотерапия. Типы и механизмы биологического окисления. Митохондриальное окисление: субстраты, цепи транспорта электронов, сопряжение с процессом окислительного фосфорилирования. Виды внемитохондриального окисления, их роль. Активные формы кислорода. Антиоксидантная система. Биологически важные углеводы человека. Переваривание и всасывание углеводов. Метаболические пути обмена углеводов, связанные с получением энергии в виде АТФ. Структурные углеводы, их синтез. Роль ГАГ, протеогликанов, углеводных компонентов гликопротеинов и гликолипидов. Источники глюкозы в крови, регуляция ее концентрации. Механизмы гликирования и гликозилирования биомолекул. Липиды организма человека: определение, классификация. Переваривание и всасывание липидов. Строение и функции триглицеридов. Синтез и распад триглицеридов. Кетоновые тела: их синтез, утилизация и роль в организме человека. Мембранные липиды: строение, свойства, роль. Синтез и распад мембранных липидов. Системы транспорта липидов. Фракции липопротеинов, методы их исследования. Биологически активные продукты катаболизма липидов. Многообразие белков организма человека. Механизмы посттрансляционной модификации белка. Азотистый баланс. Пищевая ценность белков. Переваривание белков в желудочно–кишечном тракте, всасывание аминокислот. Этапы катаболизма белка. Протеолиз. Роль тотального и ограниченного протеолиза. Регуляция протеолитических систем. Трансаминирование и дезаминирование аминокислот. Синтез заменимых аминокислот. Пути образования и обезвреживания аммиака. Пути образования и обезвреживания биологически активных продуктов аминокислотного обмена. Синтез, распад и роль креатина. Роль аминокислот в синтезе гемма и нуклеиновых кислот. Строение и функции нуклеиновых кислот. Функции нуклеотидов. Биохимические основы синтеза нуклеиновых кислот. Посттранскрипционная модификации РНК. Синтез и распад нуклеотидов. Строение и классификация гемопротеинов. Молекулярные формы и производные гемоглобина. Синтез и распад гема. Прямой и непрямой билирубин. Обмен воды и минеральный веществ и их регуляция. Состав плазмы крови. Белковые фракции крови. Функции белковых и небелковых компонентов крови. Система свертывания крови и фибринолиза. Белки иммунной системы. Системы регуляции сосудистого тонуса. Особенности химического состава и метаболизма эритроцитов и лейкоцитов. Состав миоцитов. Механизм мышечного сокращения. Источники энергии для мышечной ткани. Особенности химического состава и метаболизма нервной ткани. Химическая классификация нейромедиаторов. Функции почек. Биохимические механизмы экскреторной и гомеостатичской функций почек. Гормоны почки. Гормональная регуляция мочеобразования. Химический состав мочи человека.
Химическое пищеварение | Безграничная анатомия и физиология
Механизмы химического пищеварения
Химическое пищеварение — это опосредованный ферментами процесс гидролиза, который расщепляет крупные макроэлементы на более мелкие молекулы.
Цели обучения
Различать методы, используемые для химического расщепления молекул пищи
Основные выводы
Ключевые моменты
- Углеводы в основном поступают в виде амилозы и гликогена.Амилазы гидролизуют длинные углеводные цепи, которые расщепляют амилозу на дисахариды, а гликоген — на полисахариды. Затем ферменты тонкого кишечника расщепляют их на моносахариды.
- Белки перевариваются путем гидролиза связи углерод – азот (C – N). Пептидазы секретируются в неактивной форме, чтобы предотвратить самопереваривание. Эндопептидазы расщепляют полипептиды по внутренним пептидным связям, а экзопептидазы расщепляют концевые аминокислоты.
- Жиры перевариваются липазами, которые гидролизуют связи глицерина и жирных кислот.Соли желчных кислот эмульгируют жиры, чтобы позволить их растворению в виде мицелл в химусе и увеличить площадь поверхности, на которой действуют липазы поджелудочной железы.
- РНК и ДНК гидролизуются ферментами поджелудочной железы (рибонуклеазами, дезоксирибонуклеазами) в нуклеиновые кислоты, которые далее расщепляются на пуриновые и пиримидиновые основания и пентозы ферментами слизистой оболочки кишечника (нуклеазами).
- После того, как мозг отправляет добровольный сигнал к дефекации, начинается заключительная фаза.
Ключевые термины
- пептидаза : любой фермент, катализирующий гидролиз пептидов до аминокислот; протеаза.
- амилаза : любой из класса пищеварительных ферментов, присутствующих в слюне и расщепляющих сложные углеводы, такие как крахмал, на простые сахара, такие как глюкоза.
- гидролиз : разложение определенных биополимеров (белков, сложных сахаров) в результате химического процесса, в результате которого образуются более мелкие полимеры или мономеры, такие как аминокислоты или моносахариды.
Примеры
Поскольку амилаза превращает немного картофельного или рисового крахмала в сахар, эти продукты имеют слегка сладкий вкус.
Пищеварение — это форма катаболизма: расщепление больших молекул пищи (например, полисахаридов, белков, жиров, нуклеиновых кислот) на более мелкие (например, моносахариды, аминокислоты, жирные кислоты, нуклеотиды).
Катаболизм : упрощенная схема катаболизма белков, углеводов и жиров.
Углеводы поступают в основном в форме углеводов растений (амилоза) и углеводов животных (гликоген) вместе с некоторыми сахарами, в основном дисахаридами.Около 80% западной диеты состоит из амилозы. Амилоза не является сильно разветвленной и состоит в основном из длинных цепей глюкозы, связанных связями α1: 4.
Целлюлоза, самый распространенный в природе крахмал, состоит из связей β1: 4 и не может быть переварена у человека, хотя бактерии в толстой кишке разрушают ее незначительное количество.
Гликоген — это разветвленный крахмал со связями в положении 1: 4 и 1: 6. Это создает очень большие гранулы разветвленного крахмала.И околоушная, и панкреатическая амилазы гидролизуют связь 1: 4, но не концевые связи 1: 4 или 1: 6. Это расщепляет амилозу в основном на дисахариды и гликоген с его связями 1: 6 на полисахариды.
Конечным результатом этих действий являются многочисленные дисахариды и полисахариды. Ферменты, прикрепленные к энтероцитам тонкого кишечника, расщепляют их на моносахариды.
Гидролиз амилазой : И околоушная, и панкреатическая амилазы гидролизуют связь 1: 4, но не концевые связи 1: 4 или связи 1: 6.
Белки и полипептиды расщепляются путем гидролиза связи углерод – азот (C – N). Все протеолитические ферменты секретируются в неактивной форме для предотвращения самопереваривания и активируются в просвете кишечника. Активация вызывается HCl в случае желудочного фермента пепсиногена и энтеропептидазой и трипсином в случае ферментов поджелудочной железы.
Окончательное пищеварение происходит с помощью ферментов тонкого кишечника, которые встроены в щеточную кайму тонкой кишки.Ферменты делятся на эндо- и экзопептидазы.
- Эндопептидазы расщепляют полипептид по внутренним пептидным связям, в то время как экзопептидазы расщепляют концевую аминокислоту.
- Экзопептидазы далее подразделяются на аминопептидазы, которые отщепляют концевую аминокислоту на аминовом конце цепи, и карбоксипептидазы, которые отщепляют концевую аминокислоту на карбоксильном конце цепи.
Желудочный пепсин расщепляет внутренние связи аминокислот и особенно важен из-за его способности переваривать коллаген.Это основной компонент соединительной ткани мяса. При отсутствии желудочного пепсина пищеварение в тонкой кишке протекает с трудом. Пепсин желудка переваривает около 20% белков, а остальные перевариваются ферментами поджелудочной железы и тонкого кишечника.
Гидролиз пептидной связи : Белки и полипептиды расщепляются путем гидролиза связи C – N.
Жиры перевариваются липазами, которые гидролизуют связи глицерина и жирных кислот. Особое значение в переваривании и всасывании жиров имеют соли желчных кислот, которые эмульгируют жиры, чтобы обеспечить их растворение в виде мицелл в химусе и увеличить площадь поверхности, на которой действуют липазы поджелудочной железы.
Липазы обнаружены во рту, желудке и поджелудочной железе. Поскольку лингвальная липаза инактивируется желудочной кислотой, формально считается, что она присутствует в основном для гигиены полости рта и для ее антибактериального действия во рту. Тем не менее, он может продолжать воздействовать на пищу, хранящуюся на дне желудка, и эта липаза может переваривать до 30% жиров.
Желудочная липаза не имеет большого значения для человека. Липаза поджелудочной железы отвечает за переваривание жиров и действует вместе с солями желчных кислот.
РНК и ДНК гидролизуются ферментами поджелудочной железы (рибонуклеазами, дезоксирибонуклеазами) до нуклеиновых кислот, которые далее расщепляются на пуриновые и пиримидиновые основания и пентозы ферментами слизистой оболочки кишечника (нуклеазами).
Химическое расщепление углеводов, белков, липидов и нуклеиновых кислот
Химический распад макромолекул, содержащихся в пище, завершается различными ферментами, вырабатываемыми пищеварительной системой.
Цели обучения
Краткое описание химического разложения
Основные выводы
Ключевые моменты
- Переваривание белков происходит в желудке и двенадцатиперстной кишке под действием трех основных ферментов: пепсина, секретируемого желудком, и трипсина и химотрипсина, секретируемых поджелудочной железой.
- Во время переваривания углеводов связи между молекулами глюкозы разрушаются амилазой слюны и поджелудочной железы.
- Переваривание некоторых жиров начинается во рту, где короткоцепочечные липиды распадаются на диглицериды из-за лингвальной липазы. Жир, присутствующий в тонком кишечнике, стимулирует высвобождение липазы из поджелудочной железы, а желчь из печени способствует расщеплению жиров на жирные кислоты.
- расщепляются на мононуклеотиды под действием нуклеаз дезоксирибонуклеазы и рибонуклеазы (ДНКазы и РНКазы), которые выделяются поджелудочной железой.
ДНК и РНК
Ключевые термины
- зимоген : профермент или предшественник фермента, который требует биохимического изменения (т. Е. Гидролиза), чтобы стать активной формой фермента.
- Непереносимость лактозы : Неспособность полностью усваивать лактозу.
Химическое разложение
Переваривание белков происходит в желудке и двенадцатиперстной кишке под действием трех основных ферментов:
- Пепсин, секретируемый желудком.
- Трипсин, секретируемый поджелудочной железой.
- Химотрипсин, секретируемый поджелудочной железой.
Эти ферменты расщепляют пищевые белки на полипептиды, которые затем расщепляются различными экзопептидазами и дипептидазами на аминокислоты. Однако пищеварительные ферменты секретируются в основном в виде их неактивных предшественников, зимогенов.
Таким образом, трипсин секретируется поджелудочной железой в форме трипсиногена, который активируется в двенадцатиперстной кишке энтерокиназой с образованием трипсина.Затем трипсин расщепляет белки на более мелкие полипептиды.
У людей диетические крахмалы состоят из единиц глюкозы, расположенных в длинные цепочки полисахарида, называемого амилозой. Во время пищеварения связи между молекулами глюкозы разрушаются амилазой слюны и поджелудочной железы, в результате чего цепи глюкозы постепенно уменьшаются. В результате этого процесса производятся простые сахара, глюкоза и мальтоза (две молекулы глюкозы), которые могут всасываться в тонком кишечнике.
Сахараза — это фермент, расщепляющий дисахарид сахарозы, широко известный как столовый сахар, тростниковый сахар или свекольный сахар.При переваривании сахарозы образуются сахара, фруктоза и глюкоза, которые легко усваиваются тонким кишечником.
Лактаза — это фермент, расщепляющий дисахарид лактозу на составные части, глюкозу и галактозу, которые всасываются в тонком кишечнике. Примерно половина взрослого населения вырабатывает лишь небольшое количество лактазы и поэтому не может есть молочные продукты. Это состояние широко известно как непереносимость лактозы.
Переваривание некоторых жиров начинается во рту, где липаза языка расщепляет липиды с короткой цепью на диглицериды.Присутствие жира в тонком кишечнике производит гормоны, которые стимулируют высвобождение липазы поджелудочной железы из поджелудочной железы и желчи из печени, что способствует расщеплению жиров на жирные кислоты. Полное переваривание одной молекулы жира (триглицерида) приводит к образованию трех молекул жирных кислот и одной молекулы глицерина.
ДНК и РНК
расщепляются на мононуклеотиды под действием нуклеаз дезоксирибонуклеаза и рибонуклеаза (ДНКаза и РНКаза), которые выделяются поджелудочной железой.
Переваривание углеводов : Диаграмма действия ферментов, расщепляющих олигосахариды, в тонком кишечнике.
Переваривание липидов : Переваривание липидов включает образование мицелл в присутствии солей желчных кислот и прохождение мицелл и жирных кислот через слой без перемешивания. На диаграмме вверху изображен пищевой жир, а липаза поджелудочной железы и соли желчных кислот образуют мицеллы, которые проходят через слой без перемешивания внизу диаграммы.
5.4: Переваривание и всасывание липидов
Цели обучения
- Обобщите этапы переваривания и абсорбции липидов.
- Объясните, как липиды используются для получения энергии и накапливаются в организме.
Липиды представляют собой большие молекулы и обычно не растворяются в воде. Подобно углеводам и белкам, липиды расщепляются на мелкие компоненты для всасывания. Поскольку большинство наших пищеварительных ферментов имеют водную основу, как организм расщепляет жир и делает его доступным для различных функций, которые он должен выполнять в организме человека?
Ото рта к желудку
Первый шаг в переваривании триацилглицеринов и фосфолипидов начинается во рту, когда липиды попадают в слюну.Затем физическое действие жевания в сочетании с действием эмульгаторов позволяет пищеварительным ферментам выполнять свои задачи. Фермент лингвальная липаза вместе с небольшим количеством фосфолипида в качестве эмульгатора инициирует процесс пищеварения. Эти действия делают жиры более доступными для пищеварительных ферментов. В результате жиры становятся крошечными капельками и отделяются от водянистых компонентов.
Рисунок \ (\ PageIndex {1} \): Переваривание липидов
В желудке липаза желудка начинает расщеплять триацилглицерины на диглицериды и жирные кислоты.В течение двух-четырех часов после еды примерно 30 процентов триацилглицеринов превращаются в диглицериды и жирные кислоты. Взбалтывание и сокращение желудка помогают рассеять молекулы жира, а диглицериды, полученные в этом процессе, действуют как дополнительные эмульгаторы. Однако даже при всей этой активности в желудке происходит очень слабое переваривание жиров.
Идя в кровоток
Когда содержимое желудка попадает в тонкий кишечник, пищеварительная система решает преодолеть небольшое препятствие, а именно объединить отделенные жиры с собственными водянистыми жидкостями.Решение этой проблемы — желчь. Желчь содержит соли желчных кислот, лецитин и вещества, полученные из холестерина, поэтому она действует как эмульгатор. Он притягивает и удерживает жир, в то время как он одновременно притягивается и удерживается водой. Эмульгирование увеличивает площадь поверхности липидов более чем в тысячу раз, делая их более доступными для пищеварительных ферментов.
После эмульгирования содержимого желудка ферменты, расщепляющие жир, воздействуют на триацилглицерины и диглицериды, отделяя жирные кислоты от их глицериновой основы.Когда липаза поджелудочной железы попадает в тонкий кишечник, она расщепляет жиры на свободные жирные кислоты и моноглицериды. И снова возникает еще одно препятствие. Как жиры будут проходить через водянистый слой слизи, покрывающей абсорбирующую оболочку пищеварительного тракта? Как и раньше, ответ — желчь. Соли желчных кислот обволакивают жирные кислоты и моноглицериды с образованием мицелл. Мицеллы имеют ядро из жирных кислот с водорастворимой внешней стороной. Это обеспечивает эффективную транспортировку к микроворсинкам кишечника.Здесь жировые компоненты высвобождаются и распространяются по клеткам слизистой оболочки пищеварительного тракта.
Рисунок \ (\ PageIndex {2} \): Жиры могут перемещаться через водянистую среду тела благодаря процессу эмульсии.
Так же, как липиды требуют особого обращения в пищеварительном тракте для перемещения в водной среде, они требуют аналогичного обращения для перемещения в кровотоке. Внутри кишечных клеток моноглицериды и жирные кислоты снова собираются в триацилглицерины.Триацилглицерины, холестерин и фосфолипиды образуют липопротеины при соединении с белком-носителем. Липопротеины имеют внутреннее ядро, которое в основном состоит из триацилглицеринов и сложных эфиров холестерина (сложный эфир холестерина — это холестерин, связанный с жирной кислотой). Внешняя оболочка состоит из фосфолипидов с вкраплениями белков и холестерина. Вместе они образуют хиломикрон, большой липопротеин, который теперь попадает в лимфатическую систему и вскоре будет выпущен в кровоток через яремную вену на шее.Хиломикроны отлично переносят пищевые жиры через водную среду организма к определенным направлениям, таким как печень и другие ткани организма.
Холестерины плохо всасываются по сравнению с фосфолипидами и триацилглицеринами. Всасыванию холестерина способствует увеличение количества пищевых жировых компонентов, и этому препятствует высокое содержание клетчатки. Это причина того, что для снижения холестерина в крови рекомендуется высокое потребление клетчатки. Продукты с высоким содержанием клетчатки, такие как свежие фрукты, овощи и овес, могут связывать соли желчных кислот и холестерин, предотвращая их всасывание и вывод из толстой кишки.
Если жиры не усваиваются должным образом, как это наблюдается при некоторых заболеваниях, стул человека будет содержать большое количество жира. Если мальабсорбция жира сохраняется, состояние известно как стеаторея. Стеаторея может быть результатом заболеваний, влияющих на всасывание, таких как болезнь Крона и кистозный фиброз.
Правда о хранении и использовании жира
До того, как появилась пищевая промышленность, фитнес-центры и программы похудания, наши предки упорно трудились, чтобы даже найти еду.Они строили планы не на то, чтобы сбросить последние десять фунтов, чтобы надеть купальный костюм на время отпуска, а скорее на то, чтобы найти еду. Сегодня именно поэтому мы можем долгое время обходиться без еды, независимо от того, заболели ли мы с пропавшим аппетитом, повысился уровень физической активности или просто нет еды. Наши тела резервируют топливо на черный день.
Один из способов накопления жира в организме заключается в том, что организм преобразует углеводы в гликоген, который, в свою очередь, накапливается в мышцах для получения энергии. Когда мышцы достигают своей способности накапливать гликоген, его избыток возвращается в печень, где он превращается в триацилглицерины, а затем откладывается в виде жира.
Подобным образом большая часть триацилглицеринов, которые организм получает с пищей, транспортируется в хранилища жира внутри тела, если не используется для производства энергии. Хиломикроны отвечают за транспортировку триацилглицеринов в различные места, такие как мышцы, грудь, внешние слои под кожей и внутренние жировые слои живота, бедер и ягодиц, где они сохраняются организмом в жировой ткани для будущего использования. Как это достигается? Напомним, что хиломикроны — это большие липопротеины, которые содержат триацилглицерин и ядро жирных кислот.Стенки капилляров содержат фермент, называемый липопротеин-липазой, который расщепляет триацилглицерины липопротеинов на жирные кислоты и глицерин, позволяя им проникать в жировые клетки. Попав внутрь жировых клеток, жирные кислоты и глицерин снова собираются в триацилглицерины и сохраняются для дальнейшего использования. Мышечные клетки также могут поглощать жирные кислоты и использовать их для мышечной работы и выработки энергии. Когда потребности человека в энергии превышают количество доступного топлива, полученного от недавнего приема пищи или продолжительная физическая активность истощила запасы энергии гликогена, запасы жира извлекаются для использования энергии.
По мере того, как организм требует дополнительной энергии, жировая ткань реагирует, расщепляя свои триацилглицерины и выделяя глицерин и жирные кислоты непосредственно в кровь. Получив эти вещества, голодные до энергии клетки разбивают их на крошечные фрагменты. Эти фрагменты проходят серию химических реакций, в результате которых выделяются энергия, углекислый газ и вода.
Ключевые выводы
- В желудке жир отделяется от других пищевых веществ.В тонком кишечнике желчь эмульгирует жиры, а ферменты их переваривают. Клетки кишечника поглощают жиры.
- Длинноцепочечные жирные кислоты образуют большую липопротеиновую структуру, называемую хиломикроном, которая переносит жиры по лимфатической системе.
- Хиломикроны образуются в клетках кишечника и переносят липиды из пищеварительного тракта в кровоток.
- Короткие и средние жирные цепи могут всасываться непосредственно в кровоток из микроворсинок кишечника, поскольку они водорастворимы.
- Всасывание холестерина затруднено продуктами с высоким содержанием клетчатки.
- Когда запасы энергии низки, организм использует накопленные запасы жира для получения энергии.
Обсуждение стартеров
- Объясните роль эмульгаторов в переваривании жиров.
- Назовите часть пищеварительной системы, в которой происходит наибольшее переваривание и всасывание жиров.
- Опишите роль солей желчных кислот в переваривании триацилглицеринов и фосфолипидов.
- Определите хиломикрон.
- Объясните, как продукты, богатые клетчаткой, влияют на усвоение холестерина.
- Обсудите процессы организма по использованию энергии.
Переваривание жиров (триацилглицеринов) | Биохимические заметки
Переваривание жиров (триацилглицеринов)
Введение:
Триацилглицерины (также называемые нейтральным жиром или депо-жиром ) составляют 85-90% липидов организма.Эти триацилглицерины хранятся в жировой ткани в виде липидных капель, и служат в качестве запаса энергии для организма. Энергия, произведенная из этих восстановленных углеводородов (жиров), составляет удвоенных энергии, произведенной из того же веса углеводов или белков.
Более того, липиды обладают свойством быть нерастворимыми в воде (гидрофобными), и химически инертными , , таким образом, не имея риска взаимодействия с другим клеточным веществом. Таким образом, их пассивная природа не причиняет вреда клеткам и, следовательно, является хорошим хранилищем энергии.Эти накопленные жиры могут служить хорошим источником энергии во время длительных периодов голодания. Прекрасный пример использования этого накопленного жира наблюдается у медведей во время спячки и у перелетных птиц.
Жиры в основном перевариваются в тонком кишечнике желудочно-кишечного тракта (ЖКТ) . Для утилизации жиры, поскольку они гидрофобны по своей природе, сначала необходимо эмульгировать, чтобы они легко переваривались водорастворимыми ферментами в кишечнике. И для мобилизации этих жиров в крови они должны быть связаны с белками (такими как альбумин), чтобы противодействовать их нерастворимости.
Переваривание триацилглицеринов:
В организме человека есть три источника жира для получения энергии:
- Жир, полученный из пищевых продуктов
- Жир в жировой ткани
- Жир, вырабатываемый в печени из избыточных углеводов для передачи в другие ткани
Для использования диетических жиров
- Перед абсорбцией через кишечник эти гидрофобные (нерастворимые) жировые частицы должны быть преобразованы в микроскопически малых мицелл для увеличения их растворимости.Это достигается с помощью таких продуктов, как таурохолевая кислота , , которая представляет собой желчную соль , обычно выделяется в тонком кишечнике после приема пищи, богатой жирами, путем активации холецистокинина ( см. Изображение ниже ). Желчные соли — это , которые образуются из холестерина в печени и хранятся в желчном пузыре .
- Эти тонкодисперсные мицеллы, полученные в результате моющего действия солей желчных кислот, теперь обладают повышенной растворимостью.Теперь они гидролизуются липазой для превращения триацилглицеринов в моноацилглицерины, диацилглицерины, жирные кислоты и глицерин . Все образующиеся здесь конечные продукты диффундируют через слизистую оболочку эпителия.
Сводка усвоения жиров
- Пройдя через эпителиальную слизистую оболочку, они снова превращаются в триацилглицеринов и агрегируются с холестерином и аполипопротеинами с образованием хиломикронов .
- Аполипопротеины — это белки, которые связывают липиды и осуществляют транспортировку липидов, таких как триацилглицерины, холестерин, сложные эфиры холестерина и фосфолипиды. В зависимости от комбинации липида и белка производятся различные виды веществ разной плотности. Диапазон может варьироваться от очень липопротеинов низкой плотности (ЛПОНП) до липопротеинов очень высокой плотности (ЛПВП) .
- Поверхности клеток имеют специфические рецепторы для своих липопротеинов.Таким образом, для перехода от слизистой оболочки кишечника к лимфатической системе хиломикронов, , содержащих аполипопротеина C-II, , захватываются путем присоединения к рецепторам.
- Эти хиломикронов, затем достигают либо жировой ткани, либо мышц через крови в зависимости от их потребности.
- В капиллярах жировой ткани и мышц аполипопротеин C-II активирует фермент липопротеинлипазу , который расщепляет хиломикронов и гидролизует триацилглицеринов до жирных кислот и глицерина.
- Эти конечные продукты используются мышцами для получения энергии, тогда как в жировой ткани они повторно этерифицируются до триацилглицеринов для хранения.
- Оставшаяся часть хиломикронов , которая все еще содержит холестерин и аполипопротеины, перемещается в печень через кровь и через специфические рецепторы поглощается эндоцитозом.
- Некоторые триацилглицеринов , которые могли проникнуть через остатки хиломикрона в печень, используются для синтеза других клеточных компонентов.
Таким образом, при приеме жирной пищи часть ее используется столько, сколько требуется организму для выработки энергии, а оставшаяся фракция сохраняется в жировой ткани в виде липидных капель, которые при необходимости транспортируются. Чтобы утилизировать, сначала происходит мобилизация жиров и клеточное поглощение свободных жирных кислот с последующим окислением свободных жирных кислот для производства энергии.
Рекомендуемые тексты
- Дэвид Л.Нельсон и Майкл М. Кокс, Lehninger Principles of Biochemistry, 6th Edition
- Джереми М. Берг, Джон Л. Таймокцо и Любер Страйер, Биохимия, 7-е издание
- Реджинальд Х. Гаррет, Чарльз М. Гришам, Биохимия Реджинальда Х. Гарретта, 5-е издание .
- У. Сатьянараяна, У. Чакрапани, Биохимия У. Сатьянараяна. 3-е издание .
Похожие сообщения
Об авторе
Свити Мета
Учился Б.Pharm. в Институте фармации Мумбаи Образовательного траста (Мумбаи). 2 года и 9 месяцев проработал в Cipla, Мумбаи, менеджером по маркетингу. Получил диплом по маркетингу в Институте развития менеджмента и исследований Велингкара.
Поглощение пищевых жиров
Производство энергии из триацилглицеринов начинается с их гидролиза до свободных жирных кислот и глицерина. Ферменты, называемые липазами , , которые катализируют реакцию, осуществляют этот гидролиз.
В результате реакции высвобождаются три жирные кислоты и глицерин. Кишечный переносчик поглощает глицерин, который в конечном итоге соединяется с жирными кислотами в клетках кишечника.
Организм должен поглощать жирные кислоты, выделяемые липазами, по более сложному механизму. Жирные кислоты плохо растворимы в воде, хотя они более растворимы, чем триацилглицерины. Липиды любого вида имеют тенденцию образовывать капли. Белковые ферменты растворимы в воде и поэтому не могут получить легкий доступ к липидной капле.Для переваривания липиды должны быть эмульгированы в мелкие капли, которые имеют большую площадь поверхности. Другими словами, необходимо преодолеть гидрофобные взаимодействия, заставляющие липиды превращаться в более крупные капли. Молекулы, которые выполняют эту функцию, называются желчными солями или желчными кислотами . Метаболически печень создает их и выделяет в желчный пузырь, откуда они перекачиваются в двенадцатиперстную кишку.
Соли желчных кислот получают из холестерина и являются основным конечным продуктом метаболизма холестерина.Это мощные детергенты с большим гидрофобным компонентом и концевой группой карбоновой кислоты, которая имеет отрицательный заряд при pH, характерном для тонкой кишки. Гидрофобный компонент желчной кислоты будет связываться выше определенной концентрации (называемой критической концентрацией мицелл или CMC ) с образованием дискообразных мицелл , то есть капель. Общие желчные соли имеют КМЦ в диапазоне от 2 до 5 (миллимолярных). Мицеллы в кишечнике содержат пищевые липиды (триацилглицерин, холестерин и жирные кислоты), а также соли желчных кислот и по этой причине называются смешанными мицеллами .На рисунке представлена диаграмма смешанной мицеллы.
Рисунок 1
Соли желчных кислот образуют край мицеллы, а также в меньшем количестве оказываются рассредоточенными внутри мицеллы. Липиды существуют в бислое внутри диска. Желчные кислоты важны для абсорбции жирных кислот. Жирорастворимым витаминам (A, D, E и K) для усвоения абсолютно необходимы желчные кислоты.
Смешанная мицелла обеспечивает большую площадь поверхности для действия липазы поджелудочной железы , которая отвечает за большую часть пищеварительного действия.Липаза поджелудочной железы использует кофактор, небольшой белок под названием , колипаза , который связывается как с липазой, так и с поверхностью мицелл. Действие липазы приводит к появлению свободных жирных кислот, которые плохо растворяются в водной фазе кишечника. По большей части клетки тонкого кишечника поглощают эти свободные жирные кислоты; Бактерии в толстом кишечнике метаболизируют и / или поглощают те, которые проходят через тонкий кишечник. Соли желчных кислот реабсорбируются в последней трети тонкого кишечника.
Метаболизм желчных кислот объясняет способность определенных видов пищевых волокон снижать уровень холестерина в сыворотке крови. Молекула желчной кислоты циркулирует через печень и кишечник пять или более раз, прежде чем окончательно удаляется. Растворимая клетчатка (например, содержащаяся в овсяных отрубях) связывает желчные кислоты, но сама не усваивается. Таким образом, связанные с клетчаткой желчные кислоты выводятся со стулом. Поскольку желчные кислоты получают из холестерина, синтез большего количества желчной кислоты истощает запасы холестерина в организме, что приводит к снижению уровня холестерина в сыворотке и, следовательно, к снижению риска ишемической болезни сердца.Конечно, употребление овсяной клетчатки не может преодолеть чрезмерное потребление холестерина с пищей. Другими словами, было бы глупо потреблять чрезмерное количество хорошо мраморного стейка и надеяться на преодоление последствий, съев маффин с отрубями.
Липиды в кровотоке
Свободные жирные кислоты переносятся в виде комплексов с сывороточным альбумином. Холестерин, триацилглицерины и фосфолипиды транспортируются в виде белково-липидных комплексов, называемых липопротеинами . Липопротеины имеют сферическую форму с различным количеством и видами белков на поверхности.Белковые компоненты, которых существует не менее десяти, называются аполипопротеинами . Липопротеины классифицируются по плотности.
Самыми легкими и самыми крупными из аполипопротеинов являются хиломикронов , которые менее плотны, чем вода, поскольку состоят из более чем 95 процентов липидов по весу (помните, что масла плавают на воде, потому что они менее плотны, чем вода). Триацилглицерины составляют большую часть липидного компонента хиломикронов с небольшими количествами фосфолипидов и холестерина.Хиломикроны содержат несколько видов аполипопротеинов.
Липопротеины очень низкой плотности (ЛПОНП) менее плотны, чем хиломикроны. Они содержат больше белка, хотя липиды (жирные кислоты, холестерин и фосфолипиды в указанном порядке) по-прежнему составляют от 90 до 95 процентов их веса. Липопротеины низкой плотности (ЛПНП) состоят примерно на 85 процентов по массе и содержат больше холестерина, чем любой другой вид липидов. ЛПОНП и ЛПНП содержат большое количество аполипопротеина В. ЛПОНП и ЛПНП иногда называют «плохим холестерином», потому что повышенные концентрации этих липопротеинов в сыворотке соответствуют высокой частоте заболеваний артерий (инсульта и сердечных заболеваний).ЛПНП переносят холестерин и жирные кислоты к участкам синтеза клеточной мембраны.
Липопротеины высокой плотности (ЛПВП) содержат другую форму аполипопротеина, аполипопротеин А. Эти белки примерно наполовину состоят из липидов и наполовину из белков. Фосфолипиды и сложные эфиры холестерина являются наиболее важными липидными компонентами. HDL иногда называют «хорошим холестерином», потому что более высокое отношение HDL к LDL соответствует более низкому уровню ишемической болезни сердца.
Таким образом, триацилглицерины из рациона перевариваются липазой и связываются с солями желчных кислот в смешанные мицеллы.Свободные жирные кислоты абсорбируются клетками тонкой кишки, из которых они транспортируются по лимфатической системе в печень. Из печени они выделяются в кровоток в виде аполипопротеинов, разнося жирные кислоты и холестерин к клеткам по всему телу.
Триацилглицерины в хиломикронах и ЛПНП циркулируют по кровеносной системе; первые содержат пищевые липиды, а вторые — липиды, синтезируемые печенью. Триацилглицерины являются субстратами для клеточных липаз, которые в несколько этапов гидролизуют их до жирных кислот и глицерина.Белки-носители транспортируют липиды в клетку. Для липидов с разной длиной цепи существуют разные носители.
Переваривание липидов
Переваривание липидов
В этом отчете кратко описаны действия в желудочно-кишечном тракте при употреблении в пищу различных типов липидных комплексов; триацилглицерины, фосфолипиды и этиловые эфиры. Кроме того, что происходит во время мальабсорбции липидов, влияя на общее поглощение липидов и жирорастворимых витаминов и каротиноидов.Кроме того, этот отчет также включает в себя краткое изложение сегодняшних знаний об изучении абсорбции липидов in vivo и различных биомаркеров, которые, как предполагается, отражают потребление n-3 ПНЖК.
Липиды в продуктах питания
Липиды в пище находятся в нескольких типах различных липидных комплексов, наиболее распространенным из которых являются триацилглицерины (ТАГ), состоящие из одной молекулы глицерина и трех жирных кислот (ЖК) [1] (рис. 1). Эти липидные комплексы являются гидрофобными, что означает, что они не растворяются в воде, и это свойство влияет на их перенос через богатую водой среду в желудочно-кишечном тракте (ЖКТ).Исходя из этого, сложноэфирные связи TAG необходимо гидролизовать, что приведет к образованию свободных жирных кислот (FFA) и моноацилглицерина (MAG). СЖК и МАГ более гидрофильны, что облегчает их растворение в воде и, следовательно, увеличивает абсорбцию в тонком кишечнике. Из-за их гидрофобной природы большинство пищевых жиров существует в основном в виде эмульсий, в которых липидные капли стабилизируются в богатой водой среде за счет амфифильных липидов и белков [2]. Амфифильный означает, что молекула имеет водорастворимую группу, присоединенную к неполярной, водонерастворимой углеводородной цепи, заставляя их переходить в границу раздела между липидом и водой, растворяя липид.
FA имеет широкий диапазон различной длины цепи, степени ненасыщенности и различных изомеров FA. Обычно жирная кислота содержит 2-24 атома углерода (C) [3], с одной карбоксильной группой (COOH) на одном конце и метильной группой (Ch4) на другом конце, обычно называемой ω / n. Двойные связи также могут быть включены в цепь, дающую ненасыщенные ЖК; мононенасыщенные ЖК (МНЖК), если присутствует только одна двойная связь, и полиненасыщенные ЖК (ПНЖК), если присутствует ≥2 двойных связей [3].ПНЖК далее классифицируются как ПНЖК n-3, n-6, n-7 или n-9; в зависимости от положения первой двойной связи, считая от -Ch4 в жирной кислоте. Как длина углеродной цепи, так и наличие двойных связей будут влиять на характеристики FA. Внутри триацилглицерина (ТАГ) аналогичные FA могут быть размещены в разных положениях, обозначенных sn-1, -2 и -3 (рис. 1). Например, положение длинноцепочечных (LC) n-3 PUFA, эйкозапентаеновой кислоты (EPA) и докозагексаеновой кислоты (DHA) на TAG зависит от происхождения липида.EPA и DHA расположены в основном в sn1 и — 3 у морских млекопитающих, в то время как они обогащены в положении sn-2 в ТАГ, полученных из рыб [3].
Предыдущие исследования показали, что ПНЖК могут оказывать благотворное влияние на несколько метаболических факторов риска у людей [4, 5]. Предполагается, что положительные эффекты LC n-3 PUFA частично объясняются снижением уровня ТАГ в сыворотке и уменьшением воспаления [6, 7].
| Фиг. 1 показан в виде триацилглицерина (ТАГ), включающего глицериновую основу и три жирные кислоты (ЖК).FA прикреплены к определенным позициям TAG, сокращенно sn-1, -2 и -3. |
Переваривание и всасывание липидов человеком
Переваривание липидов очень эффективно. Примерно 95–98% липидов, содержащихся в пище, всасывается в тонком кишечнике [8, 9].Пищевые липидные комплексы необходимо расщепить на более мелкие части, которые будут поглощены энтероцитами, которые представляют собой клетки, выстилающие стенку кишечника (рис. 4). Большинство, но не все пищевые липиды содержат сложноэфирные связи, которые легко гидролизуются липазами, присутствующими в желудочно-кишечном тракте (ЖКТ). Липазы — это ферменты, которые отвечают за разрушение липидных комплексов, описанных выше, и в целом необходимы для переваривания липидов. Они поглощаются поверхностью капель, поэтому природа межфазного слоя будет определять скорость и степень гидролиза липидов [10].Кроме того, общее всасывание липидов является наибольшим в верхних отделах тонкой кишки из-за присутствия поверхностно-активных веществ [11], которые увеличивают количество смешанных мицелл. По мере того как происходит абсорбция поверхностно-активных веществ, например FFA и MAG, общий липолиз и абсорбция будут менее эффективными из-за уменьшения площади поверхности липидных капель [12].
Поскольку ТАГ являются основными липидными комплексами, присутствующими в пищевых продуктах, в основном существуют две липолитические ферментные системы, которые важны для эффективного переваривания липидов: желудочная (HGL) и панкреатическая (HPL) липазы [8, 13].Относительный вклад HGL и HPL в общий гидролиз липидов составляет приблизительно 10-30% и 70-90% соответственно (рис. 2). Однако в ЖКТ присутствуют и другие липазы; подобно панкреатической неспецифической липазе (панкреатическая карбоксилэстераза), панкреатической фосфолипазе A2 (sPLA2) [14] и белку-2, связанному с панкреатической липазой (PLRP2) [15]. Эти липазы отвечают за гидролиз других пищевых липидных комплексов, например фосфолипидов и галактолипидов [16]. Кроме того, существуют и другие липазы, которые находятся вне ЖКТ, например: печеночные (HL), липопротеиновые (LPL) и эндотелиальные (EL) липазы [17].Общая функция этих липаз, не относящихся к ЖКТ, заключается в высвобождении ЖК из липопротеинов, присутствующих в кровотоке, делая их доступными для всасывания.
|
. Фиг. 2 показывает относительный вклад липазы желудка человека (HGL) (10-30%) и липазы поджелудочной железы человека (HPL) (70-90%), в общее переваривание липидов. Цифра основана на N’Goma et al. (2012) [ 18 ] |
Пероральное переваривание липидов
Рот — это первая ступень приема пищи при попадании в ЖКТ.Механические силы измельчения зубов разрушают пищу на более мелкие кусочки. Кроме того, будет выделяться слюна, которая необходима для смазки пищевых частиц, создавая пищевой комок. Существование лингвальной липазы, возникающей во рту, ранее подвергалось сомнению. Однако установлено клеточное и тканевое происхождение предуоденальных липаз человека, что свидетельствует об отсутствии этого фермента у людей [19].
Переваривание липидов желудка
Расщепление диетических ТАГ начинается в желудке под действием желудочной липазы (HGL) [20], которая, как известно, стабильна и активна при кислом pH, с максимальной активностью при pH 5.0-5,4 [21]. Он гидролизует ЖК из всех трех положений ТАГ [22], но имеет специфичность для sn-3 [13, 23]. Исходя из этого, липолитическая активность HGL в основном дает одну свободную жирную кислоту (FFA) + один диацилглицерин (DAG) [9, 13, 24, 25], причем DAG представляет собой липидный комплекс, состоящий из одного глицеринового остова с двумя Присоединение FA происходит, когда липаза отсекает FA из одного из трех положений на глицериновой основе TAG (рис. 3). HGL ответственен за до 10-30% общего распада липидов в ЖКТ [13, 26-28], а ограниченная степень липолиза, как предполагается, связана с ингибированием липидными продуктами по обратной связи [9, 29].
|
На фиг. 3 показано распад триацилглицеринов (ТАГ) на диацилглицерин (ДАГ) и одну свободную жирную кислоту (СЖК), инициированный липазой желудка. |
Переваривание липидов в кишечнике
По мере того, как предварительно переваренная пища продвигается дальше в первую часть тонкой кишки, двенадцатиперстную кишку, она смешивается с ферментативными ферментами поджелудочной железы и желчью [30, 31].Основными поверхностно-активными веществами в желчи являются соли желчных кислот, которые необходимы для диспергирования гидрофобных липидных комплексов в богатой водой среде тонкого кишечника, способствуя высвобождению ЖК из ТАГ и ДАГ за счет образования внешнего слоя смешанных мицелл [9, 32 , 33]. Другие липиды желчи, такие как фосфолипиды и холестерин, также участвуют в образовании смешанных мицелл [9] (рис. 5). Кроме того, образование FFA и MAG в результате действия липаз в различных положениях TAG поможет увеличить скорость эмульгирования.Подводя итог, можно сказать, что эмульгирование липидной капли увеличивает площадь поверхности липидных капель, тем самым увеличивая липолитическое действие липаз [34].
Секреция ферментов поджелудочной железой стимулируется как присутствием пищи в желудке, гормонами, так и реакцией на сенсорные сигналы от мысли, вида или запаха пищи [35]. Среди ферментов, которые секретируются при этих стимулах, находится липаза поджелудочной железы (HPL) [30]. HPL — это главный фермент, ответственный за липолиз в ЖКТ человека, ответственный за гидролиз около 98% оставшихся диетических ТАГ у здоровых людей, способствуя общему всасыванию 95-98% общего содержания липидов из пищи [36].HPL отдает предпочтение FA, расположенной в положении TAG sn-1 и sn-3 [37, 38], что дает два FFA + sn-2 MAG [37, 39] (рис. 4). . HPL нуждается в коферменте, колипазе, в качестве медиатора [40, 41] для выполнения своей функции. Колипаза работает, прикрепляя HPL к своему субстрату [42]. В процессе пищеварения ЖК высвобождаются из ТАГов. FA с короткой и средней цепью (2-12 ° C), которая имеет более высокую растворимость в водной среде, увеличивает эмульгирование липидных капель за счет эффективной солюбилизации в смешанные мицеллы.В то время как длинноцепочечные ЖК (ЖК ЖК) (> 12C), которые являются более гидрофобными, будут накапливаться на межфазной границе масло-вода, в некоторой степени ингибируя ферментативное действие HPL [43]. Однако, как описано выше, переваривание и всасывание липидов чрезвычайно эффективно. Следовательно, это повлияет только на скорость липолитического действия, но не на общий липолиз.
|
Рисунок 4 показывает распад триацилглицеринов (TAG) на моноацилглицерин (MAG) и две свободные жирные кислоты (FFA), инициированный липазой поджелудочной железы |
Поглощение и распределение липидов
В тонком кишечнике мицеллы важны для переноса содержимого гидрофобного ядра, образованного, например, липидами с низкой растворимостью в воде; холестерин, МАГ и СЖК в энтероциты для абсорбции [14, 33, 44].Когда смешанные мицеллы достигают неперемешиваемого слоя, комплекс будет отключен из-за сдвига pH, что приведет к высвобождению как содержимого ядра, так и соединений, образующих внешний слой, в том числе солей желчных кислот. Механизм захвата и абсорбции FA неясен, но предполагается, что на него влияет длина цепи FA. ЖК, содержащие <12 ° C, могут быть связаны с альбумином, который является белком со сродством к ЖК [45], что делает их водорастворимыми. Следовательно, эти ЖК могут пассивно диффундировать через эпителиальные клетки, выстилающие просвет кишечника [46, 47], далее диффундируя в кровоток, где они транспортируются в печень через печеночную вену.ЖК ЖК (> 12 C), которые являются более гидрофобными, транспортируются через клеточную мембрану под действием транспортных белков [45, 48]. Внутри клетки они будут повторно синтезироваться в ТАГ внутри эндоплазматического ретикулума, прежде чем они будут доставлены в аппарат Гольджи, где они соединятся с холестерином, фосфолипидами и белками, образуя липопротеин, называемый хиломикрон (ХМ) [49]. Липопротеины являются транспортными средствами, ответственными за транспортировку различных количеств холестерина и ТАГ через богатую водой среду крови и лимфы от источника к месту назначения.Растворимость липопротеинов в богатой водой среде кровотока обусловлена покрытием из аполипопротеинов.
Эти специфические белки важны и как ферментные кофакторы, и как маркеры рецепторов. Маркеры помогают различным тканям и клеткам распознавать определенный тип липопротеинов, гарантируя, что их основное содержимое доставляется в нужное место. Как описано выше, CM ответственны за транспортировку липидов, полученных с пищей, к клеткам ткани или печени, в зависимости от потребности в FA.Поскольку ТАГ удаляются и абсорбируются тканью, CM теряет свой специфический аполипопротеин, образуя CM-остаток (CM R), который удаляется из кровотока печенью и далее катаболизируется [51-53]. Липиды, которые синтезируются в печени, упаковываются в липопротеины, называемые липопротеинами очень низкой плотности (ЛПОНП), и секретируются в периферическое кровообращение. Поскольку ТАГ удаляются из ЛПОНП под действием липаз в ткани, они восстанавливаются до липопротеинов промежуточной плотности (ЛПНП) и далее до липопротеинов низкой плотности (ЛПНП).ЛПНП содержит небольшое количество ТАГ, что увеличивает долю холестерина. Следовательно, основная функция ЛПНП — перенос холестерина в периферические ткани и печень. Липопротеин высокой плотности (ЛПВП) — это липопротеин, который отвечает за «обратный транспорт липидов», переносящий избыточный холестерин из ткани обратно в печень и стероидогенные ткани для деградации и катаболизации. Стериодогенные ткани — это ткани, которые вырабатывают стероиды в организме человека.Холестерин, среди прочего, используется для синтеза желчных кислот [51-53], важных для эффективного переваривания липидов, как описано ранее.
Этот раздел; Поглощение и распределение липидов показано на рисунке 5.
|
Рисунок 5 Обзор липидного переваривания и распределения липидов, подробности описаны в тексте в главе; 2.4 Поглощение и распределение липидов. ApoX, аполипопротеин; BS, желчная соль; CE, сложный эфир холестерина; Хл, холестерин; CM, хиломикрон; CM r — остаток хиломикрона; ДАГ, диацилглицерин; EL, эндотелиальная липаза; FFA, свободная жирная кислота; ЛПВП, липопротеины высокой плотности; HL, печеночная липаза; IDL, липопротеин промежуточной плотности; ЛПНП, липопротеины низкой плотности; LPL, липопротеинлипаза; МАГ, моноацилглицерин; ТАГ, триацилглицерин; ЛПОНП, липопротеины очень низкой плотности. Рисунок взят из Aarak, K. E (2013) [ 50 ]. |
Абсорбция n-3 ПНЖК из этиловых эфиров и триацилглицеринов
Было показано, что две n-3 ПНЖК EPA и DHA имеют несколько положительных последствий для здоровья, как описано ранее. Однако «натуральные» пищевые продукты содержат эти ЖК в относительно низком количестве. Для увеличения количества потребляемых n-3 ПНЖК были предложены концентрации этих специфических ЖК. Для этого обычно используется получение этиловых эфиров (ЭЭ) путем переэтерификации ЖК с удалением глицериновой основы ТАГ с введением вместо этого этанола [54].
Расщепление ТАГ липазой поджелудочной железы (HPL) подробно описано выше. Переваривание EE чем-то отличается от переваривания TAG из-за отсутствия глицеринового остова. Подводить итоги; EE также зависят от ферментативной активности HPL по высвобождению ЖК, поскольку для абсорбции ЖК должен присутствовать в виде свободных жирных кислот или моноацилглицерина. Однако связь между FA и этанолом более устойчива к гидролизу, что делает общее высвобождение FA из EE менее эффективным по сравнению с высвобождением FA из TAG [55-57].Биодоступность n-3 ПНЖК из EE и TAG изучалась многочисленными исследованиями. Несколько исследований показали аналогичные результаты при сравнении поглощения ТАГ и ЭЭ [58, 59]. Однако в целом проведенные исследования показывают, что n-3 ПНЖК в ТАГ имеют повышенную биодоступность по сравнению с тем, когда они присутствуют в ЭЭ [60-64]. Однако при переваривании пищи выход ферментов является избыточным, следовательно, увеличение потребления не происходит. ЭЭ не влияют ни на эффективность, ни на гидролиз ТАГ.
Расщепление фосфолипидов
В нормальном рационе фосфолипиды составляют примерно 1-10% суточного потребления жиров [65].Большинство этих фосфолипидов представляют собой фосфатидилхолин, который также является вторым по распространенности диетическим липидом после триацилглицеринов [66]. Однако в пищевых липидах присутствуют и другие фосфолипиды; например фосфатидилэтаноламин, фосфатидилсерин и фосфатидилинозитол. Фосфолипаза А2, которая представляет собой фермент, присутствующий в просвете кишечника, ответственный за высвобождение ЖК из фосфолипидов, имеет предпочтение в отношении sn-2 фосфолипидов, и ее липолитическое действие приводит к образованию свободных жирных кислот + лизо-ПК.Эти компоненты абсорбируются в виде компонентов из ТАГ и повторно синтезируются в фосфолипиды в энтероцитах, прежде чем они высвобождаются как части хиломикронов [65, 67].
Нарушение всасывания липидов
Биодоступность — это термин, обычно используемый при исследовании абсорбции питательных веществ, определяемый как доля проглоченных компонентов, которые доступны для использования в нормальных физиологических функциях, например. грамм. доступны в кровотоке [68]. Как описано ранее, переваривание и поглощение липидов очень эффективно, однако некоторые нарушения функций ЖКТ могут влиять на эффективность поглощения, вызывая вторичную реакцию, называемую мальабсорбцией.Мальабсорбция определяется как патологическое нарушение нормальной физиологической последовательности пищеварения, всасывания и транспорта питательных веществ и электролитов [69]. Это может быть вызвано несколькими различными дисфункциями в желудочно-кишечном тракте. Например; кишечные причины, такие как недостаточность поджелудочной железы, означающая нарушение выработки пищеварительных компонентов (например, ферментов), воспалительное заболевание кишечника и резекция кишечника; дисфункция слизистой оболочки, такая как глютеновая болезнь и тропический спру; лимфатическая дисфункция, такая как лимфагеэктазия, болезнь Уиппла и филяриатоз; или через другие физические изменения в желудочно-кишечном тракте, такие как лекарство, увеличивающее секрецию желчной кислоты или частичный откуп подвздошной кишки [70].Когда происходит мальабсорбция, это обычно приводит к общему дефициту макро- и микронутриентов, что приводит к классическим симптомам мальабсорбции, описанным ниже. Мальабсорбцию можно разделить на три основные группы в зависимости от степени мальабсорбции; (1) селективный, если мальабсорбция затрагивает только один конкретный микроэлемент; например непереносимость лактозы; (2) частичное, когда мальабсорбция влияет на группу макронутриентов, например, α-β-липопротеинемия у младенцев, которая не абсорбирует липиды и жирорастворимые витамины, как обычно, и (3) общая, когда функция всего тонкого кишечника ослабленный, e.г при глютеновых заболеваниях. Симптомы мальабсорбции питательных веществ также подразделяются на две разные категории: кишечные, которые обычно являются наиболее доминирующими, и внекишечные. Симптомы со стороны кишечника: Хроническая диарея, водянистый, дневной и ночной объемный стул; Изменение цвета стула, вызванное содержанием жира, в результате чего стул становится бледно-желтым, плавающим и губчатым. Наблюдения должны быть подтверждены адекватным исследованием фекалий, а содержание жира на декали не должно превышать 7 г / день, независимо от общего количества потребляемых жиров; Гиперфагия; Тошнота; Рвота; Вздутие живота; Чрезмерные газы и дискомфорт в животе, но не боль.Спазмы предполагают наличие закупоренных сегментов кишечника, наблюдаемых при таких заболеваниях, как болезнь Хрона и злокачественные новообразования. Могут быть внекишечные симптомы; невысокий рост; бесплодие, болезни костей и гематологические проблемы [71].
Нарушение всасывания липидов может привести к дефициту жирорастворимого витамина (A, D, E и K). Кроме того, мальабсорбция липидов также влияет на абсорбцию эссенциальной ЖК (линолевой кислоты) у пациентов, перенесших резекцию кишечника [72].Как было сказано выше, нарушение всасывания влияет на всасывание питательных веществ в целом. Тем не менее, ранее также сообщалось о мальабсорбции однократных. К их числу относятся желчные кислоты, которые, как известно, необходимы для абсорбции липидов и вызывают диарею при концентрации> 3 ммоль / л в толстой кишке [73]. Нарушение всасывания также может быть вызвано терапевтическими средствами, например, при снижении уровня липидов в сыворотке крови у пациентов с гиперлипидемией за счет применения фармацевтического неомизина или холестирамина. Это связано с общим снижением всасывания липидов из тонкого кишечника.Эффект был бы более сильным у субъектов, которые ранее проходили обход подвздошной кишки, из-за снижения всасывания липидов [70].
Измерение потребления n-3 ПНЖК с пищей
Отсутствуют общепринятые биомаркеры, которые отражают повышение статуса n-3 ПНЖК в ответ на повышенное потребление с пищей. Это ранее подчеркивалось как проблема при планировании и проведении клинических испытаний, изучающих эффект добавки n-3 ПНЖК in vivo .Как резюмирует Fekete et. al (2009) будет ли определенный биомаркер иметь важное значение для определения того, является ли отрицательный результат контролируемого исследования, например. грамм. отсутствие функциональных изменений в ответ на добавление связано либо с клиническим эффектом, либо с несоблюдением пациентом режима лечения, либо с неспособностью диетического вмешательства вызвать изменения в составе ЖК соответствующих биологических компартментов в организме. Ранее было предложено несколько компартментов, например, разные липиды плазмы (ТАГ, эфиры холестерина, фосфолипиды и общие липиды плазмы), эритроциты и жировая ткань [74].Однако ранее было показано, что кривая доза-ответ включения в эти компартменты различается [75, 76], что позволяет предположить, что выбор измерения также может повлиять на результат исследования. Более того, это наблюдение, полученное при изучении различных компартментов, было бы трудно сравнивать друг с другом. Обзор Øverby et. Al (2009) также предложил выбирать компартмент для анализа в зависимости от цели и продолжительности исследования [77]. Например, использование жировой ткани при оценке долгосрочного потребления ЖК [78, 79], эритроцитов при изучении включения n-3 ЖК <120 дней [80] и липидов плазмы при изучении потребления с пищей в течение более короткого промежутка времени [ 81].Тем не менее, липиды плазмы также были предложены для предоставления информации в течение более длительного периода времени, если субъекты придерживаются стабильного режима питания [82].
Отчет, написанный на основе доктора философии Кристи Экранн Аарак, озаглавленный «Высвобождение жирных кислот из жира и мышц лосося во время пищеварения in vitro — влияние состава пищи» (ISBN 978-82-575-1165-4)
Список литературы
- Mu, H. and T. Porsgaard, Метаболизм структурированных триацилглицеринов. Prog Lipid Res, 2005. 44 (6): стр. 430-48.
- Borgström, B., Расщепление жиров в просвете . 2-е изд. Поджелудочная железа: биология, патбиология и болезни, под ред. э.а. Вай Лян В. Го. 1993, Нью-Йорк: Raven Press, Ltd.
- Ackman, R.G., Некоторые возможные воздействия на биохимию липидов различий в распределении по глицерину длинноцепочечных жирных кислот n-3 в жирах морской рыбы и морских млекопитающих. Atherosclerosis, 1988. 70 (1-2): p.171-3.
- Wang, C., et al., n-3 Жирные кислоты из рыбы или рыбьего жира, но не альфа-линоленовая кислота, улучшают исходы сердечно-сосудистых заболеваний в исследованиях первичной и вторичной профилактики: систематический обзор. Am J Clin Nutr, 2006. 84 (1): стр. 5-17.
- Bjerve, K.S., et al., добавление альфа-линоленовой кислоты и длинноцепочечных омега-3 жирных кислот у трех пациентов с дефицитом омега-3 жирных кислот: влияние на функцию лимфоцитов, липиды плазмы и эритроцитов, а также образование простаноидов. Am J Clin Nutr, 1989. 49 (2): стр. 290-300.
- Hu, F.B., et al., Потребление рыбы и длинноцепочечных омега-3 жирных кислот и риск ишемической болезни сердца и общая смертность среди женщин с диабетом. Тираж, 2003. 107 (14): с. 5.
- Calder, P.C., n-3 полиненасыщенные жирные кислоты, воспаления и воспалительные заболевания. Am J Clin Nutr, 2006. 83 (6 приложений): стр. 1505С-1519С.
- Armand, M., Липазы и липолиз в пищеварительном тракте человека: где мы находимся? Curr Opin Clin Nutr Metab Care, 2007. 10 (2): п. 156-64.
- Кэри, М.С., Д.М. Смолл и К. Bliss, Переваривание и всасывание липидов. Annu Rev Physiol, 1983. 45 : p. 651-77.
- Филлери-Трэвис, А.Дж., Л.Х. Фостер и М.М. Робинс, Устойчивость эмульсий, стабилизированных двумя физиологическими поверхностно-активными веществами: L-альфа-фосфатидилхолином и таурохолатом натрия. Biophys Chem, 1995. 54 (3): p. 253-60.
- Mun, S., E.A. Декер, Д.Дж.McClements, Влияние типа эмульгатора на усвояемость липидных капель липазой поджелудочной железы in vitro. Food Research International, 2007. 40 (6): p. 770-781.
- Westergaard, H. and J.M. Dietschy, Механизм, посредством которого мицеллы желчных кислот увеличивают скорость поглощения жирных кислот и холестерина клетками слизистой оболочки кишечника. J Clin Invest, 1976. 58 (1): p. 97-108.
- Carriere, F., et al., Секреция и вклад в липолиз липаз желудка и поджелудочной железы во время пробного приема пищи у людей. Гастроэнтерология, 1993. 105 (3): с. 876-88.
- Эмблтон, Дж. К. и C.W. Pouton, Структура и функция желудочно-кишечных липаз. Advanced Drug Delivery Reviews, 1997. 25 : p. 17.
- Eydoux, C., et al., Дополнительная биохимическая характеристика белка 2, связанного с липазой поджелудочной железы человека, экспрессированного в дрожжевых клетках. J Lipid Res, 2007. 48 (7): p. 1539-49.
- Amara, S., et al., Липолиз естественных длинноцепочечных и синтетических среднецепочечных галактолипидов с помощью белка, связанного с липазой поджелудочной железы 2. Biochim Biophys Acta, 2010. 1801 (4): p. 508-16.
- Бирари, Р. Б. и К. К. Bhutani, Ингибиторы липазы поджелудочной железы из природных источников: неизученный потенциал. Drug Discovery Today, 2007. 12 (19-20): p. 879-89.
- N’Goma, J.-C.B., et al., Понимание процессов переваривания липидов в желудочно-кишечном тракте до разработки систем доставки лекарств на основе липидов. Терапевтическая доставка, 2012. 3 (1): с. 19.
- Моро, Х., et al., Скрининг предуоденальных липаз у нескольких млекопитающих. Biochim Biophys Acta, 1988. 959 (3): p. 247-52.
- Хамош, М., Лингвальные и желудочные липазы. Nutrition, 1990. 6 (6): p. 421-8.
- Gargouri, Y., et al., Кинетический анализ желудочной липазы человека на эмульсиях триацилглицерина с короткой и длинной цепью. Гастроэнтерология, 1986. 91 (4): с. 919-25.
- Carriere, F., et al., Очистка и биохимическая характеристика липазы желудка собак. Eur J Biochem, 1991. 202 (1): p. 75-83.
- Carriere, F., et al., Желудочные липазы: клеточные, биохимические и кинетические аспекты , в Липазы: их структура, биохимия и применение , П. Вулли, редактор. 1994, Издательство Кембриджского университета: Нью-Йорк. п. 181-205.
- Patton, J.S., et al., Гидролиз триацилглицериновых эмульсий лингвальной липазой.Микроскопическое исследование. Biochim Biophys Acta, 1982. 712 (2): p. 400-7.
- Hayes, R.J., et al., Обзор переваривания, абсорбции и метаболизма триацилглицерина в отношении триацилглицеринов Salatrim. J. Agric. Food Chem, 1994. 42 : p. 474-483.
- Armand, M., et al., Характеристика эмульсий и липолиза пищевых липидов в желудке человека. Am J Physiol, 1994. 266 (3 Pt 1): p. Г372-81.
- Armand, M., et al., Физико-химические характеристики эмульсий при переваривании жиров в желудке и двенадцатиперстной кишке человека. Am J Physiol, 1996. 271 (1 Pt 1): p. Г172-83.
- Armand, M., et al., Переваривание и абсорбция 2 жировых эмульсий с каплями разных размеров в пищеварительном тракте человека. Emerican Journal of Clinical Nutrition, 1999. 70 (6): p. 1096-106.
- Хамош М., Д. Ганот и П. Хамош, Липаза языка крысы.Характеристики ферментативной активности. J Biol Chem, 1979. 254 (23): p. 12121-5.
- Miled, N., et al., Пищеварительные липазы: от трехмерной структуры к физиологии. Biochimie, 2000. 82 (11): p. 973-86.
- Borovicka, J., et al., Регулирование секреции липазы желудка и поджелудочной железы с помощью CCK и холинергических механизмов у людей. Am J Physiol, 1997. 273 (2 Pt 1): p. G374-80.
- Рейс, П., et al., Липазы на границах раздела: обзор. Adv Colloid Interface Sci, 2009. 147-148 : p. 237-50.
- Хернелл, О., Дж. Э. Стаггерс и М.С. Кэри, Физико-химическое поведение пищевых и желчных липидов во время пищеварения и всасывания в кишечнике. 2. Фазовый анализ и агрегационные состояния люминальных липидов при переваривании двенадцатиперстной кишки у здоровых взрослых людей. Biochemistry, 1990. 29 (8): p. 2041-56.
- Гаргури, Ю., et al., Важность липазы желудка человека для липолиза кишечника: исследование in vitro. Biochim Biophys Acta, 1986. 879 (3): p. 419-23.
- Келлер, Дж. И П. Лайер, Экзокринная реакция поджелудочной железы человека на питательные вещества при здоровье и болезни. Gut, 2005. 54 Suppl 6 : p. vi1-28.
- Porsgaard, T., et al., Различия во внутримолекулярной структуре структурированных масел не влияют на активность липазы поджелудочной железы in vitro или на всасывание (n-3) жирных кислот крысами. Journal of Nutrition, 2005. 135 (7): p. 1705-11.
- Маттсон, Ф.Х. и Р.А. Volpenhein, Переваривание и всасывание триглицеридов. J Biol Chem, 1964. 239 : стр. 2772-7.
- Э. Рогальска, С. Ранзак и Р. Вергер, Стереоселективность липаз. II. Стереоселективный гидролиз триглицеридов липазами желудка и поджелудочной железы. Journal of Biological Chemistry, 1990. 265 (33): p. 20271-6.
- Маттсон, Ф.H., et al., Промежуточные продукты, образующиеся при расщеплении триглицеридов. J Nutr, 1952. 48 (3): стр. 335-44.
- Borgstrom, B. and C. Erlanson, Ко-липаза панкреатического сока: физиологическое значение. Biochim Biophys Acta, 1971. 242 (2): p. 509-13.
- Морган, Р. и Н.Э. Hoffman, Взаимодействие липазы, кофактора липазы и солей желчных кислот при гидролизе триглицеридов. Biochim Biophys Acta, 1971. 248 (1): p.143-8.
- Freie, A.B., et al., Val-407 и Ile-408 в бета5′-петле липазы поджелудочной железы опосредуют взаимодействия липаза-колипаза в присутствии мицелл желчных солей. J Biol Chem, 2006. 281 (12): p. 7793-800.
- McClements, D.J., et al., Разработка пищевой структуры для контроля стабильности, переваривания, высвобождения и абсорбции липофильных компонентов пищи Food Biophysics, 2008. 3 : p. 219-228.
- Каспары, W.Ф., Физиология и патофизиология кишечной абсорбции. Am J Clin Nutr, 1992. 55 (1 приложение): стр. 299С-308С.
- Stremmel, W., et al., Новая концепция клеточного поглощения и внутриклеточного переноса длинноцепочечных жирных кислот. Lipids, 2001. 36 (9): p. 981-9.
- Artursson, P., Эпителиальный транспорт лекарств в культуре клеток. I. Модель для изучения пассивной диффузии лекарств через абсорбирующие кишечные (Caco-2) клетки. J Pharm Sci, 1990. 79 (6): p. 476-82.
- Гамильтон, Дж. А. и F. Kamp, Как свободные жирные кислоты транспортируются в мембранах? За счет белков или за счет свободной диффузии через липиды? Diabetes, 1999. 48 (12): p. 2255-69.
- Fitscher, B.A., et al., Опосредованные белком процессы поглощения жирных кислот, билирубина и других амфипатических соединений. Proc Soc Exp Biol Med, 1996. 212 (1): p. 15-23.
- Smith, W.L. и R.C. Murphy, Эйкозаноиды: пути циклооксигеназы, липоксигеназы и эпоксигеназы , в Biochemistry of Lipids, Lipopoteins and Membranes, 5th edition , D.E. Вэнс и Дж. Э. Вэнс, редакторы. 2008 г., Elsevier: Оксфорд, Великобритания. п. 30.
- Aarak, K.E., Высвобождение жирных кислот из жира и мышц лосося во время пищеварения in vitro — влияние состава корма , в Институт химии, биотехнологии и пищевых наук .2013 г., Университет естественных наук: Ос, Норвегия.
- Vance, J.E. and K. Adeli, Сборка и секреция триацилглицерин-богатых липопротеинов , в Biochemsitry of Lipids, Lipoproteins and Membranes, 5th edition , D.E. Вэнс и Дж. Э. Вэнс, редакторы. 2008 г., Elsevier: Оксфорд, Великобритания. п. 26.
- Филдинг, С.Дж. и П.Е. Филдинг, Динамика транспорта липопротеинов в системе кровообращения , в Биохимия липидов, липопротеинов и мембран, 5-е издание , D.Э. Вэнс и Дж. Э. Вэнс, редакторы. 2008 г., Elsevier: Оксфорд, Великобритания. п. 22.
- Schneider, W.J., Липопротеиновые рецепторы , в Biochemistry og Lipids, Lipoproteins and Membranes, 5th edition , D.E. Вэнс и Дж. Э. Вэнс, редакторы. 2008 г., Elsevier: Оксфорд, Великобритания. п. 24.
- Mogelson, S., S.J. Пайпер, Л. Lange, Термодинамические основы для синтазы этилового эфира жирных кислот, катализируемой этерификацией свободной жирной кислоты этанолом и накоплением этиловых эфиров жирных кислот. Biochemistry, 1984. 23 (18): p. 4082-7.
- Янг, Л.Ю., А. Куксис, Дж. Дж. Myher, Липолиз триацилглицеринов менхаденового масла и соответствующих алкиловых эфиров жирных кислот липазой поджелудочной железы in vitro: повторное исследование. J Lipid Res, 1990. 31 (1): p. 137-47.
- Янг, Л.Ю., А. Куксис, Дж. Дж. Myher, Всасывание в кишечнике масел менхадена и рапса и их метиловых и этиловых эфиров жирных кислот у крыс. Biochem Cell Biol, 1990. 68 (2): п. 480-91.
- Dyerberg, J., et al., Биодоступность составов морских n-3 жирных кислот. Prostaglandins Leukot Essent Fatty Acids, 2010. 83 (3): p. 137-41.
- von Schacky, C. and P.C. Weber, Метаболизм и влияние на функцию тромбоцитов очищенной эйкозапентаеновой и докозагексаеновой кислот у человека. J Clin Invest, 1985. 76 (6): p. 2446-50.
- Terano, T., et al., Влияние перорального введения высокоочищенной эйкозапентаеновой кислоты на функцию тромбоцитов, вязкость крови и деформируемость эритроцитов у здоровых людей. Атеросклероз, 1983. 46 (3): с. 321-31.
- Лоусон, Л. и Б. Hughes, Поглощение человеком жирных кислот рыбьего жира в виде триацилглицеринов, свободных кислот или этиловых эфиров. Biochem Biophys Res Commun, 1988. 152 (1): p. 328-35.
- Visioli, F., et al., . Потребление рыбы с пищей по сравнению с препаратами приводит к более высоким концентрациям n-3 жирных кислот в плазме. Lipids, 2003. 38 (4): p. 415-8.
- Икеда, И., et al., Переваривание и лимфатический транспорт эйкозапентаеновой и докозагексаеновой кислот, вводимых крысам в форме триацилглицерина, свободной кислоты и этилового эфира. Biochim Biophys Acta, 1995. 1259 (3): p. 297-304.
- Valenzuela, A., et al., Влияние добавок с этиловым эфиром докозагексаеновой кислоты и sn-2 докозагексаенилмоноацилглицеридом на жирные кислоты плазмы и эритроцитов у крыс. Ann Nutr Metab, 2005. 49 (1): стр. 49-53.
- el Boustani, S., et al., Энтеральное всасывание у человека эйкозапентаеновой кислоты в различных химических формах. Lipids, 1987. 22 (10): p. 711-4.
- Cohn, J.S., et al., Диетические фосфолипиды и абсорбция холестерина в кишечнике. Nutrients, 2010. 2 (2): с. 116-27.
- Phan, C.T. and P. Tso, Абсорбция и транспорт липидов в кишечнике. Front Biosci, 2001. 6 : стр. D299-319.
- Мансбах, К.М., 2-й и Ф. Горелик, Развитие и физиологическая регуляция всасывания липидов в кишечнике. II. Всасывание липидов с пищей, комплексный синтез липидов, а также внутриклеточная упаковка и секреция хиломикронов. Am J Physiol Gastrointest Liver Physiol, 2007. 293 (4): стр. G645-50.
- Guerra, A., et al., Актуальность и проблемы моделирования желудочного и тонкого кишечного пищеварения человека. Trends Biotechnol, 2012. 30 (11): с. 591-600.
- Bai, J.C., Синдромы мальабсорбции. Пищеварение, 1998. 59 (5): стр. 530-46.
- Thompson, G.R., Последствия кишечной мальабсорбции, связанные с липидами. Гут, 1989. 30 ТУ № : с. 29-34.
- Corazza, G., et al., Иммунная реактивность глиадина связана с явной и латентной энтеропатией у родственников больных глютеновой болезнью. Гастроэнтерология, 1992. 103 (5): с. 1517-22.
- Пресс, М., et al., Диагностика и лечение дефицита незаменимых жирных кислот у человека. Br Med J, 1974. 2 (5913): p. 247-50.
- Fromm, H. and M. Malavolti, Диарея, вызванная желчными кислотами. Clin Gastroenterol, 1986. 15 (3): p. 567-82.
- Fekete, K., et al., Методы оценки статуса длинноцепочечных n-3 полиненасыщенных жирных кислот у людей: систематический обзор. Am J Clin Nutr, 2009. 89 (6): стр. 2070С-2084С.
- Brown, A.J., E. Pang, D.C. Roberts, Устойчивые изменения в составе жирных кислот мембран эритроцитов после умеренного потребления n-3 полиненасыщенных жирных кислот: последствия для дизайна исследования. Am J Clin Nutr, 1991. 54 (4): стр. 668-73.
- Tremoli, E., et al., Длительное ингибирование агрегации тромбоцитов после приема этилового эфира жирной кислоты n-3 здоровыми добровольцами. Am J Clin Nutr, 1995. 61 (3): стр. 607-13.
- Оверби, Северная Каролина, Л. Серра-Маджем и Л.Ф. Андерсен, Методы диетической оценки потребления n-3 жирных кислот: систематический обзор. Br J Nutr, 2009. 102 Suppl 1 : p. С56-63.
- Knutsen, S.F., et al., Сравнение жирных кислот жировой ткани с диетическими жирными кислотами по результатам 24-часового опроса и опроса частоты приема пищи в Black and White Adventists: the Adventist Health Study. Ann Epidemiol, 2003. 13 (2): p.119-27.
- Arab, L., Биомаркеры потребления жиров и жирных кислот. J Nutr, 2003. 133 Приложение 3 : стр. 925S-932S.
- Салливан, Б.Л., П.Г. Уильямс и Б.Дж.Мейер, Подтверждение биомаркеров опросника частоты приема пищи длинноцепочечных полиненасыщенных жирных кислот омега-3. Lipids, 2006. 41 (9): p. 845-50.
- Hodge, A.M., et al., Состав жирных кислот фосфолипидов в плазме как биомаркер привычного потребления жиров с пищей в этнически разнообразной когорте. Nutr Metab Cardiovasc Dis, 2007. 17 (6): с. 415-26.
- Ottestad, I., et al., Окисленный рыбий жир не влияет на установленные маркеры окислительного стресса у здоровых людей: рандомизированное контролируемое исследование. Br J Nutr, 2012. 108 (2): с. 315-26.
Поглощение липидов
Поглощение липидов
Основная масса пищевых липидов — это нейтральный жир или триглицерид, состоящий из глицериновой основы, каждый углерод которой связан с жирной кислотой.Пищевые продукты обычно также содержат фосфолипиды, стерины, такие как холестерин, и многие второстепенные липиды, включая жирорастворимые витамины. Наконец, содержимое тонкого кишечника содержит липиды из отшелушенных эпителиальных клеток и значительный холестерин, поступающий с желчью.
Для абсорбции триглицерида должны происходить два процесса:
- Крупные агрегаты пищевых триглицеридов, которые практически нерастворимы в водной среде, необходимо физически расщеплять и удерживать во взвешенном состоянии — процесс, называемый эмульгированием.
- Молекулы триглицеридов должны ферментативно перевариваться с образованием моноглицеридов и жирных кислот, которые могут эффективно диффундировать или транспортироваться в энтероцит
Ключевыми участниками этих двух превращений являются желчные кислоты и липаза поджелудочной железы , обе из которых смешаны с химусом и действуют в просвете тонкой кишки. Желчные кислоты также необходимы для растворения других липидов, включая холестерин.
Эмульгирование, гидролиз и образование мицелл
|
Желчные кислоты играют свою первую важную роль в ассимиляции липидов, способствуя эмульгированию.Как производные холестерина желчные кислоты имеют как гидрофильные, так и гидрофобные домены (т.е. они являются амфипатическими). При воздействии большого агрегата триглицерида гидрофобные части желчных кислот интеркалируются в липид, а гидрофильные домены остаются на поверхности. Такое покрытие желчными кислотами способствует разрушению крупных агрегатов или капель на более мелкие и мелкие капли. |
|
|
Гидролиз триглицерида до моноглицерида и свободных жирных кислот осуществляется преимущественно липазой поджелудочной железы.Активность этого фермента заключается в урезании жирных кислот в положениях 1 и 3 триглицерида, в результате чего остаются две свободные жирные кислоты и 2-моноглицерид. Лекарство орлистат (ксеникал), которое продвигается для лечения ожирения, действует путем ингибирования липазы поджелудочной железы, тем самым уменьшая переваривание и всасывание жира в тонком кишечнике. Липаза — это водорастворимый фермент, и, проявив немного воображения, легко понять, почему эмульгирование является необходимой прелюдией к его эффективному действию.Вскоре после еды липаза присутствует в тонком кишечнике в довольно больших количествах, но может действовать только на поверхности капель триглиеридов. Для данного объема липида, чем меньше размер капель, тем больше площадь поверхности, а это означает, что большее количество молекул липазы может работать. |
|
|
Поскольку моноглицериды и жирные кислоты высвобождаются под действием липазы, они сохраняют свою связь с желчными кислотами и образуют комплекс с другими липидами с образованием структур, называемых мицеллами .Мицеллы представляют собой небольшие агрегаты (4-8 нм в диаметре) смешанных липидов и желчных кислот, взвешенных в пищеварительном тракте. При перемешивании пищи мицеллы сталкиваются с щеточной каймой энтероцитов тонкого кишечника, и липиды, включая моноглицериды и жирные кислоты, захватываются эпителиальными клетками. |
Поглощение и перенос в кровь
Основные продукты переваривания липидов — жирные кислоты и 2-моноглицериды — проникают в энтероцит путем простой диффузии через плазматическую мембрану.Значительная часть жирных кислот также попадает в энтероцит через специфический белок-переносчик жирных кислот в мембране.
Липиды транспортируются из энтероцитов в кровь по механизму, явно отличному от того, который мы наблюдали для моносахаридов и аминокислот.
Попав внутрь энтероцита, жирные кислоты и моноглицериды транспортируются в эндоплазматический ретикулум, где они используются для синтеза триглиеридов. Начиная с эндоплазматического ретикулума и заканчивая Гольджи, триглицерид упаковывается с холестерином, липопротеинами и другими липидами в частицы, называемые хиломикрон . Вспомните, где это происходит — в абсорбирующем энтероците тонкой кишки.
Хиломикроны вытесняются из Гольджи в экзоцитотические пузырьки, которые транспортируются в базолатеральную часть энтероцита. Везикулы сливаются с плазматической мембраной и подвергаются экзоцитозу, сбрасывая хиломикроны в пространство за пределами клеток.
Поскольку хиломикроны являются частицами, практически все шаги на этом пути можно визуализировать с помощью электронного микроскопа, как демонстрирует монтаж изображений ниже.
Транспортировка липидов в кровоток также отличается от того, что происходит с сахарами и аминокислотами. Вместо того, чтобы абсорбироваться непосредственно в капиллярную кровь, хиломикроны сначала транспортируются в лимфатический сосуд, который проникает в каждую ворсинку, называемую центральным молочным . До недавнего времени было непонятно, как большие хиломикроны попадают в млечные железы. Оказывается, есть участки молочной железы, в которых эндотелиальные клетки удерживаются вместе с помощью специализированных «кнопочных соединений», которые намного более проницаемы для хиломикронов, чем нормальные клеточные соединения.Лимфа, богатая хиломикронами, затем стекает в лимфатическую систему, которая быстро поступает в кровь. Хиломикроны, передающиеся с кровью, быстро разбираются, и составляющие их липиды используются по всему телу.
Когда абсорбируется большое количество хиломикронов, лимфа, оттекающая из тонкой кишки, кажется молочной, а лимфатические сосуды хорошо видны. На изображении ниже брюшного содержимого койота тонкие белые линии (стрелки) представляют собой лимфатические сосуды кишечника, заполненные хиломикронами.Эта лимфа проходит через брыжеечные лимфатические узлы (ЛУ), а затем в более крупные лимфатические узлы.
Другой важный липид, который всасывается в тонком кишечнике, — это холестерин. Гомеостатический холестерин является результатом баланса синтеза холестерина, абсорбции пищевого холестерина и выведения холестерина с желчью. Много лет назад было показано, что холестерин, но не растительные стерины, легко всасывается в кишечнике. Совсем недавно был идентифицирован специфический транспортный белок (NPC1L1), который переносит холестерин из просвета кишечника в энтероцит.Оттуда большая часть холестерина этерифицируется, включается в хиломикроны и перемещается в кровь с помощью механизмов, описанных выше.
Если вы хотите подтвердить для себя хотя бы некоторые из описанных выше процессов, вам следует провести следующий эксперимент:
- Съешьте чашку жирных сливок или мешок картофеля фри быстрого приготовления.
- Сделайте что-нибудь продуктивное, например, учебу в течение 30 минут.
- Возьмите образец крови у себя (достаточно капиллярной трубки) — используйте антикоагулянт, чтобы предотвратить свертывание.
- Центрифугируйте образец крови для разделения клеток и плазмы.
Когда вы исследуете свою плазму, она будет выглядеть отчетливо молочной из-за присутствия миллиардов светоотражающих хиломикронов (состояние называется липемия ). Если вам нужен дополнительный балл, продолжайте забор крови каждые 15 минут, пока плазма не очистится, а затем нанесите результаты на миллиметровую бумагу. В качестве альтернативы вы можете просто изучить изображение справа, чтобы увидеть, как выглядит сыворотка собаки после нескольких часов голодания по сравнению с липемической сывороткой, полученной вскоре после приема пищи для щенков.
Обновлено в мае 2019 г. Отправляйте комментарии по адресу [email protected]
Поглощение липидов — обзор
Липиды
Поглощение жира энтероцитами начинается с эмульгирования и растворения холестерина в просвете кишечника липидами и солями желчных путей. Большинство клинических нарушений, связанных с мальабсорбцией жира, возникает в результате тяжелого заболевания печени, заболевания поджелудочной железы (например, кистозного фиброза) или обширной резекции подвздошной кишки (как при болезни Крона) с потерей энтерогепатической циркуляции желчных кислот.Биопсия кишечника играет ограниченную роль в диагностике этих заболеваний. Однако заболевания, связанные с нарушением транспорта жира внутри энтероцита, хотя и встречаются гораздо реже, но могут привести к вакуолизации энтероцита при биопсии кишечника.
Абеталипопротеинемия, гиполипопротеинемия и болезнь удержания хиломикронов (болезнь Андерсона) имеют много общих характеристик, таких как мальабсорбция жира, низкий уровень липидов в сыворотке крови, неспособность развиваться в детстве, неврологические и зрительные проблемы, возникающие в результате мальабсорбции жирорастворимых витаминов, и (диагностическое) накопление липидных капель в энтероцитах.Эти состояния связаны с нарушениями аполипопротеинов, которые находятся на поверхности хиломикронов. Нативными для кишечника аполипопротеинами являются аполипопротеин (апо) AI, апо A-IV и апо B, который имеет две формы: апо B-100 и апо B-48, обе кодируются одним и тем же геном, расположенным на хромосоме 2. 35 Локализация аполипопротеинов в аппарате Гольджи и вдоль микроворсинок энтероцитов показана с помощью иммуноэлектронной микроскопии. 36
Абеталипопротеинемия — аутосомно-рецессивное заболевание, характеризующееся отсутствием липопротеинов, содержащих апо B.Пациенты страдают диареей и нарушением всасывания жиров, обычно возникающими в течение первых нескольких месяцев жизни, с акантоцитозом и дефицитом жирорастворимых витаминов, что приводит к пигментному ретиниту и неврологическим симптомам. Клиническая неоднородность проявляется в значительном количестве случаев у пожилых пациентов. Уровни холестерина и триглицеридов в сыворотке крови обычно низкие и не повышаются после жирной еды. Наполненные жиром энтероциты отмечаются в биоптатах кишечника натощак, которые при электронной микроскопии имеют неправильный размер и, как правило, не связаны с мембраной (рис.9-1). Во внеклеточном пространстве липидов не наблюдается. Молекулярной основой дефекта является отсутствие микросомального белка-переносчика триглицеридов, ответственного за сборку липопротеиновых частиц и за правильную укладку апо B, что предотвращает его преждевременную деградацию. 37 Биопсия печени в этих случаях обычно выявляет стеатоз, а у отдельных пациентов фиброз переходит в цирроз. 38
Гипобеталипопротеинемия — аутосомно-доминантное заболевание, характеризующееся низким уровнем апо B.Гомозиготные пациенты имеют клинический и биохимический профиль, идентичный таковому у пациентов с абеталипопротеинемией, с энтероцитами, заполненными жиром. Большинство гетерозиготных пациентов асимптоматичны, хотя описаны редкие случаи мальабсорбции липидов в раннем возрасте. 35
Болезнь задержки хиломикронов (болезнь Андерсона) похожа на гомозиготную гипобеталипопротеинемию и абеталипопротеинемию по своим проявлениям в ЖКТ и влиянию на рост, хотя акантоцитоз обычно отсутствует, а неврологические и глазные аномалии гораздо менее серьезны.Кроме того, в отличие от абеталипопротеинемии, уровни триглицеридов в сыворотке крови натощак являются нормальными, а гипохолестеринемия менее выражена. В основе расстройства, как следует из названия, лежит неспособность экспортировать хиломикроны из энтероцитов в молочные железы. 39 Гистологический и ультраструктурный вид аналогичен абеталипопротеинемии, хотя некоторые наблюдатели отмечают, что липидные капли при болезни задержки хиломикронов более однородны и связаны с мембраной, чем при абеталипопротеинемии. 40
Незначительные степени вакуолизации энтероцитов (например, после недавнего кормления) часто встречаются при биопсии кишечника у младенцев; в этих случаях вакуолизация не является ни такой выраженной, ни такой диффузной, как при абеталипопротеинемии или болезни накопления хиломикронов. Кроме того, липидные капли присутствуют в межклеточных пространствах и млечных сосудах после кормления, тогда как они отсутствуют в этих пространствах при нарушениях, вызывающих нарушение транспорта липидов.


